2024年1月3日,专注前沿基因治疗领域的创新型企业信念医药集团(Belief BioMed,BBM)宣布:由其自主研发和生产的BBM-H803 注射液的注册临床研究(CTR20233400)在中国顺利完成首例受试者给药。
热门推荐: A型血友病 , 信念医药 , BBM-H803注射液7月19日,罗氏在国际血栓与止血学会2021年大会(ISTH2021)上公布了A型血友病药物Hemlibra(emicizumab)IIIb期研究的最终分析结果,数据证实了Hemlibra的良好安全性,并与III期HAVEN临床项目一致。
热门推荐: 罗氏 , A型血友病 , Hemlibra截止到目前为止,myPKFiT®是中国首 个且目前唯 一国家药品监督管理局批准支持A型血友病药代动力学(PK)指导下的管理工具,与百因止®配合使用,可降低出血风险,优化患者的治疗效果和药物可及性,提升患者治疗信心并改善依从性,助力患者实现“零出血”的治疗目标。
热门推荐: 武田制药 , A型血友病 , myPKFiT武田中国今日宣布,旗下药代动力学(PK)指导下的A型血友病(先天性凝血因子VIII缺乏)管理工具myPKFiT®正式上市,供熟悉血友病A治疗的执业医疗专业人士(HCP)使用,辅助16岁及以上(体重45 kg及以上)A型血友病患者接受百因止®(注射用重组人凝血因子VIII)的预防治疗。
热门推荐: 药代动力学 , A型血友病 , 武田中国 , myPKFiT2020年第62届美国血液学会年会(ASH)于12月5-8日召开。此次会议上,罗氏公布了来自4项关键HAVEN研究(HAVEN 1-4)中401例A型血友病患者(包括儿童、青少年、成人)的汇总三年随访数据的新分析结果。
热门推荐: 罗氏 , A型血友病 , Hemlibra5月23日,据CDE官网罗氏艾美赛珠单抗注射液的第二个上市申请被受理,笔者猜测此次艾美赛珠单抗在国内申请扩大适应症,用于所有类型A型血友病的出血预防治疗。
 热门推荐:
上市申请
, A型血友病
, 艾美赛珠单抗
热门推荐:
上市申请
, A型血友病
, 艾美赛珠单抗
18日美国联邦贸易委员会(FTC)宣布经过10个月调查,没有证据表明罗氏收购Spark会减慢或终止Spark的A型血友病基因疗法的开发,也不会影响罗氏自己F8模拟物、双特异抗体Hemlibra的可及性。FTC惊奇地发现Spark只是开发血友病基因疗法公司之一,这个收购不仅不会减慢这些药物的开发、反而因为与其它厂家竞争会加速。
热门推荐: 罗氏 , 基因疗法 , A型血友病今天BioMarin宣布将利用其A型血友病基因疗法Valrox的一/二期临床数据和部分三期临床数据在今年年底申请加速审批上市。这个叫做Gener8-1的三期临床20患者中有17位VIII号因子(F8)可以评价,其中8位23-26周F8水平中值超过40 IU/dL。据专家估计这个产品明年中期有望成为首款上市的A型血友病基因疗法。
热门推荐: 辉瑞 , 基因疗法 , A型血友病今日,BioMarin Pharmaceutical公司宣布,基于近日与美国和欧洲监管机构的交流,该公司计划在第四季度向美国FDA和欧盟EMA递交治疗A型血友病的基因疗法——valoctocogene roxaparvovec的监管申请。预计这将是首款进入监管审评阶段的血友病基因疗法。
热门推荐: 基因疗法 , A型血友病 , 因子VIII日前,Sangamo Therapeutics公司和辉瑞公司公布了双方联合开发的A型血友病基因疗法SB-525在1/2期临床试验中获得的最新结果。试验结果表明,SB-525能够剂量依赖性提高凝血因子VIII的水平,并且具有良好的安全性和耐受性。FDA同时授予SB-525再生医学先进疗法(RMAT)认定。
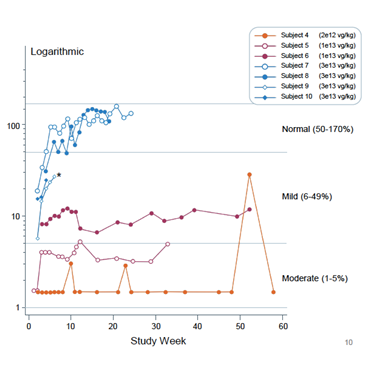
热门推荐: A型血友病 , SB-525 , 凝血因子VIII2019年7月5日,Sangamo/Pfizer公布其在研A型血友病基因疗法SB-525最新I/II期Alta临床数据。本文概述了SB-525 I/II期临床Alta的最新数据,以及A型血友病候选基因疗法Valrox和SPK-8011。
 热门推荐:
Pfizer
, Sangamo
, A型血友病
, SB-525
热门推荐:
Pfizer
, Sangamo
, A型血友病
, SB-525
诺和诺德6月20日宣布,其长效化凝血因子VIIIEsperoct®(turoctocog alfa pegol,N8-GP)获得欧盟委员会的上市许可,用于治疗青少年(≥12岁)和成人A型血友病。该授权涵盖所有28个欧盟成员国。
热门推荐: 诺和诺德 , A型血友病 , Esperoct生物技术公司BioMarin 5月28日宣布,其A型血友病的基因疗法valocogene roxaprovec(valrox)达到了美国和欧盟监管审查的预先规定的临床标准。
热门推荐: 基因疗法 , BioMarin , A型血友病日前,诺和诺德(Novo Nordisk)宣布其在研新药Esperoct(turoctocog alfa pegol,N8-GP)获得FDA批准上市。Esperoct是一款经聚乙二醇(PEG)修饰的长效重组凝血因子VIII(FVIII)。
热门推荐: FDA , A型血友病 , 长效凝血因子今日(12月4日),罗氏宣布舒友立乐®(英文商品名: HEMLIBRA®,化学通用名:艾美赛珠单抗)于日前正式获得国家药品监督管理局(NMPA)的批准,用于存在凝血因子VIII抑制物的A型血友病(先天性凝血因子VIII缺乏)成人和儿童患者的常规预防性治疗,以防止出血或降低出血发生的频率,这也是目前首个可每周一次进行皮下注射的预防性治疗药物。
热门推荐: A型血友病 , 舒友立乐® , 预防性治疗药物罗氏(Roche)集团日前宣布,FDA批准其治疗A型血友病的重磅药Hemlibra(emicizumab-kxwh),作为日常预防性疗法,治疗体内不含因子VIII抑制物的A型血友病患者,为患者预防或减轻频繁出血状况。Hemlibra是目前唯一一款面向体内含有或不含因子VIII抑制物的A型血友病患者,且让患者可以每周、每两周或每四周一次接受皮下注射的预防性疗法。
热门推荐: 新药 , 罗氏 , A型血友病近日,罗氏集团(Roche Group)成员基因泰克(Genentech)宣布了两项关键3期研究(HAVEN 3和HAVEN 4)的数据。
热门推荐: FDA , 基因泰克 , A型血友病4月17日,罗氏制药宣布,美国FDA已授予公司Hemlibra®(emicizumab-kxwh)用于未产生VIII因子抑制剂A型血友病治疗的突破性疗法认定。突破性疗法指定是为了加速那些用于严重疾病治疗且相比现有疗法具有很大治疗改善药物的开发和审查。
热门推荐: 罗氏 , A型血友病 , Hemlibra2018年4月17日,Roche发表声明表示其A型血友病新药Hemlibra获得FDA突破性疗法认定,用于治疗体内不含因子VIII抑制剂的血友病患者的治疗。而2018年4月17日恰好是每30个"世界血友病日"。
热门推荐: Roche , A型血友病 , Hemlibra欧洲药品管理局(EMA)人用药品委员会(CHMP)已经对7种新药在该地区的批准审核时间进行了前移,其中包括A型血友病、糖尿病以及罕见遗传疾病的新治疗选择,这也意味着这些药物有望尽快获得上市许可授权。
热门推荐: EMA , CHMP , A型血友病 直播报名 | 制药行业日常仪器实验操作的安全、规范与维护
直播报名 | 制药行业日常仪器实验操作的安全、规范与维护
 直播报名 | 泛素化-蛋白酶体系统与药物研发
直播报名 | 泛素化-蛋白酶体系统与药物研发
 2024CPHI制药在线买家采购会邀您同启智慧采购之旅!
2024CPHI制药在线买家采购会邀您同启智慧采购之旅!
 2024制药产业线上主题展——天然提取物专场
2024制药产业线上主题展——天然提取物专场
 如何提高药品包装的安全性和可持续性?Syensqo专家在线分享超高阻隔药品包装材料!
如何提高药品包装的安全性和可持续性?Syensqo专家在线分享超高阻隔药品包装材料!
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030