https://www.cphi.cn 2018-01-17 11:36 来源:药渡头条
近日,上海复星医药(集团)股份有限公司控股子公司上海复星医药产业发展有限公司、上海复星星泰医药科技有限公司(原名:上海星泰医药科技有限公司,系复星医药产业之控股子公司)收到国家食品药品监督管理总局关于同意注射用FN-1501临床试验的批准。
FN-1501是由中国药科大学理学院陆涛教授研究团队自主研发的创新型小分子化学药物,该项目以总价五千万元人民币及上市后销售提成一亿元人民币转让给上海复星医药产业发展有限公司,于2017年8月获注册审评受理,近期该药将在美国和中国大陆地区开展临床试验。
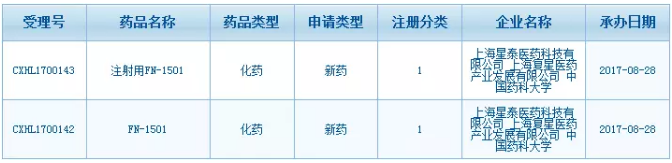
药品名称:注射用FN-1501
剂型:注射剂
规格:10mg
申请类别:化学药品第1类
申请人:复星医药产业、星泰医药、中国药科大学
受理号:CXHL1700143
批件号:2017L05285
审批结论:同意本品进行临床试验
该新药为本集团经中国药科大学转让、后续自主研发的创新型小分子化学药物,主要用于白血病治疗。2017年8月,该新药用于白血病治疗获国家食药监总局临床试验注册审评受理;美国东部时间2017年10月,该新药用于白血病治疗获美国食品药品监督管理局临床试验批准。
截至本公告日,于中国境内(不包括港澳台地区)尚无具有自主知识产权的、与该新药同靶点的药物上市;与该新药同靶点的新药在2017年首次于美国上市,本公司尚无法通过IMS MIDASTM资料获悉与该新药同靶点的新药于全球的年度市场数据。
截至2017年12月,本集团现阶段针对该新药已投入研发费用人民币约3,100万元。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030