2017年12月14日,三叶草生物制药宣布获得由四川天和生物医药产业创业投资基金领投的6280万人民币的A轮融资,用于推进大分子生物药的开发。预计在2018年,公司将有两个产品进入人体临床试验。小编将从三叶草生物的核心技术和研发管线着手,对三叶草生物进行解读。
三叶草生物概况
三叶草生物由董事长梁朋博士2007年在成都创办,致力于创新药及高端生物类似药的研发和产业化。梁朋博士本科毕业于北京大学生物系,80年代经中美交换计划CUSBEA赴美留学,是CUSBEA第二届的学生。在哈佛大学做博士后期间,梁朋博士发明了“基因差异显示技术”,并以此创办了GenHunter公司。之后,基于自己开发的蛋白质三聚体技术,梁朋博士2007年回成都创办了四川三叶草生物制药公司。目前,除了担任三叶草生物的董事长之外,梁朋博士还是四川大学生命科学学院的教授。
三叶草生物制药公司规模虽然不大,但获得了国家十二五重大新药创制科技重大专项及国家863计划重点支持。管理团队的阵容也堪称豪华,共有五名中组部国家“千人计划”入选者,除了梁朋博士本人之外,还有北京生命科学研究所所长及百济神州董事长王晓东博士和天津杰科生物医药研限公司总裁朱建伟博士,以及两名科学顾问张劲游博士和罗顺博士。除了一流的科研团队,三叶草还拥有创新生物制药研发平台Trimer-Tag© ,和符合cGMP要求的生产车间。包括本轮融资,三叶草在2017年累计获得了8430万元人民币的投资,相信可以加速公司手中大分子生物制药产品,包括即将进入人体临床试验的两个产品的研发和推进。
核心技术 Trimer-Tag©
三叶草生物的核心技术在于其Trimer-Tag© (蛋白质三聚体化)平台。许多重要疾病的治疗靶点及其相关信号通路的激活依赖于配体的三聚体化,如肿瘤坏死因子超家族(TNF gene superfamily)以及负责进入宿主细胞的包膜RNA病毒抗原等。三叶草生物主要通过其核心的Trimer-Tag© 技术,将目的蛋白与分泌性全人胶原蛋白C端前肽(C-prodomain peptide)标签融合,通过该标签形成天然的二硫键共价交联的同源三聚体蛋白,用以靶向那些天然需要三聚体配体来激活的疾病靶点。
与传统的单克隆抗体药物或重组蛋白药物相比,Trimer-Tag© 技术下的三聚体融合蛋白有以下几点优势:
1. 天然共价交联的三聚体结构更利于激活需要三聚体配体-受体结合的靶点。与之相比,单克隆抗体/Fc-融合蛋白为非天然的二聚体结构,并不能有效地激活需要三聚体的信号通路,这也许是为什么之前许多TRAIL相关的抗体药物在临床测试中并没有良好表现的原因之一。此外,一些天然人重组三聚体蛋白由于是非共价交联的结构,本身结构不稳定,也无法有效地激活下游信号通路。相比之下,Trimer-Tag© 构建的天然共价交联的三聚体融合蛋白更能稳定有效地激活目标靶点。
2. 全人的蛋白氨基酸序列,**或免疫原的可能性较低。Trimer-Tag© 使用的标签为能够自身以二硫键共价稳固三聚化的胶原蛋白原C端前肽,主要来源于原纤型胶原蛋中的pro.α.1(I)、pro.α.2(I)、pro.α.1(II)、pro.α.1(III)、pro.α.1(V)、pro.α.2(V)、pro.α.1(XI)、pro.α.2(XI)和 pro.α.3(XI)。胶原蛋白是哺乳动物体内最丰富的蛋白质,其中胶原蛋白的三聚C端前肽在血液中天然为亚微克/毫升水平,并且未知对身体有**。因此,使用胶原蛋白原C端前肽作为标签的三聚体融合蛋白可能的人体**或免疫原性较低,而不像此前使用非人源性亮氨酸拉链(leucine zipper)标签或His标签的三聚体蛋白一样有较强的肝**。
3. 保留可变区目的蛋白天然的氨基酸顺序和功能。由于三聚体化是由通用的胶原蛋白C端前肽实现,因此不需要改变可变区蛋白的氨基酸序列,此外可变区的蛋白质与胶原C-前肽间的距离可以通过胶原的线性三股螺旋区来精确调节,以实现其生物活性。这为Trimer-Tag© 的灵活应用提供了可能性。
4. 药物动力学优化,通过修饰胶原蛋白C端前肽标签,延长融合蛋白的半衰期。之前天然人重组三聚体蛋白被发现在哺乳动物中半衰期非常短,有可能是因为其分子量小且非共价交联的结构不稳定导致了被肾滤过清除。Trimer-Tag© 中使用的标签一方面增大了融合蛋白的分子量,另一方面通过共价交联提高了蛋白的稳定性,有助于其半衰期的延长。此外,在一些情况下,胶原蛋白C端前肽标签上的BMP-1蛋白酶识别序列发生了突变或缺失,进一步有助于融合蛋白在体内稳定性的提高。
目前,Trimer-Tag© 已有全球专利保护(美国、欧洲、日本、中国),三叶草生物从梁朋博士在美国创办的GenHunter公司获得了用Trimer-Tag© 进行药物研发的独家授权。
从三叶草生物制药的研发管线布局可以看到,三叶草生物应用Trimer-Tag© 技术,重点发展领域为肿瘤治疗和自身免疫性疾病,此外,在重组**这一领域也在进行前期研发和寻求合作机会。
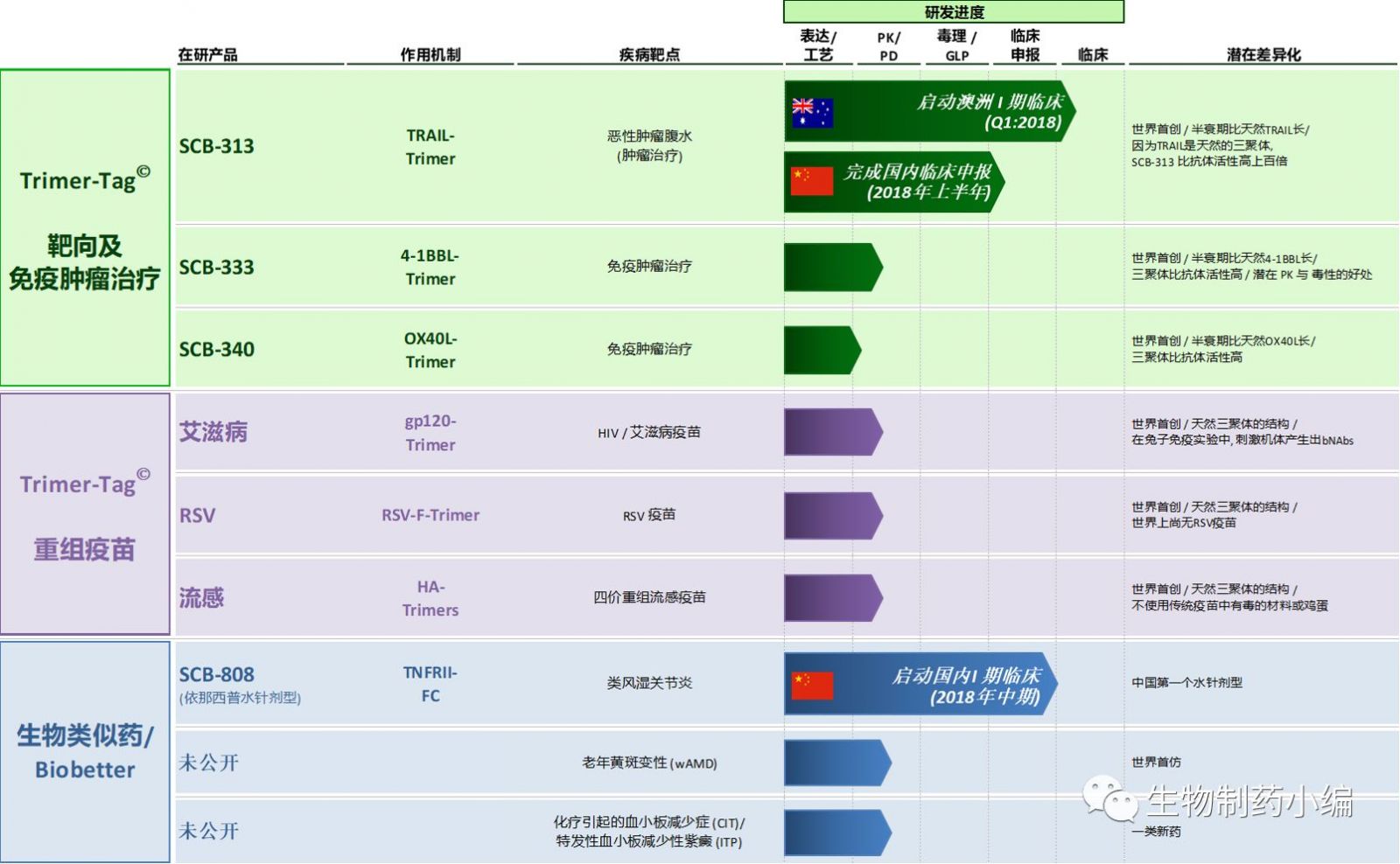
肿瘤治疗
目前,三叶草生物制药临床研究进展最快的是重组人肿瘤坏死因子相关凋亡诱导配体(TRAIL)三聚体融合蛋白(SCB-313),预计在2018年初在澳洲进入I期临床试验,并计划在2018年上半年完成国内临床申报。
TRAIL, 也被称为Apo2L,可以通过结合受体DR4或DR5(也被称为TRAIL-R1及TRAIL-R2)而诱导受体三聚体化并特异性地诱导肿瘤细胞凋亡。
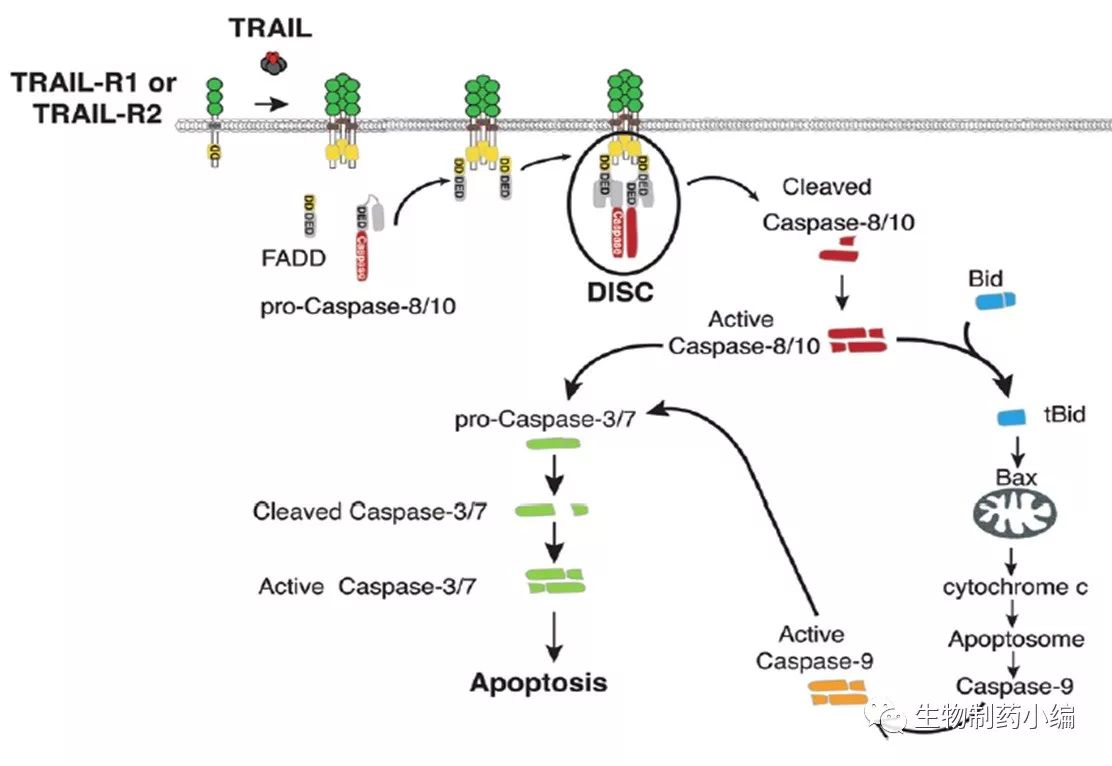
△源自H. Belkahla et al. Nanoscale, 2017,9,5755
由于其特异性杀伤肿瘤细胞的特性,TRAIL的受体DR4和DR5很早就被视为有潜力抗癌药物靶点并被寄予厚望。然而,此前不管是针对DR4的单克隆抗体药物Mapatumumab (HGS-ETR1),还是针对DR5的单克隆抗体药物Conatumumab (AMG-655),Lexatumumab (HGS-ETR2),Tigatuzumab (CS-1008),Drozitumab (PRO95780/ apomap) 及LBY-135,都因为没有明显的抗肿瘤效果而纷纷止步于I期或II期临床试验。由于DR4及DR5的激活需要受体的三聚体化,因此这些二聚体化的抗体药物没有明显的临床效果也在意料之中。然而,Amgen的可溶性重组人肿瘤坏死因子相关凋亡诱导配体药物Dulanermin (AMG-951/rhApo2L)尽管拥有天然的TRAIL三聚体结构,也没有在临床试验中有很好的表现。这可能是因为Dulanermin的分子量太小以及非共价交联的结构不稳定,导致其在人体内半衰期太短而对肿瘤没有疗效。虽然可以通过人为地给TRAIL添加标签,如亮氨酸拉链标签(izTRAIL)及N端His标签(SuperKillerTRAIL)来稳定TRAIL并延长其半衰期,然而融合了这些非人源性的标签的TRAIL都展现了较强的肝**,不适于进一步人体试验。
三叶草生物的SCB-313应用Trimer-Tag© 技术将人源TRAIL与人源胶原蛋白α1(I)C端前肽融合形成了由二硫键共价交联的分泌性三聚体蛋白,并在中华仓鼠卵巢细胞(CHO)中高表达产生。与二聚体TRAIL-Fc相比,SCB-313,也就是TRAIL-Trimer的体外生物活性和结合受体能力提高了4个数量级。另一方面,虽然TRAIL-Trimer与天然三聚体TRAIL相比体外生物活性相当,但得益于Trimer-Tag© 的作用,其在老鼠体内的半衰期是天然三聚体TRAIL的三倍,并在裸鼠移植瘤模型中体现了更好的肿瘤杀伤力。安全性方面,TRAIL-Trimer和天然三聚体TRAIL一样表现出了低**,在人源肝细胞、裸鼠以及猕猴体内都没有表现出肝**。
总而言之,SCB-313作为世界首例人源胶原蛋白重组三聚体化TRAIL靶向药物,通过Trimer-Tag© 技术,既兼顾了天然TRAIL的低**,又克服了其不稳定半衰期短的问题,与此同时,TRAIL-Trimer比之前二聚体结构的TRAIL抗体生物活性既受体结合能力高出4个数量级,临床效果值得期待。当然,基于此前对TRAIL信号通路的研究,有许多种情况可能阻断TRAIL诱导的肿瘤细胞凋亡,如肿瘤细胞过表达TRAIL-R3/R4、cFLIP、IAP、Bcl-2,或者缺失Bax及Bak等。因此TRAIL临床上的有效性也要依赖于进一步对TRAIL适用型肿瘤生物标记的研究。
除了TRAIL-Trimer,三叶草制药在研的三聚体药物还有靶向4-1BB的SCB-333(4-1BBL-Trimer)和靶向OX40的SCB-340(OX40L-Trimer)。这两种药物都是通过刺激T细胞活化和增殖来达到杀伤肿瘤的作用。这两种药物都是应用Trimer-Tag© 技术来构建的三聚体融合蛋白,目前还在较为早期的研发阶段。
自身免疫性疾病
除创新型药物外,三叶草生物研发管线中另一个重要领域是生物类似药的研发。其中,用于治疗类风湿性关节炎和其他自身免疫性疾病的Enbrela(依那西普)生物类似药SCB-808预充填小容量注射液已经获得CFDA的临床批件,预计在2018年中期进入中国I期临床试验。依那西普是类风湿性关节炎和其他自身免疫性疾病患者的一线靶向用药之一,2016年的全球销售额超过600亿人民币。中国市场上的依那西普生物类似药都是冻干粉制剂型,需要在医务人员的协助下用注射用水进行溶解后才能注射使用。SCB-808作为中国首例水针剂型依那西普注射液,一方面价格可能仅为原研药的1/5,另一方面有可能让患者或家属在家自行注射使用,使用更为方便。
此外,三叶草生物也在进行针对化疗引起的血小板减少症(CIT)、特发性血小板减少性紫癜(ITP),以及老年黄斑变性(wAMD)进行生物类似药的早期研发,具体的产品信息尚未公开。
重组**
从三叶草研发管线布局看,三叶草生物也想利用Trimer-Tag© 技术开发针对有三聚体抗原的病毒的**,主要包括艾滋病(HIV-1),呼吸道合胞病(RSV)和流感。到目前为止,已有一些初步的理论或数据表明三聚体抗原**可能更有效地刺激抗体的产生。三叶草生物正在寻找潜在的合作者共同开发三聚体**项目。
总结
三叶草生物是为数不多的拥有核心技术(Trimer-Tag© )创新生物药研发平台及自身cGMP生产能力的生物制药公司之一。其三聚体技术开发的肿瘤靶点药物与传统的抗体药物和重组蛋白靶点药物相比,理论上有更好的效果,目前即将在澳洲进入I期临床试验。如果此次临床获得较好的结果,可以想象三叶草制药作为一家走在三聚体靶点药物开发最前沿的创新型公司,将吸引更多投资者的目光。








合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57