https://www.cphi.cn 2018-01-31 10:43 来源:药渡网 作者:杨柳青
序言
近年来,随着CFDA大刀阔斧的改革:仿制药一致性评价、新的药品注册分类、MAH制度的落地等;这些除旧布新的药品监管政策正在打破一个旧的世界,建立一个新的未来。中国正处于万众创新的大环境,新药研发在各种政策支持下,也越发显得活跃。本系列文章将介绍小分子新药口服固体制剂的开发技术和流程。
处方前研究
一旦一个新苗头化合物通过一系列细胞和动物试验,初步确认其有较好的生物活性后,即可开始着手准备临床试验的申请。由于临床试验是在人体上进行相关有效性、安全性的评价,故其需要开发合适的给药途径和剂型,即新药制剂的开发。在正式开始制剂处方、工艺开发之前,需要对新化合物的主要性质进行考察,即处方前研究。
成盐性和多晶型
新化合物的固体形态(盐型和晶型)会影响其稳定性、溶解性、溶出速率、临床疗效和制剂的处方工艺等。由于化合物一般为游离酸或碱,其往往溶解度较差,影响生物利用度,所以需要对新化合物进行盐筛。在开始筛盐之前需要明确成盐的目的:是为了改善溶解度和生物利用度,还是为了提高产品的稳定性、工业化可开发性等;然后通过相关目标的评价指标进行筛选。当新化合物或其盐的溶解度和生物利用度均满足要求,此时需要进一步筛选其晶型,以便选出稳定性和工业化可开发性的优势晶型。新化合物盐型和晶型筛选、评估流程如下图:
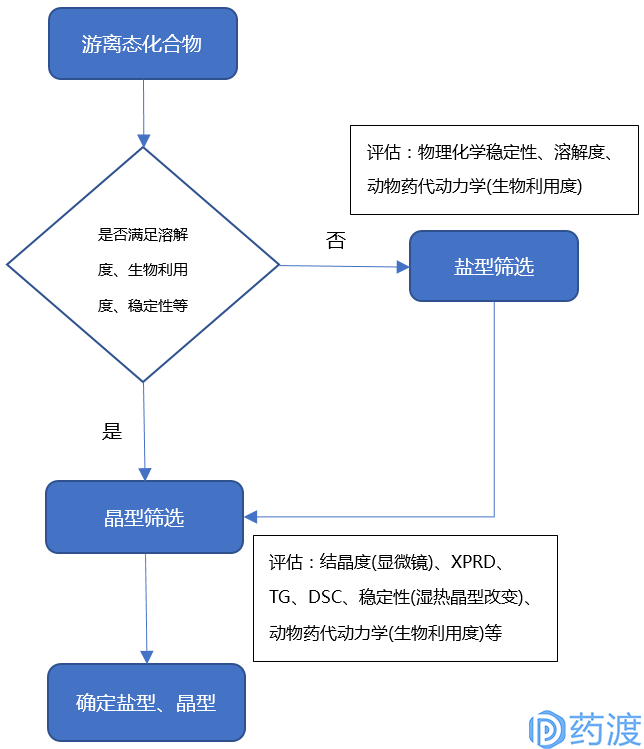
盐型比游离酸(碱)具有更高的初始溶解度和吸收速度,即使溶解后的盐型在生理PH条件下盐型会变成游离酸(碱)沉淀,但该沉淀过程可产生细小的无定型沉淀,导致更高的初始溶出和吸收速度。成盐的反离子应与相应化合物的PKa相差大于2,一般2-3为宜,这样保证盐型的溶解度远大于游离化合物。使用FDA已批准过的反离子,否则需要提供反离子的完整毒理学数据。
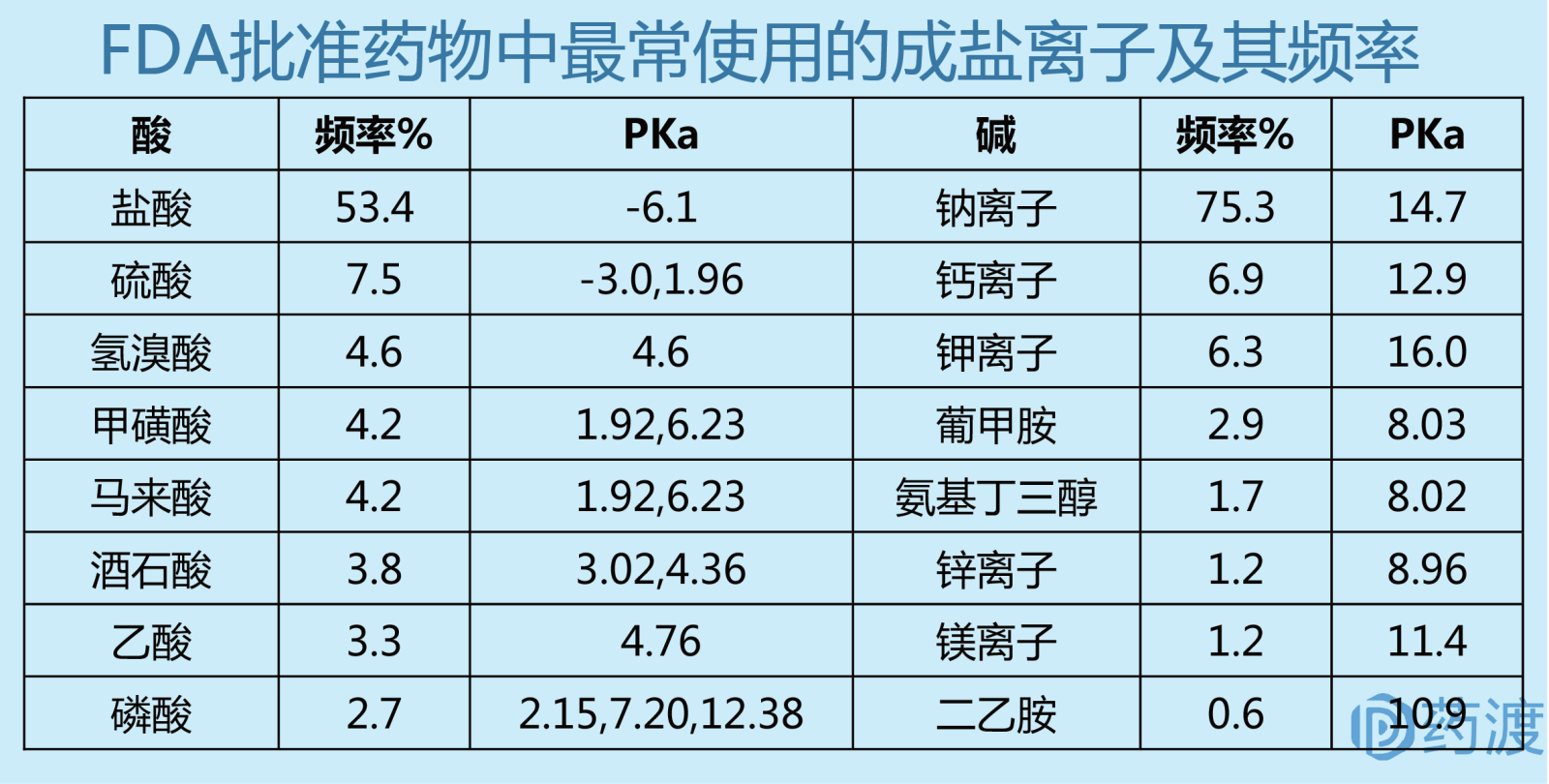
溶解度和溶液稳定性
药物发现阶段,为了增强与靶蛋白结合能力,化合物一般具备较强的亲脂性,所以在药物开发的后期,化合物溶解度往往是比渗透性大得多的问题,低溶解度往往会导致差的生物利用度。对于确定晶型和盐型的化合物需要测定其PH-溶解度曲线,以便为制剂处方工艺的开发策略提供指导。FDA指南《Waiver of In Vivo Bioavailability and Bioequivalence Studies for Immediate-Release Solid Oral Dosage Forms Based on a Biopharmaceutics Classification System Guidance》提供了化合物PH-溶解度曲线试验方法:

同时,为了解析化合物在不同生理PH条件下的稳定性,需考察PH 1-6.8介质下化合物的溶液稳定性,具体可参考ICH Q1。
通过测定不同生理PH条件下的溶解度,判断化合物溶解度是否为PH依赖型,溶解度是否满足BCS分类对高溶解度的定义;如是低溶解性化合物,可能制剂开发需要考虑API微粉化或添加增溶剂。同时通过PH-溶解度曲线和溶液稳定性试验,可以为制剂溶出条件和制剂开发提供帮助,如溶出PH条件的选择,是否需要添加表面活性剂,是否需要做成肠溶片等。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030