https://www.cphi.cn 2018-03-14 09:59 来源:转载
在“两票制”、《药品管理法》修订、GSP认证制度取消、监管部门检查人员职业化、医药监管线上线下并行等一系列政策的出台并推行下,医药流通企业经营压力越来越大,合规成本也越来越高,违法成本越来越大。
2017年相关监管部门为贯彻落实“四个最严”的要求,政策层出不穷。而对于医药流通企业而言,2017年可以说是摸着石头过河。
进入2018年,企业需要适应政策变化,改变经营理念,提高合规意识,才能越走越远。为此,笔者对2017年医药流通重要政策法规进行梳理及浅析。
整治整合医药批发
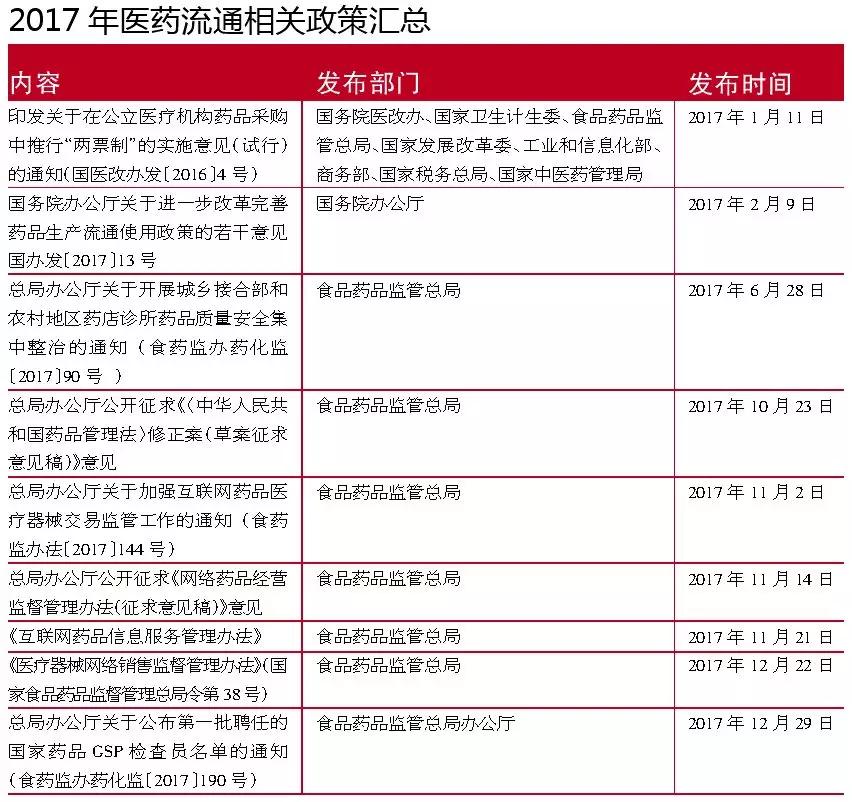
2017年1月,国务院医改办、国家卫生计生委、食品药品监管总局等八部委共同制定了《关于在公立医疗机构药品采购中推行“两票制”的实施意见》(试行),此意见定义了“两票制”实施的范围和推行时间。自此,各省就公立医疗机构执行“两票制”陆续拉开了序幕。
“两票制”的执行无疑是对医药流通企业的一次“洗牌”,对于以公立医院为主要客户群体的中小型医药企业是一种压力。同时,相关监管部门利用“两票制”的契机,加强了对医药批发企业的监管。
“两票制”规定出台后不久,2017年2月9日,国家食药监总局发布《国务院办公厅关于进一步改革完善药品生产流通使用政策的若干意见》(国办发〔2017〕13号),进一步明确推进药品流通体制改革的目的是要培育大型现代药品流通企业,鼓励大型企业兼并中小企业,同时再次强调“两票制”要在2018年全面推开,要求药监部门重点严厉打击租借证照、虚假交易、伪造记录、非法渠道购销药品、伪造或虚开 发 票等违法违规行为。
在行业整合和监管趋严的背景下,中小型医药流通企业的发展可谓举步维艰。
监管延伸到零售
2017年6月,国家食药监总局发布《总局办公厅关于开展城乡结合部和农村地区药店诊所药品质量安全集中整治的通知》(食药监办药化监〔2017〕90号),这是继2016年5月总局发文重点整治医药批发企业后,针对零售终端开展的专项整治。其提出整治重点包括企业违法回收药品,超范围经营药品,购进药品未索取发票,违规销售含特殊药品复方制剂、米非司酮等具有终止妊娠作用的药品等内容。这场整治淘汰了不少药店,其中不乏一些大型连锁企业的药店。
进一步完善“互联网+”
随着“互联网+”行动的不断推进,药品医疗器械产业与互联网融合不断加快,药品医疗器械网络销售日趋活跃。
在此环境下,2017年11月、12月,国家总局分别发布了《网络药品经营监督管理办法》(征求意见稿)、《互联网药品信息服务管理办法》、《医疗器械网络销售监督管理办法》(国家食品药品监督管理总局令第38号),监管由线下继续向线上延伸。
其中,《网络药品经营监督管理办法》以六章共57条内容,规定了网络药品的销售管理、交易服务平台管理需要的硬件、软件等内容。《医疗器械网络销售监督管理办法》的出台则填补了医疗器械网络销售监管的空白,不仅明确了器械网络销售企业、器械网络交易服务第三方平台提供者的法律责任,还规定了相关责任人的惩戒措施。
药品检查员职业化
继2016年底国家级药品检查员颁证及宣誓仪式后,2017年12月底,国家食药监总局办公厅聘任并公布了第一批国家药品GSP检查员名单,这为日后取消GSP认证、加强事后监管提供了人力保障。此后,148名GSP检查员将奔赴全国各地的医药经营企业开展各项检查。未来,医药流通企业将随时被飞检。
修订核心法律适应需求
2017年10月国家食药监总局办公厅发布《<中华人民共和国药品管理法>修正案(草案征求意见稿)》意见。其中,直接关系到医药流通企业的关键内容包括:
一是取消药品经营质量管理规范认证制度。也就是取消GSP认证的制度,日后将不会核发GSP证书,实行药品许可证与GSP证合二为一,采用日常监管替代GSP认证。待正式修订稿落地,一旦企业违规,撤证风险将会大大增加。
二是增加药品职业化检查制度。这是为日后提高检查的专业性、合法性提供保障。
三是落实处罚到人。对存在资料数据造假和被吊销许可证的单位及其直接负责的主管人员和其他直接责任人员,十年内行业禁入。因药品安全犯罪被判处有期徒刑以上刑罚的人员,终身不得从事药品的研制、生产、经营、进出口活动。作为公司直接负责管理的人员或直接责任人,一旦为了谋取经济上的利益而做了违法违规的事,不仅饭碗丢了,还会在医药行业寸步难行,甚至终止医药职业生涯。药品上市许可持有人、研制单位、生产企业、经营企业、医疗机构故意实施违法行为或存在重大过失,或者违法行为情节严重、性质恶劣或造成严重后果以及其他严重不良社会影响的,对单位直接负责的主管人员和其他直接责任人员处以其上一年度从本单位取得的收入百分之三十以上一倍以下罚款。可见,企业违法的成本高了,而与企业关联的责任人担负的责任也更大了。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030