https://www.cphi.cn 2018-05-07 14:36 来源:学术经纬 作者:药明康德
全世界范围内,新型抗生素的缺乏已经带来了严重的公共卫生危机,而针对革兰氏阴性菌的抗生素新药研发则一直困难重重。在最新一期的《自然》杂志上,科学家们面对这一难题做出了突破。
在介绍这项研究前,我们先来了解一下革兰氏阴性菌。这类细菌的致病性更高,常见的大肠杆菌就属于这一范畴。与革兰氏阳性菌不同,革兰氏阴性菌有两层细胞膜(外膜与内膜)。因此,想要有效地针对革兰氏阴性菌,抗生素需要穿透的防护要来得更多。
在革兰氏阴性菌体外,一类叫做脂多糖(lipopolysaccharide)的物质是挡在抗生素面前的一大障碍。而将脂多糖运输到革兰氏阴性菌表面,又离不开一种叫做MsbA的转运蛋白。因此,研究人员们自然而然地想到,如果我们能抑制MsbA的功能,也许就能带来新型抗生素研发上的转机。
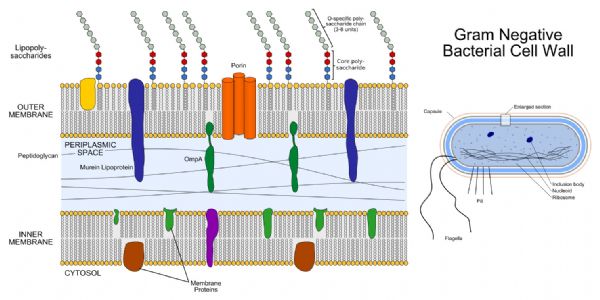
革兰氏阴性菌有着复杂的细胞膜结构
从300万个候选药物中,研究人员们筛选出了多个能特异抑制大肠杆菌MsbA的小分子。利用X射线晶体衍射的方法,他们又进一步获得了MsbA与这些小分子抑制剂结合时的高清结构,分辨率达到了2.9?。而这些高清结构也为后续的研究带来了洞见——研究人员们发现,一款代号为G907的小分子抑制剂能与MsbA多个保守跨膜域之间的空间契合,而结合了G907的MsbA无法完成执行生理功能所需的关键构象转变。这从结构上回答了G907的一大抑制机理。
有趣的是,进一步的研究发现,G907居然还有第二种抑制MsbA的机制。在细菌中,MsbA的正常工作需要水解ATP产生的能量,因此MsbA结构中的核酸结合域(nucleotide-binding domain)对其功能而言至关重要。而G907与MsbA的结合,可以影响到核酸结构域,从而对MsbA产生变构上的抑制。
研究人员们指出,这项研究有望用于一大类转运蛋白抑制剂(统称ATP结合盒转运蛋白,或ABC转运蛋白)的设计。与常规的ABC转运蛋白抑制剂不同,G907及其类似物并不会与转运的底物发生竞争性抑制,而是通过结构上的抑制,影响MsbA的功能。
在文章的最后,研究人员们也提到,ABC转运蛋白家族成员具有较高的结构保守性,这项研究有望带来全新的选择性抑制剂,为新型抗生素的研发提供洞见与协助。我们期待创新抗生素能早日问世,为全球公共卫生做出贡献!
原始出处:
Hoangdung Ho,et al.Structural basis for dual-mode inhibition of the ABC transporter MsbA.Nature.02 May 2018
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030