今日(9月21日),辉瑞(Pfizer)宣布其在研候选**PF-06482077,获得FDA授予的突破性疗法认定。PF-06482077是一款20价肺炎链球菌偶联(20vPnC)**,将用于在18岁以上的成人中预防由肺炎链球菌感染引起的肺炎和侵袭性疾病。此前,FDA已于去年10月授予该候选**“快速通道资格”。
肺炎链球菌是一种柳叶状、革兰氏阳性、兼性厌氧菌,有超过90种血清型。这一细菌能引起肺炎、脑膜炎、血液感染、与鼻窦感染等严重症状。据美国疾病控制与预防中心(CDC)估计,每年约有90万名美国人受该细菌引起的肺炎困扰,并造成40万人次住院。此外,每年有18000名老人死于和肺炎链球菌感染相关的疾病。
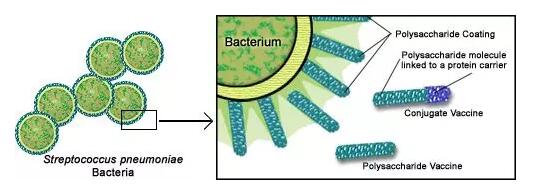
肺炎链球菌偶联**结构示意图
偶联**(conjugate vaccine)是通过化学方法将多糖或寡糖抗原,偶联到蛋白质载体上。它能够更好地刺激成人与儿童的免疫反应,从而促使B细胞生产IgG抗体。偶联**有望对多种传染性疾病的预防产生重要作用。
此次突破性疗法认定的授予是基于该20vPnC候选**的2期临床试验结果。这项随机双盲的2期试验,评估了多价肺炎链球菌偶联**,用于60至64岁成人中的安全性和免疫原性。辉瑞计划近期公布这一试验的具体结果,并于几个月内开展3期实验。
辉瑞**研发部主任,高级副总裁Kathrin U. Jansen博士说:“辉瑞期待保持与FDA对话,以期加快这一新一代,适用于成人的20vPnC候选**的开发计划。全球保健行业仍然需要防护手段,以避免肺炎链球菌引起的侵袭性疾病和肺炎的潜在破坏性影响。我们将基于这款候选**继续积累在偶联**方面的专长。”








合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57