2023年,一共49种新药(不包括疫苗和基因疗法)在美国、欧盟和日本首次获批。其中,40个药物有明确的作用机制靶点。其中,有12个新颖的以前没有被批准的药物调节的靶点。见表1。
表1 2023年批准的具有新作用机制靶点的药物(表格来源于nature)
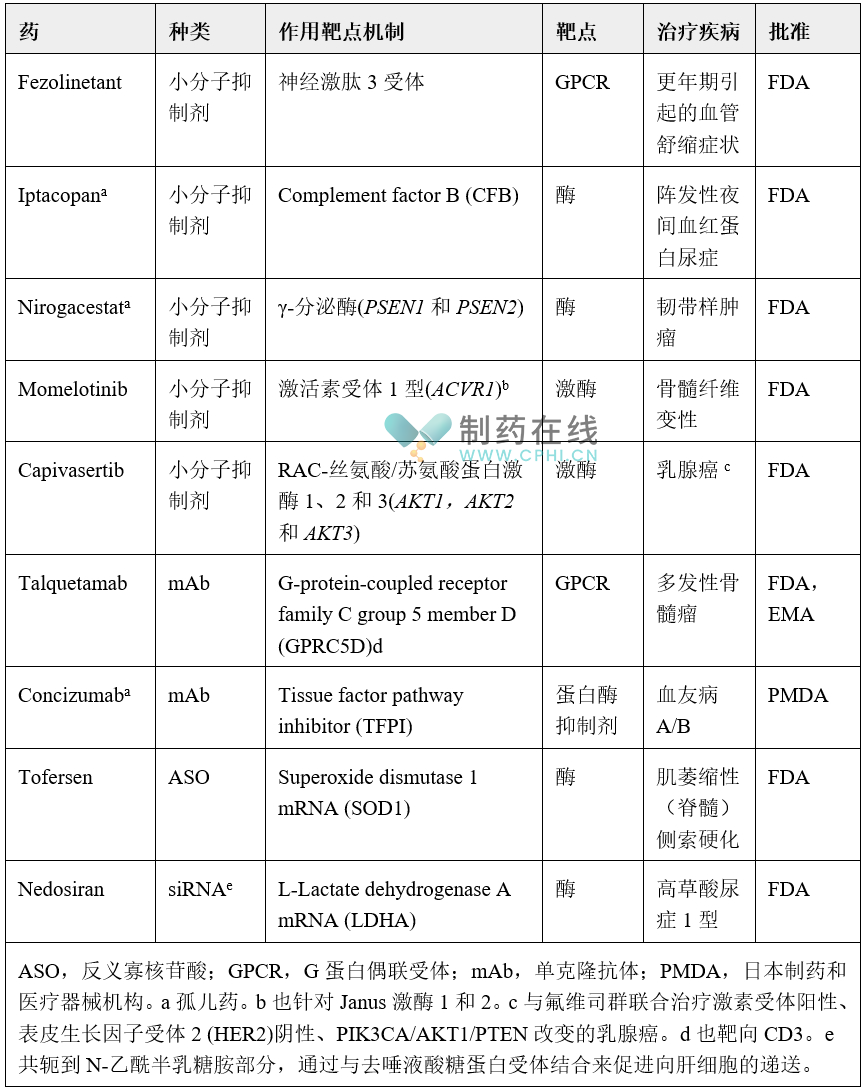
九种具有新靶点的药物中有五种是小分子药物。其中包括一种G蛋白偶联受体拮抗剂和四种酶抑制剂,它们总共有七个新靶点(其中四个是激酶)。
第一款神经激肽3受体拮抗剂Fezolinetant被批准用于治疗menopausal hot flashes。这种药物通过阻断下丘脑中神经激肽B的结合来调节体温,是第一个用于治疗该适应症的非激素疗法。Fezolinetant(VEOZAH)由Astellas Pharma Inc .开发用于治疗中度至重度血管舒缩症状(VMS)或menopausal hot flashes。抑制中枢神经系统中NK3R介导的信号传导是一种调节与体温调节相关的神经元活性的非激素策略,从而降低VMS的频率和严重程度。Fezolinetant于2023年5月在美国首次获得批准,用于治疗因绝经引起的中度至重度VMS。
Iptacopan抑制替代补体途径中的Factor B inhibitor,是第一种用于阵发性夜间血红蛋白尿症患者的口服单药疗法。Iptacopan (FABHALTA® ) 是诺华制药公司开发的一种口服Factor B inhibito。2023年12月5 日,iptacopan 在美国获得批准用于治疗成人阵发性睡眠性血红蛋白尿症 (PNH)。
Nirogacestat是一种γ-分泌酶抑制剂,可防止Notch受体的蛋白水解激活,是第一个获准用于治疗韧带样瘤的药物,由SpringWorks Therapeutics,Inc .开发。Nirogacestat可切割多个跨膜蛋白复合物,包括Notch和膜结合B细胞成熟抗原(BCMA)。抑制γ-分泌酶可能导致过度表达Notch的肿瘤细胞的生长抑制,保留膜结合BCMA可能增加BCMA靶向治疗的靶密度。2023年11月,nirogacestat在美国获批用于需要全身治疗的进展性韧带样瘤成年患者。
另外两种药物也被批准用于癌症治疗,这两种药物都是激酶抑制剂。Capivasertib是一种口服小分子pan-AKT抑制剂,由阿斯利康开发,用于治疗各种癌症,包括乳腺癌和前列腺癌。Capivasertib于2023年11月在美国首次获得批准,用于患有一种或多种局部晚期或转移性乳腺癌的成年患者。Capivasertib还在欧盟和其他几个国家接受HR阳性、HER2阴性乳腺癌的监管审查,并在III期临床开发中用于(与其他抗癌药物联合)治疗三阴性乳腺癌、去势抵抗性前列腺癌和激素敏感性前列腺癌。
Momelotinib被批准用于骨髓纤维化伴贫血的患者,是第四种被批准用于骨髓纤维化的Janus激酶1/2(JAK1/2)抑制剂,但也是第一种抑制活化素A受体1型(ACVR1)的药物,可促进红细胞生成增加以改善贫血。2023年9月,Momelotinib美国获批用于治疗中度或高危MF,包括成人贫血的原发性MF或继发性MF。
两种获得批准的基于抗体的疗法利用了新的药物靶点。Talquetamab是一种双特异性抗体,可与多发性骨髓瘤细胞表面的GPRC5D和T细胞上的CD3结合,促进T细胞介导的癌细胞杀伤。2023年8月初,Talquetamab在美国获得加速批准,用于治疗成人复发或难治性MM,2023年8月下旬,Talquetamab在欧盟获得有条件上市许可,用于治疗成人RRMM患者。Concizumab是日本药品管理局在该清单中批准的唯一一种药物,适用于甲型和乙型血友病。这种单克隆抗体与组织因子途径抑制剂(TFPI)结合,破坏对活化因子X的抑制,从而促进止血。2023年3月,加拿大批准concizumab用于治疗患有B型血友病的青少年和成人患者(12岁或以上),这些患者使用FIX抑制剂,需要常规预防以防止或减少出血事件的频率。
还有两种新的寡核苷酸药物具有新的靶点,这两种药物都被批准用于罕见疾病。Tofersen是一种促进超氧化物歧化酶1mRNA降解的反义寡核苷酸(ASO),被批准用于治疗肌萎缩侧索硬化症患者。Nedosiran(RIVFLOZA)正在由诺和诺德公司的Dicerna Pharmaceuticals开发,用于治疗原发性高草酸尿症(PH)。它通过抑制肝乳酸脱氢酶(LDH)的表达来减少草酸盐的过量产生。Nedosiran于2023年9月29日在美国首次获得批准,用于降低9岁以上儿童和PH1型且肾功能相对保留的成人的尿草酸盐水平。
总体而言,治疗罕见疾病的药物解决了八个新的作用机制靶点。
[1]https://www.nature.com/articles/d41573-024-00057-9








合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57