https://www.cphi.cn 2018-02-05 09:50 来源:CPhI制药在线 作者:小药丸
1月25日,CFDA发布了《总局关于适用国际人用药品注册技术协调会二级指导原则的公告》,按照公告的要求,自2月1日起,国内1类、5.1类化药及1类治疗/预防用生物制品的注册申请将适用ICH的指导文件《M4:人用药物注册申请通用技术文档(CTD)》。据悉,CFDA此举的目的 在于推动我国药品注册技术标准与国际接轨。
早在2010年9月,CFDA发布了《关于按CTD格式撰写化学药品注册申报资料有关事项的通知》,其中提及到了"化学药品注册分类3、4、5和6的生产注册申请的药学部分申报资料,可参照印发的CTD格式整理提交"等相关内容,后续又出台了多项关于CTD格式申报资料技术审评的相关要求。需要说明的是,始于2010年的这些指导文件并非是强制性要求,而是鼓励制药企业按照CTD的格式撰写和提交申报资料,在实际操作中,申报人可以进行自主选择。
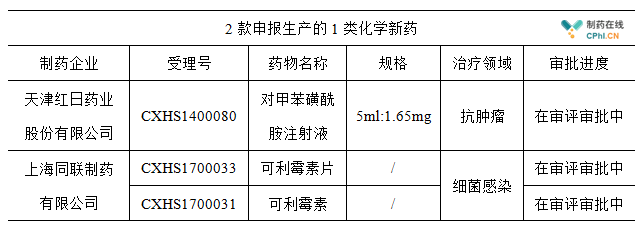
2018年1月,国内共有两款1类化学新药提交了注册申报,分别是天津红日药业的对甲苯磺酰胺注射液以及上海同联制药的可利霉素及片剂, 赶在了1月25日CFDA《公告》规定的ICH指导文件适用的开始时间之前,申报人至少可以按照原有的申报格式进行申报资料的撰写和提交。
需要说明的一点是,1月提交注册申请的上述这两款1类新药均不是首次申报国内上市。
对甲苯磺酰胺注射液
早在2009年4月,对甲苯磺酰胺注射液项目(CXHS1400080)的Ⅲ期临床获得了《药物临床试验批件》,批件号2009L03443,适应症为严重气道阻塞的中央型非小细胞肺癌;在2015年的722临床数据自查中,天津红日药业与红日健达康共同主动撤回了该在研新药的注册申请,理由是考虑到"CFDA出台的最新有关药品的审评审批政策而审慎作出的决定"。
此次申请是该在研新药继2015年撤销之后首次提交的上市申请。
可利霉素及片剂
可利霉素属于大环内酯类抗生素,该在研药物是全球首个通过合成生物学技术开发的抗生素新品种。鉴于早期研究中在抗感染方面安全性及有效性的不俗表现,该在研抗生素拟用于阿奇霉素的替代产品。
2010年,可利霉素的上市申请并没有获得CFDA的批准,此次申请属于再次申报上市的情况。
作者简介:小药丸,制药行业从业者,自媒体时代的文字搬运工,专注于制药圈内的阴晴冷暖。
版权所有,未经允许,不得转载。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030