https://www.cphi.cn 2020-04-28 08:54 来源:新浪医药新闻
4月27日,CDE官网显示,四川普锐特药业按照新注册分类4类递交「吸入用布地奈德混悬液」的上市申请,并获药审中心承办(受理号:CYHS2000278)。

布地奈德混悬液属吸入性糖皮质激素,通过雾化器给药,原研是阿斯利康的普米克令舒。在2000年8月获美国FDA批准上市,我国于2001年11月批准进口,规格为0.5mg/2ml、1mg/2ml。
在慢阻肺、哮喘领域的治疗药物上,主要有气管舒张剂、激素类药物、磷酸二酯酶-4抑制剂等。目前,全球哮喘和慢阻肺用药市场中,约有80%份额由吸入剂型所占据。其中,布地奈德属于糖皮质激素吸入剂,是目前我国市场规模较大的哮喘治疗代表品种。
与其他治疗哮喘的药物相比,布地奈德及其复方制剂在我国哮喘临床用药领域具有绝对的领先优势。与普通的吸入溶液不同,混悬液被称为吸入类产品的「皇后」,研制技术难度较高,故而吸入制剂的市场集中度相对较高。
目前,我国上市的布地奈德及其复方制剂(布地奈德福莫特罗)共有8个品种,其中Astra Zeneca就拥有4个品种。公开数据显示,2017年 Astra Zeneca的这4个品种合计占我国布地奈德及其复方制剂市场份额的 99% 以上。
2020年2月26日,正大天晴成功拿下布地奈德混悬液国内首仿,获批规格为2ml:1mg,一举打破原研国内长达20年垄断的局面。目前,正大天晴的布地奈德混悬液已经成功挂网,Insight 数据库显示在3月份的挂网价为386.40元/盒,而同规格原研的中标价为429.60元/盒。
Insight 数据库显示,目前按新4类提交布地奈德混悬液上市申请的还有深圳太太药业和长风药业,其中深圳太太药业第一轮补充资料已经完成,顺利的话有望今年Q3获批,此外长风药业上市申请在审评中。
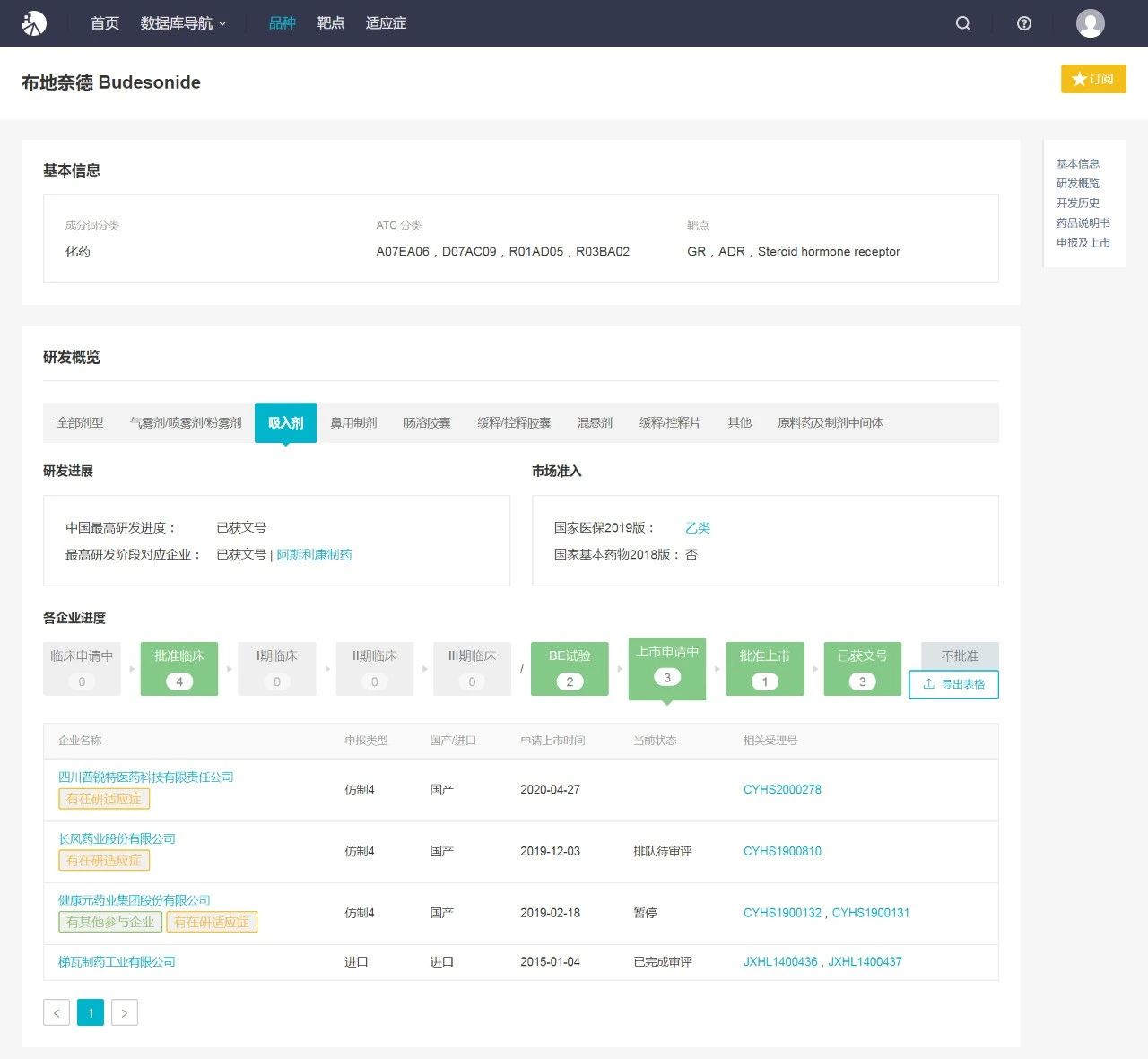
来源 Insight 数据库(https://db.dxy.cn/v5)
据 Insight 数据库显示,四川普锐特药业开展的吸入用布地奈德混悬液人体生物等效性试验在2019年12月完成首例入组(规格为2mL:1mg),目前最新信息显示已完成患者招募。
三家报上市的企业如果审评顺利的话,最早的有望年底获批第二家布地奈德混悬液仿制药,届时原研国内市场有望实现国产加速替代。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030