2018年3月20日,罗氏PD-L1 抗体Tecentriq的一项3期临床试验传出好消息,IMpower131表明Tecentriq联合化疗能够降低初治鳞状NSCLC患者肿瘤恶化和死亡风险,达到PFS临床主要终点,该项研究对Tecentriq冲击鳞状NSCLC一线疗法至关重要,可能将Tecentriq年销售额推升10亿美金。笔者在这里分享IMpower131试验设计和初步数据,并简单比较了opdivo,keytruda和Tecentriq的市场份额。
一.IMpower131:拿下鳞状NSCLC一线疗法
IMpower131是一项多中心、开放标签3期临床试验,共计招IV期鳞状NSCLC患者1021例,以标准化疗方案为对照,评价Tecentriq联合化疗方案的安全性和有效性,毫无疑问,这种设计是冲着鳞状NSCLC一线疗法去的。
试验设计:
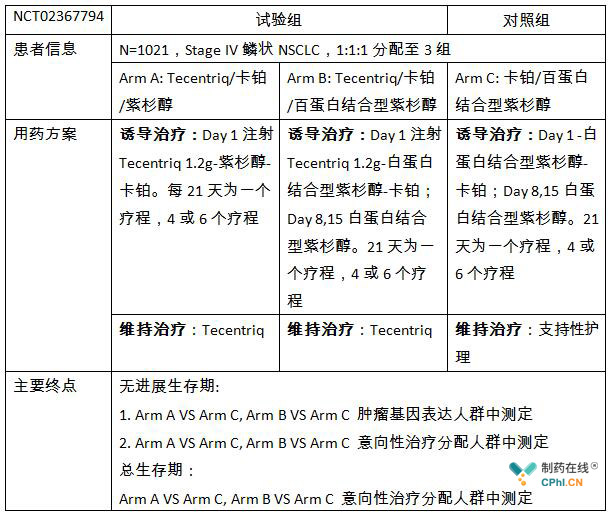
目前IMpower131数据显示,Tecentriq联合化疗能够降低初治鳞状NSCLC患者肿瘤恶化和死亡风险,达到无进展生存期临床主要终点,而总生存期主要终点尚未达到,该数据也至关重要,且待最终结果。
二.Opdivo和keytruda是PD-(L)1市场的两大王牌
PD-(L)1市场总规模已经超过100亿美金,opdivo全球销售额已经突破50亿美金,keytruda同时也在快速增长,相比而言,Tecentriq的2017年销售额为7800万美金,3者获批的临床适应症见附表。
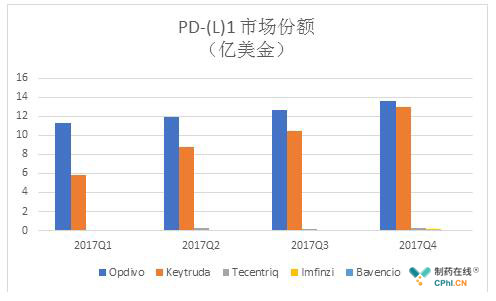
肺癌严重威胁着人类健康,据统计,世界范围内每年约159万人死于该疾病,一般的,肺癌可以分为NSCLC和小细胞肺癌,其中85%肺癌患者为NSCLC;在NSCLC患者中,25%-30%为鳞状NSCLC。IMpower131的重要进展对Tecentriq未来市场预期具有非常重要的作用。
Opdivo/keytruda/Tecentriq已获批适应症:
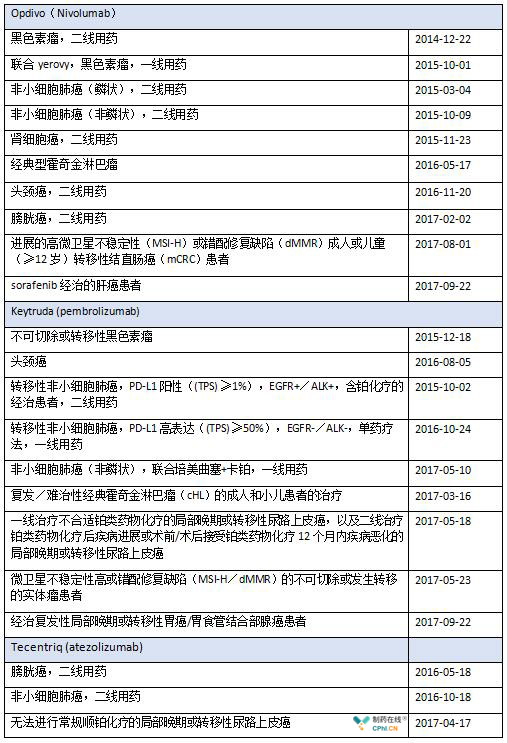
来源:https://www.roche.com/media/store/releases/med-cor-2018-03-20.htm
作者简介:Dopine,注册执业药师,河南省药学会会员,就职于河南省某三级甲等医院PIVAS,精于临床药学服务,专注临床用药安全和不合理用药。对国内外医药审评审批政策,研发动态,新药注册审批等长期关注。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57