https://www.cphi.cn 2018-10-12 15:29 来源:新浪医药新闻
Vertex制药公司与合作伙伴CRISPR Therapeutics近日联合宣布,美国食品和药物管理局(FDA)已经解除了实验性基因编辑疗法CTX001的临床搁置,并已接受了该疗法用于治疗镰状细胞病的实验性新药申请(IND)。这也将成为美国首例CRISPR基因编辑疗法的人体临床试验。
两家公司最初在今年4月提交了IND,以支持一项计划中的I/II期临床试验。但在5月时,美FDA搁置了CTX001的IND,理由是需要解决IND中存在的一些问题。此次FDA解除此前的临床搁置,引发CRISPR公司股价在盘前交易中上涨近12%。不过,在宣布解除临床搁置的简短声明中,两家公司并没有具体说明FDA之前究竟存在哪些顾虑,也没有说明双方是如何解决这些问题的。
Vertex和CRISPR于2017年12月开始合作开发CTX001,这进一步巩固了双方最初于2015年建立的合作伙伴关系。今年8月,双方获得了在欧洲开展CTX001针对β地中海贫血和镰状细胞病的I/II期临床研究的许可,这也是全球首个由制药公司启动的CRISPR基因编辑人体临床研究。目前,治疗β地中海贫血的欧洲I/II期研究正在招募输血依赖型β地中海贫血患者,双方表示,将在2018年底开始进行CTX001治疗镰状细胞病的欧洲I/II期临床研究。
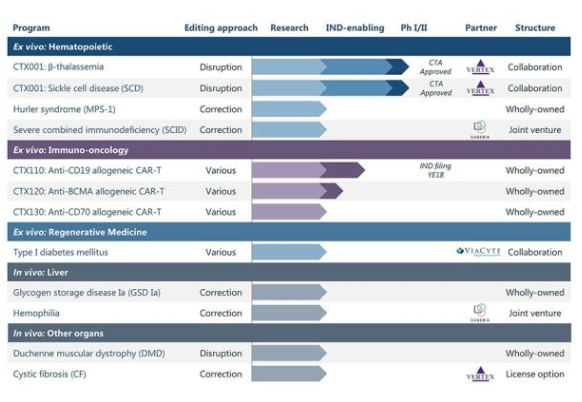
CRISPR公司在研管线(来自CRISPR Therapeutics官网)
此前,Editas Medicine被认为将是开展基因编辑技术人体临床研究的首个制药公司,该公司原计划在2017年启动临床研究调查一种CRISPR基因编辑疗法治疗一种罕见类型的失明。但因为制造问题,临床时间表被推迟至2018年,该公司首席执行官Katrine Bosley在今年二季度更新报告中表示,计划在10月提交IND。
β地中海贫血和镰状细胞病是由β珠蛋白基因突变引起,该基因编码红细胞的载氧成分——血红蛋白的一个亚基。由于该基因突变导致血红蛋白丢失或有缺陷,最终引发严重的医疗问题。不过,在一些罕见病例中,尽管成人血红蛋白存在缺陷,但病情却并不是那么严重,因为这些患者在成年期会继续产生胎儿血红蛋白(HbF),这是在胎儿期产生的一种血红蛋白,也是新生儿的主要血红蛋白,在出生后逐渐减少,到大约6个月时,HbF几乎停止产生,开始产生成人血红蛋白。在成人中,HbF只占总血红蛋白的0.5%。与成人血红蛋白相比,HbF对氧的亲和力更大。目前已知,促进HbF的产生可以改善疾病的症状。
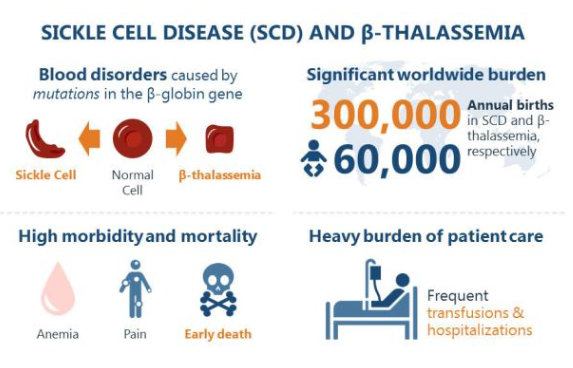
β地中海贫血和镰状细胞病(来自CRISPR Therapeutics官网)
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030