https://www.cphi.cn 2023-12-20 09:51 来源:深交所
近日,合肥立方制药股份有限公司(以下简称“公司”或“立方制药”)收到国家药品监督管理局核准签发的关于甲磺酸多沙唑嗪缓释片《药品补充申请批准通知书》(通知书编号:2023B06360)。公司甲磺酸多沙唑嗪缓释片通过仿制药质量
和疗效一致性评价。现将相关情况公告如下:
一、药品基本情况
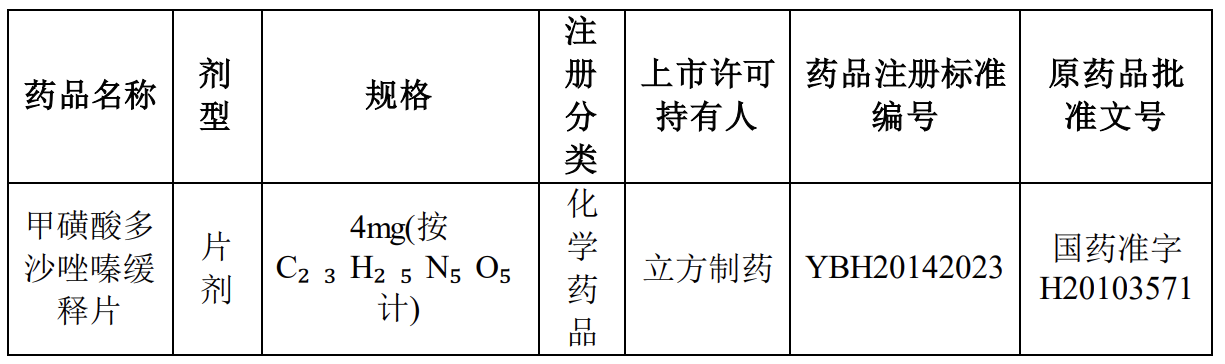
申请内容:一致性评价工作的注册申请,同时变更生产场地、处方工艺、质量标准。
审批结论:根据《中华人民共和国药品管理法》《国务院关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号)和《关于仿制药质量和疗效一致性评价工作有关事项的公告》(2017年第100号)规定,经审查,本品通过仿制药质量和疗效一致性评价,同意变更处方工艺、质量标准及生产场地。
二、药品的其他相关情况
甲磺酸多沙唑嗪缓释片的适应症为:良性前列腺增生对症治疗;高血压。公司甲磺酸多沙唑嗪缓释片于2010年获批上市,批准文号为国药准字H20103571,规格为4mg(按C₂ ₃ H₂ ₅ N₅ O₅ 计)。公司2022年12月向国家药品监督管理局药品审评中心递交甲磺酸多沙唑嗪缓释片的一致性评价补充申请,于2022年12月12日获受理。截至本公告日,除原研外,国内共有2家企业甲磺酸多沙唑嗪缓释片按化学药品4类仿制药注册申请获批,视同通过仿制药质量与疗效一致性评价,公司为首家按一致性评价补充申请注册申报获批的企业。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030