https://www.cphi.cn 2024-01-12 13:57 来源:药智数据 作者:兆景
1月11日,劲方医药宣布,高选择性CDK9抑制剂GFH009(SLS009 )近期再次获得两项美国FDA资格认定,目前该药物治疗复发/难治性急性髓系白血病(AML)和复发/难治性成人外周T细胞淋巴瘤(PTCL)均获得了FDA快速通道资格认定和孤儿药资格认定。据了解,这是GFH009于2023年获得多项FDA资格认定后,又获得治疗急性髓系白血病的快速通道资格认定。

图片来源:劲方医药
2022年,劲方医药与SELLAS生命科学集团(以下简称“SELLAS”)就GFH009开发达成战略授权合作,目前双方正加速推动GFH009的研究进程。
多个资格认定
研发进程加速中
细胞周期蛋白依赖性激酶9(CDK9)是一类丝氨酸/苏氨酸激酶,在细胞周期调节及细胞转录过程中有着关键的作用,CDK9是CDK激酶家族中最 具潜力的靶点之一。相关研究表明,CDK9活性与多种类型癌症患者的总生存率呈现负相关,包括AML、淋巴瘤、黑色素瘤、子宫内膜瘤等各类癌症。
GFH009正由劲方医药与SELLAS合作开发,是一款强效、高选择性的CDK9抑制剂。临床前试验数据显示,GFH009能够降低下游原癌基因表达、加速肿瘤细胞衰老凋亡,且对CDK9蛋白的选择性抑制率远超其他CDK亚型。此外,体外、体内药效实验还表明CFH009对血液肿瘤细胞系增殖有抑制效果。
劲方医药表示,GFH009针对两项适应症的临床试验分别在中国与美国开展、并均已进入II期研究阶段。在I期及II期试验中,有多例患者观察到完全或部分缓解、以及超越同类靶向疗法的安全性和疗效。

图片来源:劲方医药
聚焦肿瘤、免疫
管线日渐壮大中
劲方医药聚焦于肿瘤、免疫类疾病领域,已建立涵盖TGF-β R1、KRAS G12C、RIPK1、CDK9等靶点的产品管线,涉及NSCLC、自免疾病、白血病、淋巴瘤等各类疾病。其中,GFH925、GFH018、GFH312等多款产品在2023年取得了重大进展。
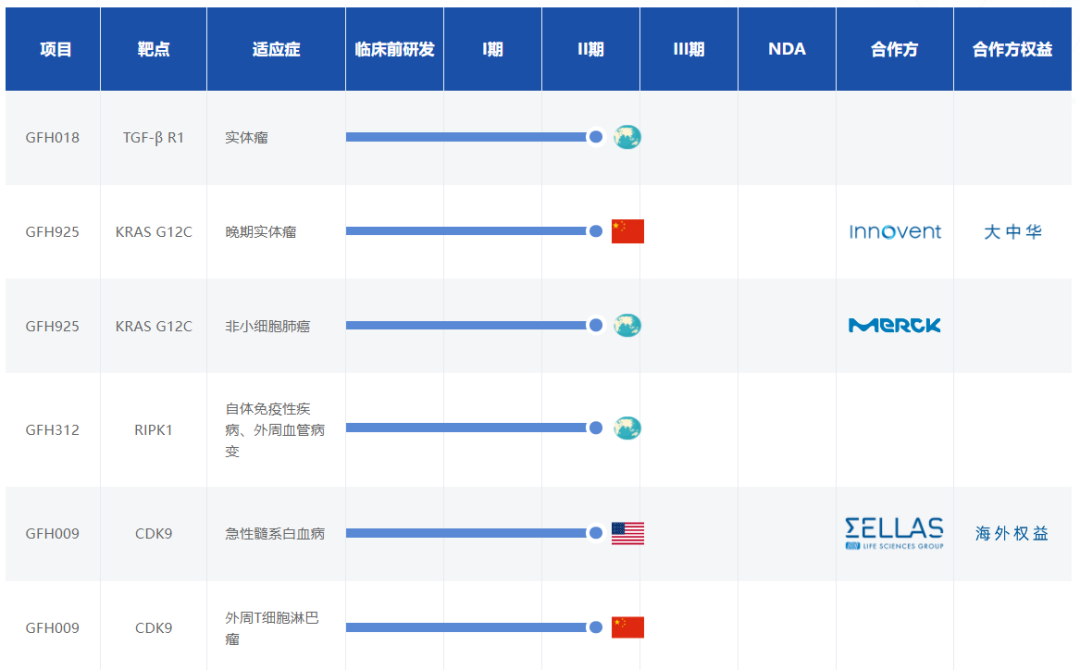
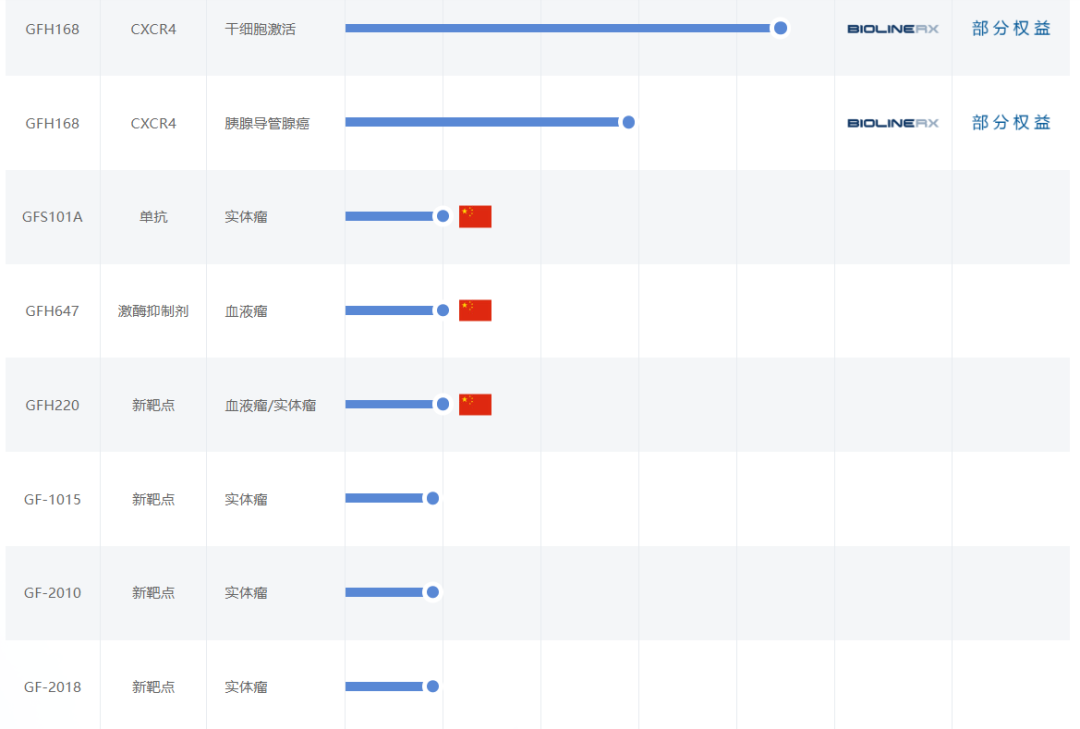
图片来源:劲方医药
GFH925
GFH925是一款国内自研的新型、具口服活性的强效KRAS G12C抑制剂,同时是国内首 个递交上市申请并获受理、且纳入CDE优先审评品种名单的KRAS G12C抑制剂,此外,GFH925已获得CDE两项突破性疗法认定。目前,劲方医药正与信达生物、默克合作开发GFH925。

图片来源:CDE官网
GFH018
GFH018是劲方医药自主开发的一款TGF-β R1抑制剂,于2019年开启临床试验。在2023 ASCO大会上,劲方医药首次公布了GFH018联合特瑞普利单抗的Ib/II期临床试验数据,显示联合疗法在鼻咽癌受试者中具有良好的耐受性、抗肿瘤活性。此外,该研究还是国内药企主导的首 个小分子TGF-β R1抑制剂联合PD-1抑制剂的全球多中心研究。
GFH312
GFH312是一款RIPK1抑制剂,同时是劲方医药首 个进入临床阶段的自免领域产品以及首 个获批美国II期临床的项目。在2023 ASCPT年会上,劲方医药首次公布了GFH312在I期试验健康受试者中的研究结果,显示GFH312在研究中的安全性/耐受性良好,并且药代动力学/药效学特性支持后续临床开发。
此外,2023年,劲方医药将三款自主开发、以RAS通路靶向药领衔的创新疗法授权予Verastem Oncology,总交易金额或超6亿美元。
结语
劲方医药正加速多款药物临床研究进度,有望在未来不久迎来密集收获期。与此同时,劲方医药研发管线日渐丰盈,将为其开辟更多领域的道路。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030