https://www.cphi.cn 2023-11-07 11:57 来源:CPHI制药在线 作者:203的spuer
PD-1/PD-L1皮下剂型的竞争硝烟早已经在全球范围内弥漫,就目前来看罗氏和BMS已经成为了领跑者。
近期,BMS宣布O药(Opdivo)皮下注射制剂对比其静脉注射制剂用于既往接受过全身治疗的晚期或转移性肾透明细胞癌(ccRCC)患者的III期CheckMate-67T研究达到了共同主要终点和关键次要终点。研究结果显示,与静脉制剂相比,纳武利尤单抗皮下制剂显示出非劣的药代动力学特征与客观缓解率,在被K药(Keytruda)压制了多年之后,BMS在O药皮下制剂推进的时间进度上终于反超了MSD的K药一个身位。
今年九月,罗氏(Roche)宣布其靶向PD-L1抗体Tecentriq(T药,阿替利珠单抗)皮下制剂获得英国药品和医疗产品监管署(MHRA)批准上市。Tecentriq皮下制剂获批在英国用于Tecentriq静脉制剂之前已获批的所有适应症(包括某些类型的肺癌、膀胱癌、乳腺癌和肝癌)。与耗时30-60分钟的静脉输注相较,Tecentriq皮下注射大约仅需7分钟。根据罗氏的新闻稿,这次批准是Tecentriq皮下制剂首次在全球获得监管单位批准,目前药物于美国FDA以及欧洲药品管理局(EMA)的审评正在进行中。
这是罗氏第四款由皮下注射抗肿瘤产品,此前三款分别是Phesgo(帕妥珠单抗(Pertuzumab)+曲妥珠单抗)、Herceptin (赫赛汀单抗)以及MabThera(利妥昔单抗),在渐渐摆脱对三驾马车的依赖之后,罗氏也想凭借着剂型创新,寻求在抗肿瘤药物领域的差异化, Tecentriq在2022年销售额为37.17亿瑞士法郎(38.96亿美元),和O药的93.62亿美元也都还相距甚远,Tecentriq皮下制剂能否为罗氏打开新的增长点,也值得期待。
图1
在两年之前,国内诞生了全球首 款获批的皮下注射PD-1/PD-L1药物--我国药监局附条件批准恩沃利单抗注射液上市,其也成为我国首 个获批的国产PD-L1抑制剂,同时也是全球首 个皮下注射PD-L1抑制剂,如今两年时间已经过去,在一片红海的国内市场,恩沃利单抗的市场表现其实也一直备受关注。
01 全球首 款皮下注射PD-1/PD-L1药物表现如何
皮下注射产品最大的卖点,就是大大提高PD-1/PD-L1产品的依从性,在安全性以及有效性数据和静脉注射制剂差异不大的情况下,皮下注射将大幅降低由静脉注射导致的漫长的给药时间,节约医疗资源。
皮下制剂有可能将临床优势以及差异化转化为市场优势吗,这个问题在全球范围内还需要更多时间来加以印证。
2021年11月,国家药监局通过优先审评审批程序,附条件批准恩沃利单抗注射液上市,适应症为适用于不可切除或转移性微卫星高度不稳定(MSI-H)或错配修复基因缺陷型(dMMR)的成人晚期实体瘤患者,成为国内首 个获批该适应症的PD-1/PD-L1药物。在K药在今年九月获批该适应症之前,恩沃利单抗也为该适应症唯一的PD-1/PD-L1药物,独占市场,那么在这两年时间里,恩沃利单抗交出了怎样的市场答卷呢?
恩沃利单抗开发历史较为复杂,其所属权益涉及多方,康宁杰瑞作为原研方负责生产和质量,思路迪把控肿瘤领域的临床开发,歌礼开展病毒 性疾病领域的开发和商业化,先声承接中国大陆的独家商业推广。根据公开信息,在康宁杰瑞、思路迪和先声药业的合作下,恩沃利单抗2022年覆盖约2万患者,在首 个商业化完整年取得5.67亿元营收。
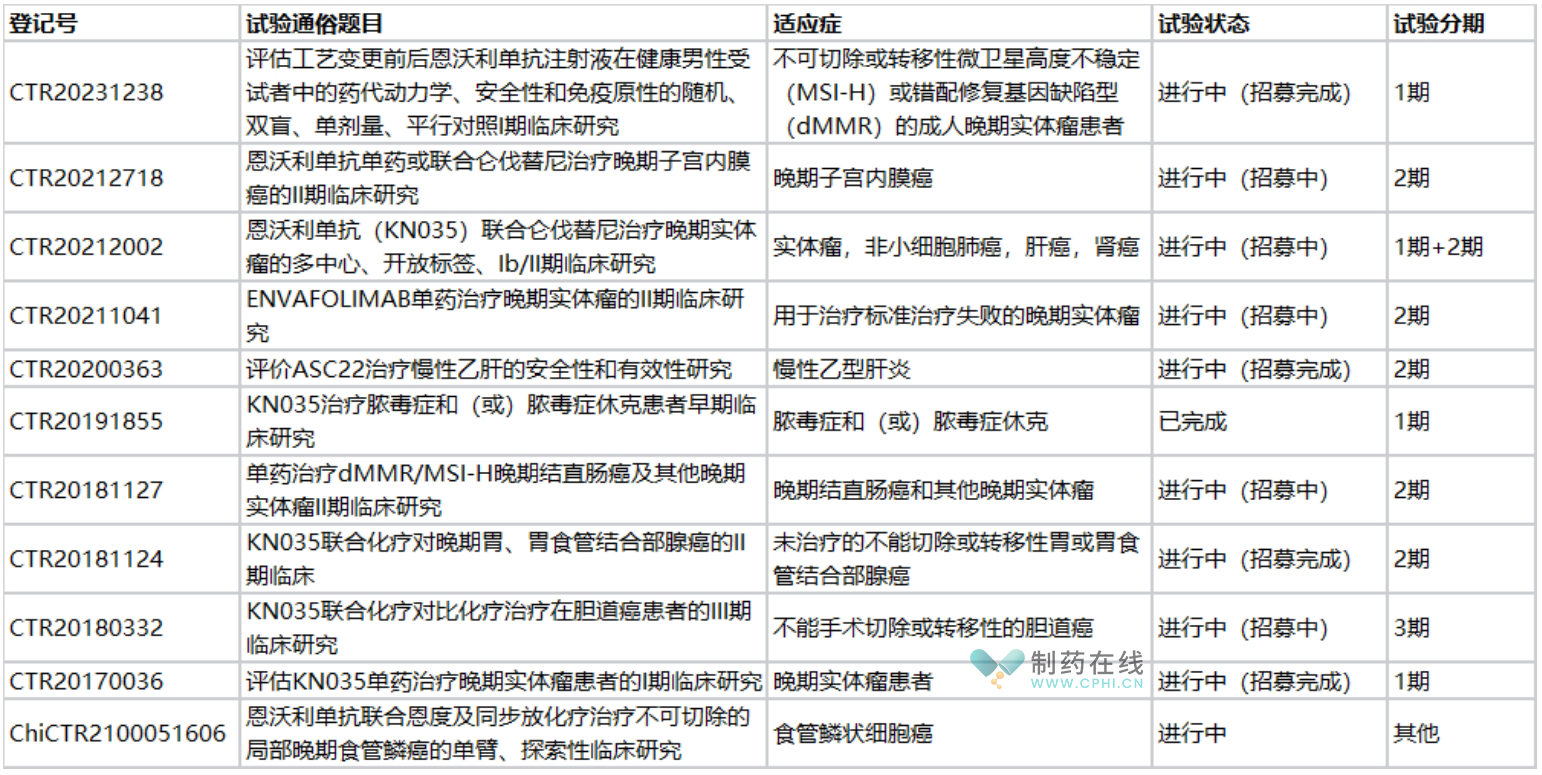
表1:恩沃利单抗正在国内开展的临床试验(梳理自药智数据)
仅仅靠单适应症,即使有皮下给药的依从性优势,也很难转化为市场优势,在目前已经杀成红海的国内市场下,恩沃利单抗也开展了多项临床,积极扩展其适应症,其中联合化疗对比化疗治疗在胆道癌目前已经进入III期临床,在国内这一适应症领域目前处于领先状态,未来恩沃利单抗有望靠着新适应症拓展冲击10亿元关卡。
02 BMS、默沙东、罗氏、辉瑞.....MNC已展开全面竞速,国内竞争愈演愈烈
罗氏的PD-L1抗体Tecentriq皮下注射制剂已经率先在英国获批上市,其在欧洲其他国家以及美国的商业化预计也将于明年完成,届时实现全球商业化的Tecentriq皮下制剂也将带给我们不少期待。BMS也紧随其后,O药(Opdivo)皮下注射制剂三期临床也顺利到达终点,同样也将为O药注入新的差异化增长曲线。
作为全球PD-1领域的霸主,默沙东也得为Keytruda 2028年关键专利以及独占期到期提前布局,这也进一步增加了默沙东开发皮下制剂的动力,其对于Keytruda皮下制剂的开发也是花了大量资源。
目前K药的皮下注射制剂也正在开展III期MK-3475-A86试验,以评估皮下给药与化疗联用,对比静脉给药与化疗联用,治疗鳞状和非鳞状一线非小细胞肺癌(NSCLC),根据默沙东在8月披露的信息,该研究目前已经达到了研究终点,但其目前并没有公布下一步举措。同时,默沙东也在做多手准备,另一个重点则放在了K药与透明质酸酶的皮下复方制剂,和K药单药每三周给药一次不同,这一复方制剂可以实现每六周给药一次,其临床Ⅰ期试验预计将于 2026 年完成。
此外,在进度上和上述几家MNC保持一致的还有辉瑞,尽管在这一领域并非其所长,但其实辉瑞开发的PD-L1皮下制剂Sasanlimab目前也在III期临床阶段,适应症则瞄准了更为差异化的非肌层浸润性膀胱癌,预计试验将于2024年年中结束,不过这一项目目前公开的数据较少,在目前辉瑞的管线中并不具备优先级别,鉴于辉瑞本年度直接收购了Seagen将其ADC药物收入麾下,未来该药在抗肿瘤领域更加深入的探索倒也有可能发生。
国内企业的布局速度也并不算慢,恒瑞、君实以及百济目前都有PD-1皮下制剂的产品进入临床,恒瑞医药的 SHR-1901 在2021年年底就首次启动临床试验,是第2款进入临床阶段的国产皮下注射剂型PD-1单抗产品,君实生物开发的 JS001sc 注射液则是在已上市产品特瑞普利单抗注射液的基础上开发的,针对晚期鼻咽癌,而百济神州替雷利珠单抗皮下注射剂型也在上个月国内获批临床,用于治疗恶性肿瘤,预计未来国内的PD-1皮下剂型竞争也将会愈演愈烈。
03 差异化之路并不好走
从以上其实也不难看出,PD-1皮下制剂的竞争也在全球蔓延,未来该剂型的竞争想必也是一片红海,这条差异化之路,也随着入局者越来越多显得荆棘遍布。
仔细思考其中的逻辑,其实从历史进程来说,PD-1从静脉注射卷到皮下注射也是必然的,随着K药和O药专利到期日越来越近,MSD和BMS必然会使出浑身解数守住全球市场优势,而以罗氏辉瑞为代表的PD-1全球第二梯队必然也会进行差异化布局,以临床优势另辟蹊径,再加上以重组人透明质酸酶(rHuPH20)为代表的透明质酸技术在大分子药物上的应用,实现了实现从静脉给药到皮下给药的转换和剂量优化,减轻疾病的治疗负担的目标,也成功的将罗氏、强生的多款重磅产品完成上市,验证了递送技术的可行性,各个因素助推,也让目前PD-1皮下剂型的竞争也成了红海一片。
从市场逻辑来说其实倒也不难理解,通过同时改善给药方式、开发联合疗法等策略,降低因市场独占期以及专利到期仿制药带来的冲击,充分利用已有市场优势延长产品生命周期,这一点已经在罗氏身上而得以印证了,罗氏采取皮下制剂替代的策略,开发了曲妥珠单抗皮下注射剂 Herceptin Hylecta和曲妥珠+帕妥珠复方皮下制剂 Phesgo,其中 Phesgo 自上市以来也持续保持着高增长,本年度H1销售额达到了7亿美元,同比翻倍,目前来看默沙东、BMS们也都延续了这一市场逻辑。
上周君实生物PD-1特瑞普利单抗获得FDA批准,无疑给国产创新药出海注入了一针强心剂这是国产 PD-1 产品在美国斩获的首 个上市批准,具有里程碑意义,其适应症也是差异化的鼻咽癌,而目前PD-1药物的竞争已经全面席卷到了皮下制剂,未来谁将成为PD-1皮下制剂第一个吃蛋糕的人,我们也正在等待着。
参考资料:
1. https://www.roche.com/investors/updates/inv-update-2023-08-29b;
2. Phase 3 CheckMate -67T Trial of Subcutaneous Nivolumab (nivolumab and hyaluronidase) Meets Co-Primary Endpoints in Advanced or Metastatic Clear Cell Renal Cell Carcinoma,from BMS;
3. 药智数据、CDE以及临床试验登记平台官网;
4. Study of Pembrolizumab (MK-3475) Subcutaneous (SC) Versus Pembrolizumab Intravenous (IV) Administered With Platinum Doublet Chemotherapy in Participants With Metastatic Squamous or Nonsquamous Non-Small Cell Lung Cancer (NSCLC) (MK-3475-A86)。
版权所有,未经允许,不得转载。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030