https://www.cphi.cn 2024-02-26 14:27 来源:药智头条 作者:游游
日前,默沙东公布了 2023年财报,全年营收 601.15 亿美元,同比增长 1 %。其中明星产品PD-1单抗Keytruda(K药,帕博利珠单抗)强劲增长19%,达到250.11 亿美元,占总营收的41.6%,终于登顶“药王”宝座。
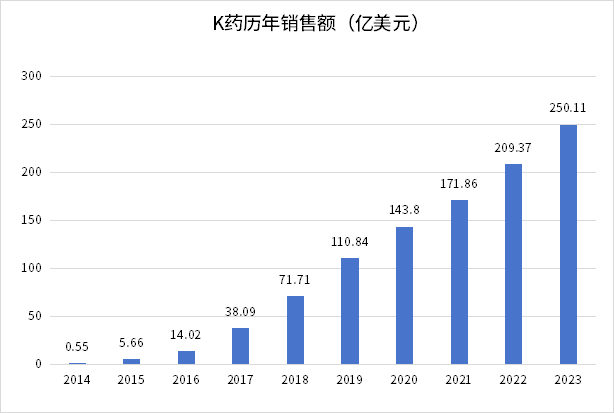
数据来源:默沙东历年财报
不过K药核心专利保护将在2028年到期,且面临强劲的竞争对手——来自诺和诺德的GLP-1类似物司美格鲁肽2023年销售额已达212亿美元,较2022年的109亿美元,近乎翻倍。
在内外压力下,默沙东一方面不断拓展K药适应范围,另一方面多次出手并购、license in潜力肿瘤产品,以稳固在肿瘤领域的地位。
PD-1之后
默沙东继续引领PD-1+ADC
2009年默沙东以400亿美元收购先灵葆雅获得K药,目前K药在美国FDA获批的适应症已经超过30项,在中国已获批13项,覆盖约20个癌种。2023年K药以250亿美元的销售额如愿登上药王宝座。
不过,K药的专利将于2028年到期,还有不到5年时间,默沙东很显然已开始焦虑,不断为步入PD-1后时代做着准备。
默沙东不断为K药开发新适应症、拓展肿瘤早期阶段治疗、扩大不同适用人群,以及开发联用疗法。在联用方面,目前K药联合化疗已开始进入收获期。而K药联合ADC开始也开始展现出潜力。
2023年12月,默沙东宣布FDA提前批准了K药联合Nection-4 ADC(Padcev)一线治疗不适于接受含顺铂化疗的局部晚期或转移性尿路上皮癌患者。这是全球首 个获批的“PD-1+ADC”组合疗法。

图片来源:默沙东官网截图
长期以来,晚期尿路上皮癌(mUC)的治疗以含铂化疗方案为主,然而患者在含铂化疗失败后,后续的治疗选择有限。相较之下,ADC药物如Padcev、维迪西妥单抗的临床数据优于化疗及免疫疗法,而PD-1+ADC联合疗法在一线治疗表现中更加亮眼。
K药+Padcev的获批是基于 KEYNOTE-869(EV-103)的研究数据。结果显示,OS与PFS近乎翻倍增长,且患者死亡风险降低53%。
看重“PD-1+ADC”的不止默沙东一家,事实上,已有多个癌种的临床试验数据显示PD-1+ADC联合疗法的疗效优于单药,产生“1+1>2”的疗效潜力。
2023 ASCO大会上,荣昌生物公布了维迪西妥单抗联合特瑞普利单抗治疗局部晚期或转移性尿路上皮癌的最新研究成果:截至2022年11月18日,显示确证客观缓解率(cORR)为73.2%,完全缓解(CR)为9.8%,初治患者ORR为76.0%,中位疗效持续时间(DOR)为8.2个月。在HER2 IHC 3+/2+、IHC 1+亚组中,ORR分别为83.3%、64.3%。结果显示DCR为90.2%,PFS为9.2个月,2年总生存率(OS)为63.2%,展现出良好的疗效和安全性。
2023 ASCO大会上,第一三共公布了DS-1062+K药±铂类化疗的TROPION-Lung02研究结果:在一线无驱动基因突变的NSCLC人群中(nsq占比约70%),二联疗法的ORR=50%,DCR=91%;三联疗法的ORR=57%,DCR=91%,展现出良好的初步疗效。
2023 WCLC大会上,吉利德公布了Trodelvy联用K药一线治疗无驱动基因突变的晚期或转移性NSCLC的EVOKE-02临床试验结果:其中针对TPS≥50%(队列A)患者的ORR为69%,DCR为86%;针对TPS<50%(队列 B)的ORR为44%,DCR为78%。所有队列的ORR为56%,DCR为82%。DoR未达到,6个月DoR率为88%。
目前各大药企都在积极开展PD-1+ADC联合疗法的研究,PD-1+ADC有望成为未来几年肿瘤免疫的主线。
牵手科伦、第一三共
加速布局ADC
默沙东在拿下首 个PD-1+ADC适应症后,又不断加码ADC布局,继续拓宽肿瘤领域护城河。
2022年,默沙东与科伦博泰签订三项许可及合作协议,以118亿美元达成多个 ADC 合作,包括已推进至临床阶段的3项 ADC 资产,分别为MK-2870(SKB264,Trop2 ADC)、MK-1200(Claudin18.2 ADC)、MK-3120(Nectin-4 ADC)及多个临床前 ADC 资产。
2023年10月,默沙东以40亿美元的前期付款,220亿美元的合作总金额,与第一三共达成合作,开发三款ADC药物候选药物:MK-1022(HER3 ADC)、MK-2400(B7H3 ADC)和MK-5909(CDH6 ADC)。
与科伦博泰和第一三共的合作让默沙东快速拥有了6个临床阶段的ADC管线。
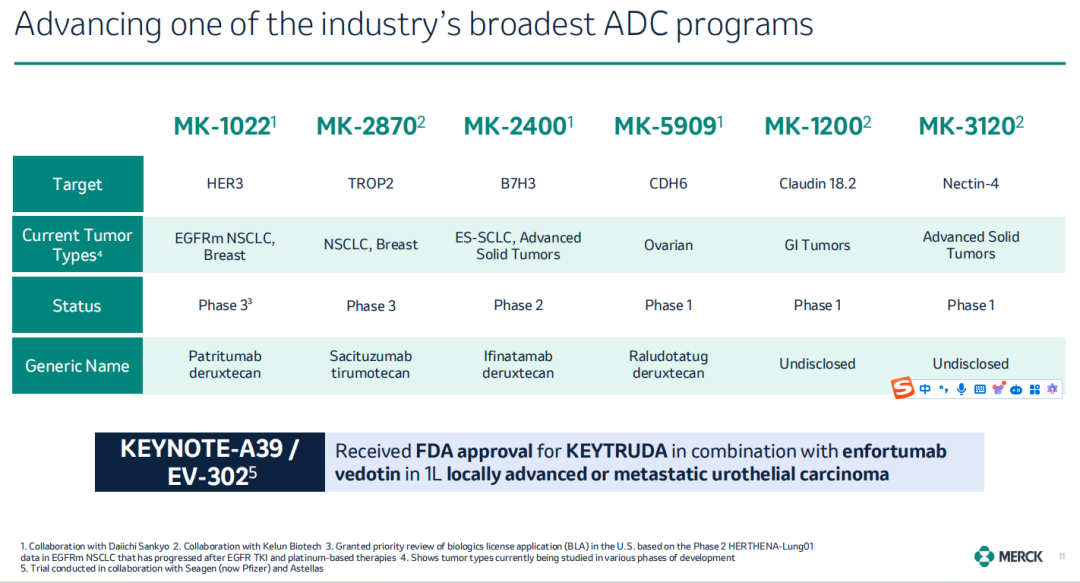
图片来源:默沙东JPM2024 PPT
其中MK-1022(U3-1402,HER3 ADC)和MK-2870(SKB264,Trop2 ADC)已进入上市申报阶段。
MK-1022(HER3-DXd,HER3 ADC)
Patritumab deruxtecan(HER3-DXd)是一款采用第一三共技术设计的潜在first-in-class靶向HER3的ADC,由全人源化抗HER3 IgG1单克隆抗体通过可裂解四肽连接子与拓扑异构酶I抑制剂有效载荷(一种依喜替康衍生物,DXd)连接组成。
2023年12月,HER3-DXd的生物制品许可申请(BLA)获美国FDA受理并授予优先审评资格,用于治疗既往接受过两种或两种以上全身治疗的局部晚期或转移性EGFR突变非小细胞肺癌(NSCLC)成人患者。《处方药使用者付费法案》(PDUFA)日期为2024年6月26日。
此次BLA基于HERTHENA-Lung01研究结果:HER3-DXd对225例既往接受EGFR TKI和含铂化疗后出现病情进展的EGFR突变局部晚期或转移性NSCLC患者产生持久且具有临床意义的疗效,客观缓解率(ORR)为29.8%(95% CI:23.9~36.2),其中包含1例完全缓解(CR),66例部分缓解(PR)。中位缓解持续时间(DOR)为6.4个月(95% CI:4.9~7.8)。
安全性方面,因治疗中出现的不良事件(TEAE)导致终止治疗的患者比例较低(7.1%)。3级或3级以上的TEAE发生率为64.9%。
MK-2870(SKB264,Trop2 ADC)
SKB264是由科伦博泰的ADC研发平台—OptiDC研发的靶向TROP2 ADC,由具有高亲和力和靶向性的人源化抗TROP2单抗,通过稳定性经过优化的CL2A连接子与自研毒素小分子T030(拓扑异构酶Ⅰ抑制剂)结合而成,药物抗体比(DAR) 7.4。
SKB264已获得3项突破性疗法认定(BTD),分别用于治疗局部晚期或转移性三阴性乳腺癌(TNBC)、EGFR-TKI治疗失败的局部晚期或转移性EGFR突变非小细胞肺癌(NSCLC)、既往接受过至少二线系统化疗的局部晚期或转移性激素受体阳性(HR+)和人表皮生长因子受体2阴性(HER2-)乳腺癌。
2023年12月,SKB264(MK-2870,商品名:佳泰莱)用于既往至少接受过2种系统治疗(其中至少1种治疗针对晚期或转移性阶段)的不可切除的局部晚期或转移性三阴性乳腺癌(TNBC) 成人患者的新药上市申请获中国国家药品监督管理局受理。此次新药上市申请已被CDE纳入优先审评审批程序,SKB264有望成为中国首 个获批上市的国产创新TROP2-ADC。
在全球,默沙东已登记SKB264治疗EGFR等突变NSCLC的国际多中心三期临床。该三期临床计划入组556例非小细胞肺癌患者,预计2027年5月初步完成。
布局DACs
寻找偶联药物新大陆
既然看中了偶联技术,默沙东的野心自然不止ADC,还重金布局了DACs。
2023年12月,默沙东与C4 Therapeutics(C4T)达成合作,共同开发抗体偶联蛋白降解药物(DACs)。

图片来源:C4T公司官网截图
DAC结合了两种强大的技术:抗体药物偶联物(ADCs)和蛋白质降解技术。DAC的工作原理简单来说就是,抗体部分负责寻找并精确靶向病变细胞,就像一个有高度专业知识的导游,能够在繁忙的城市中精确找到目的地。一旦抗体找到目标细胞,它就会将绑定在它上的降解剂“送货上门”。这个降解剂就像是一个拆迁专家,它可以拆除导致细胞变成癌细胞的部分结构。通过这种方式,抗体和降解剂的结合不仅提高了药物的精确度,还增强了其摧毁癌细胞的能力。
C4T 和默沙东将合作开发一款针对未公开肿瘤学靶点的DAC,C4T 将获得 1000 万美元的预付款,总计约 6 亿美元的里程碑付款,以及未来销售的分级特许权使用费。默沙东还获得扩大合作范围的选择权,包括 3个独家合作靶点,如果行使所有选择权,C4T 将有资格获得高达约 25 亿美元的潜在付款。C4T 将负责使用其专有的 TORPEDO 平台在发现阶段开发降解剂有效载荷,默沙东将负责抗体偶联,以在发现阶段创建 DAC,进行临床前和临床开发以及商业化。
目前,全球范围内对于DAC的研发,仍然处于早期阶段,但已经使用各种PROTAC有效载荷成功制备了许多DAC分子实体,显示出良好的体外和体内生物学活性。默沙东在此时布局,有望抢得先机。
小 结
目前,K药是默沙东最重要的收入来源,年销售额250亿美元,占总营收比例高达41.6%。为了应对K药专利悬崖的逼近,默沙东不得不早做准备,不断加码ADC,拓展PD-1+ADC联合疗法。凭借K药的广泛适用性,默沙东在未来几年内将继续在肿瘤领域保持领先地位。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030