https://www.cphi.cn 2024-01-17 14:58 来源:博药 作者:费翔
去年两项大型临床试验显示,GLP-1受体激动剂不仅能够有效降低体重,还能够改善肥胖相关的心血管和肾脏疾病,被《科学》杂志评为年度突破。
GLP-1类似物是多肽药物的一个重要类别,GLP-1药物的成功推动了多肽药物市场持续扩容,多肽制药工艺研究成为当前多肽研究的前沿与热点。
多肽药物简史
合成技术的进步推动多肽药物开发
多肽药物是一种介于小分子化学药物和大分子蛋白质药物之间的“独特药物”,由氨基酸组成。它们因具有较少的副作用、高度的特异性和优异的疗效而被广泛关注。此外,多肽药物的结构明确且质量可控,使其在药物开发过程中更为可靠。
小分子、多肽药物、生物制剂优缺点比较
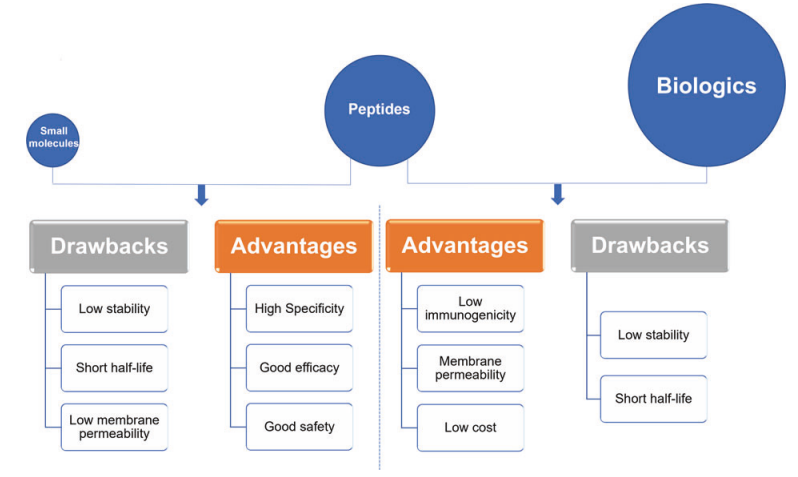
图片来源:参考资料1
1922年,第一种多肽药物胰岛素被引入市场,最初是从牛和猪的胰腺中提取的,用于治疗糖尿病。
1954年,化学家文森特·迪维尼奥首次完成了催产素和血管加压素的全合成,并因此获得1955年诺贝尔化学奖。
1963年,固相多肽合成(SPPS)技术诞生,通过在固相上组装氨基酸,实现了多肽合成的自动化,极大地促进了多肽药物的开发。
20世纪80年代多肽重组技术的出现,使大规模生产绿色多肽成为可能。
得益于在制备技术、剂型与给药途径、缓释技术等方面的重大突破,多肽药物在医药领域的潜力正在逐渐得到实现。目前全球已有超过100种多肽药物上市,200种多肽药物正在临床试验阶段,广泛用于免疫学、肿瘤学、心血管疾病等多个治疗领域。
多肽药物GLP-1类药物(用于治疗肥胖症和糖尿病)和生长 激素是多肽药物市场中的典型代表,展示了这一领域的巨大潜力和发展前景。
GLP-1爆火
多肽需求增长,工艺研究成热点
目前,多肽重磅药品主要集中于糖尿病领域。2022年司美格鲁肽、度拉糖肽、门冬胰岛素、赖脯胰岛素、甘精胰岛素销售额超过20亿美元。
除减肥、糖尿病之外,其他疾病领域也有不少多肽畅销药,涉及多家大型制药企业和生物技术公司。
肿瘤领域,Ipsen(益普生)的兰瑞肽、诺华的奥曲肽2022年销售额都超过了10亿美元。此外,诺华的放射 性多肽靶向肿瘤治疗药物Pluvicto自2022年3月获得FDA批准以来快速放量,2023年销售额有望突破10亿美元,跻身重磅炸 弹行列。
抗感染领域,辉瑞的Paxlovid曾在新冠病毒防治中发挥了重要作用,2022年销售额更是达到了189美元,成为当年最畅销的小分子药品。
罕见病也是多肽药物的主战场。梯瓦(Teva)研发并于1996年上市的格拉替雷曾是多肽药物中最大的品种,2014年其全球销售额达42.37亿美元,用于治疗多发性硬化症(MS)。2023年6月28日,醋酸格拉替雷注射液(商品名:固派松)获得在中国正式批准,适用于治疗复发型多发性硬化(MS)成人患者。
当然,近两年最受关注的莫过于GLP-1类多肽药物。GLP-1激动剂主要通过刺激胰岛释放葡萄糖依赖性胰岛素发挥作用。其次,这类药物还能减缓胃排空和抑制食欲。美国疾病控制与预防中心(CDC)的数据显示,约有3500万美国人患有2型糖尿病,全球糖尿病患者约4.6亿,占全球总人口的6.3%。这一数据体现了抗糖尿病药物市场的巨大规模。
最初,天然肠促胰岛素并不适合作为药物开发的候选物,但随着对降糖尿药物需求的增加,研究人员最终将GLP-1受体激动剂开发成药物。
司美格鲁肽作为目前GLP-1激动剂的代表产品,通过在第2位上将甘氨酸替换为2-氨基异丁酸(Aib)以及十八烷二酸与Lys-26侧链的连接,实现了对自然肽的有效改造。这种改造增强了其对蛋白水解酶DPP-4的抵抗能力,并通过脂肪酸部分与血清白蛋白高度结合,将人体内半衰期延长至约7天。
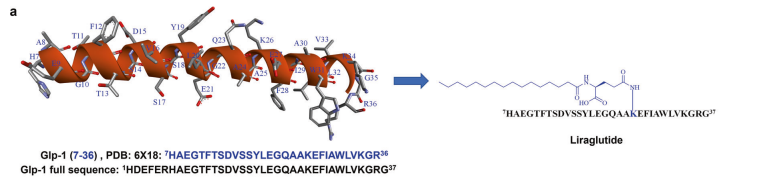
天然GLP-1及其多肽类药物的序列和结构。利拉鲁肽是一种源自GLP-1的肽药物,在其天然序列的第26位(K)进行了修饰。
图片来源:参考论文1
目前司美格鲁肽已获批糖尿病和肥胖两大适应症,诺和诺德还在推进司美格鲁肽在心血管疾病、NASH、CKD、PAD、阿尔茨海默病、心衰领域的临床研究。
由于需求激增,诺和诺德的司美格鲁肽、利拉鲁肽都出现短缺。应对产能供应不足的问题,诺和诺德拟在其位于丹麦希勒勒德的工厂增加原料药(API)的生产能力,以支持诺和诺德在严重慢性病领域的未来产品组合。
另一方面,行业需求的增加带来多肽药物CDMO的持续火热。全球领先的CDMO企业正在大力发展多肽合成业务,进行多方位产能建设,以迅速填补多肽药物产能需求。
这也引发了全球对多肽药物产能的关注,多肽药物工艺研究因此成为当前多肽研究的前沿与热点。
合成与改良
多肽化学合成法成主流
发现具有潜在治疗作用的活性分子是肽类药物开发的第一步,其次是通过化学或生物合成以及序列修改来提高其药理学特性。最后,多肽药物的量产则需要通过工业化生产才能实现。
传统多肽药物的研发主要采取生物发酵法,存在着生产成本高、纯度低、稳定性差等问题。随着多肽合成技术的不断进步,现代多肽药物的研发主要依赖于人工合成。
实验室合成多肽药物相对简单,但在进行多肽工业化生产时需要考虑多方面的问题,包括技术应用、生产工艺、过程控制、产量规模、设备需求、生产成本、质量管理、环保要求等。其主要技术挑战在于提纯难度较大且过程控制要求高,同时还需要考虑产量规模、生产布局与设备需求,控制生产成本。同时多肽药物生产需要遵循严格的质量管理规范,符合法律法规的要求,最后要重视环保要求,提高资源利用效率,减少废弃物产生。
综上考虑,在已有的多肽合成方法中,目前已上市的多肽药物多数是通过化学合成法制备,并且固相合成工艺占主导。据肽研社统计,截至2021年11月,68.8%的多肽分子通过化学合成方法制备,22.8%通过生物合成法获得。固相合成法具有粗产品收率和纯度高,研发周期短等优点,而且固相合成可以切成多个片段,分包给全球不同的生产服务商,再组装成API,从而有效地规避风险。
例如采用固相合成法合成缩宫素,高效、安全、环保、质量好、自动化程度高,相比液相合成法在规模级工业化生产具有一定优势。此外,化学合成法在类似物合成方面有着与生物合成法无法比拟的独特优势。通过化学合成法合成单链胰岛素前体,可快速筛选胰岛素类似物,增加化学多样性,改善产物物理、化学特性,从而获得新的治疗特性,实现胰岛素类似物的工业制造。
固相肽合成(SPPS)技术由梅里菲尔德(Merrifield)于1963年开发。SPPS技术在方法论和合成材料方面得到了显著改进,对现代肽生产起着至关重要的作用。
SPPS通过在一个简单的反应器中结合氨基酸偶联和脱保护步骤,进一步促进了自动肽合成器的发明。与重组技术相比,SPPS得到的原始肽更为单一,不含其他生物化合物如酶、DNA和RNA片段、非相关蛋白和肽。此外,SPPS最终产品中的杂质易于鉴定,因为它们主要来自合成过程中的不完全反应或副反应,使得后续纯化相对简单。
SPPS包括一个循环,即将氨基酸的羧基与固态聚合树脂偶联,并从保护基团中释放氨基(见图4)。使用各种树脂,如4-甲基苯乙烯基胺(HMBA)树脂、王氏树脂、2-氯三苯甲烷氯化物(CTC)树脂和梅里菲尔德树脂,来引入肽C末端的酰胺或游离羧基。现代肽工业通过将树脂与不同的连接器偶联,开发了各种功能性树脂,使得在固相中合成长肽和肽环化成为可能。
固态多肽合成(SPPS)原理示意图
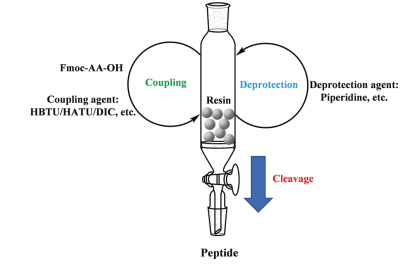
图片来源:参考资料1
在合成过程中,氨基酸的氨基和侧链通常通过不同的化学基团保护,这会导致肽聚集并降低原始肽的纯度。两种主要的SPPS策略:Fmoc-SPPS和Boc-SPPS,分别用于去除主要的氨基保护基团,即荧光甲氧基羰基(Fmoc)和叔丁氧羰基(Boc)。
Boc-SPPS使用三氟乙酸溶液去除氨基保护基团,并使用氢氟 酸溶液切割最终的肽,但这些过程伴随着刺激性气味和毒性。Fmoc在较温和的条件下可被去除,因此Fmoc-SPPS策略通常更受青睐。然而,对于长肽合成而言,Boc-SPPS有其优势,因为三氟乙酸脱保护有效地破坏了肽合成过程中的聚集。
Fmoc-SPPS研究目前专注于解决两个主要问题,包括长肽合成过程中的聚集和某些序列中天冬酰亚胺的形成。
长肽合成过程中的聚集问题,可采取使用低取代树脂分离肽链、使用微波减少反应时间、混合溶剂作为反应溶液以及使用伪脯氨酸打破肽链骨架的氢键等方法,以避免或减少SPPS过程中的聚集。
天冬酰亚胺在Fmoc-SPPS过程中的形成显著降低了原始肽的纯度。减少天冬酰亚胺形成的解决方案包括使用微波减少反应时间、使用N-α-烷基天冬酸-甘氨酸二肽或在脱保护过程中添加1-羟基苯并三唑(HOBt)、Oxyma Pure。
固态多肽合成已成为目前多肽合成的首选,但固相合成仍存在许多缺点:
缩合及洗涤过程中对环境不友好的溶剂(DCM和DMF等)和缩合剂的大量使用使得成本过高并引起浪费。因此当合成大规模的短肽时,液相合成法(LPPS)相对更合适。而且随着液相+flow技术的发展,LPPS也将是未来多肽药物公斤或吨级规模生产的重要工艺路线。
固相多肽合成的难度属于序列依赖性,尽管合成能力上限一直在不断提高,但长于50个氨基酸的肽(尤其是在大规模制造中)仍然难以通过固相合成一次性获取。片段合成法是近年来发展较快的多肽合成方法,其化学专一性在长肽合成领域具有突出作用。片段合成法的核心思想是将目标肽合理地分为若干片段,在合成这些片段后进行连接缩合,最终得到目标肽。目前,应用最广泛的连接技术是自然化学连接(NCL)。该技术由芝加哥大学的Kent等于1994年提出,通过一个多肽片段的C-端硫酯与另一个N-端Cys多肽片段的选择性化学反应,在连接位点处形成天然酰胺键。早期, C-端硫酯的合成受到稳定性差的困扰,近年来通过酰肼氧化的C-端硫酯原位合成及连接策略极大地促进了这一方法的应用。多肽片段合成的其他连接方式还有天然化学连接、化学区域选择连接、可去除辅助基连接、光敏感辅助基连接、施陶丁格连接和正交化学连接等。此外,在多肽片段合成法中,企业可以片段外包,分包生产。CDMO可以提供多种服务,包括多肽片段的合成、纯化、结构鉴定、质量控制等。因此肽片段合成法已经成为多肽药物制备的重要手段之一。
尽管固相合成是目前多肽工艺生产的主要方式,但液相合成也有不可替代的优势。不同于经典的液相多肽合成,如今的液相手段增加了可溶性C-端标签(Tag)策略,但因其标签巨大的亲脂性,可以通过简单的沉淀、过滤或萃取得到这些多肽-标签的加合物中间体,从而实现类似于固相合成的洗脱法去除过量试剂和副产品的目的。此外,液相+flow技术的兴起为化学合成多肽提供了新的方法,可以解决传统单纯固相SPPS合成,溶剂用量高,排放高的问题,同时液相flow技术还将进一步提高生产工艺效率。
随着对多肽研究的不断深入,多肽合成长度和化学修饰复杂程度不断提高,对多肽合成工艺水平提出了更高要求,单一的合成方法往往不能满足需求,研究者常将多种方法结合使用。例如诺和诺德的司美格鲁肽采取发酵+固相合成,该方法通过发酵法制备GLP-1前体分子,然后通过固相法制备最终产物司美格鲁肽。礼来的替尔泊肽便采用固相+液相多肽合成方法,先通过固态合成某几个片段,再通过液相合成最终的产物。
多肽药物由于技术门槛较高,主要玩家多为深耕多肽领域多年的专业企业。国际老牌知名多肽原料药生产企业包括Bachem、Polypeptide等凭借项目经验、地缘优势、客户关系和政策壁垒,长期占据垄断地位。
近年来,随着我国企业在多肽领域的不断投入和努力,多肽生产技术不断发展提升。目前我国已成为多肽原料药出口大国,同时生产的多肽原料药逐渐从低端产品逐渐转向氨基酸个数更多和结构更加复杂的中高端产品,代表企业包括诺泰生物、昂博等老牌多肽企业,以及博腾等新一代具备多肽研发生产能力的CDMO企业。
小结
多肽药物凭借其作为天然生物分子的独特属性,对人类的高度特异性和低毒性,已成为创新药的新重点。随着需求的增加,多肽制药工艺研究成为当前多肽研究的前沿与热点,特别是化学合成法的广泛使用极大地提高了多肽药物的工业化效率。但同时也应当注意到多肽制药工艺存在试剂用量多等诸多问题与挑战,需要多肽药物研究者与从业者共同努力不断改进。
随着绿色多肽工艺的开发和应用、人工智能自动化控制技术等新技术与多肽合成工艺的有效融合,多肽制药工艺将得到进一步发展和提高,助推更多的多肽药物进入市场造福更多大众。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030