https://www.cphi.cn 2024-03-22 11:09 来源:药渡Daily 作者:黄仲平
非酒精性脂肪肝病(NAFLD)是指与大量饮酒无关的、超过肝脏重量5%的脂肪堆积引起的肝脏变性,是一种代谢应激性肝损伤。NAFLD通常是患者出现代谢问题的综合表现,常与肥胖、高血压、糖尿病等相关联,是最常见的慢性肝病之一。进一步发展之后,NAFLD会演变成为非酒精性脂肪肝炎(NASH)。
由于NASH极其复杂的病理机制,导致治疗NASH药物迟迟无法问世。但这无药可治的历史,在这个多彩的春天被彻底终结,NASH的治疗从此进入崭新的阶段。
01
历史的里程碑
3月15日,Madrigal公司重磅宣布其治疗NASH新药Rezdiffra(Resmetirom)获美国FDA批准上市,适应症为联合饮食和运动用于成人非肝硬化非酒精性脂肪性肝炎(NASH)伴中度至晚期肝纤维化(与F2至F3期纤维化一致)的治疗。
Resmetirom是一款每日一次口服的THR-β激动剂,旨在针对NASH关键的疾病机理。Resmetirom的加速批准基于III期MAESTRO-NASH临床试验结果,该结果医发表在《新英格兰》医学杂志上。
MAESTRO-NASH是一项关键性、多中心、随机、双盲、安慰剂对照试验,纳入了1759名经活检证实患有NASH的患者。经过52周的治疗后,Resmetirom的100毫克和80毫克剂量在两个主要终点上均显示出相对于安慰剂的统计学上显著的改善:NASH缓解(包括非酒精性脂肪性肝病[NAFLD]活动评分降低≥2分),且纤维化没有恶化;纤维化至少改善一个阶段,且NAFLD活动评分没有恶化。无论年龄、性别、2型糖尿病状态或纤维化阶段如何,纤维化的改善和NASH的缓解都是一致的。
Resmetirom作用机制
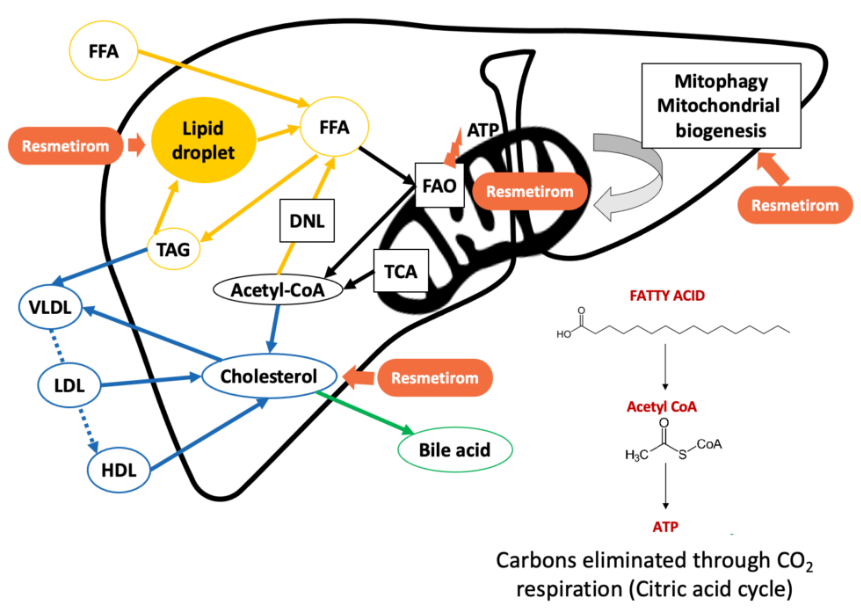
图片来源:官网
这是首 款获FDA批准的NASH疗法,具有历史性的里程碑意义,意味着NASH无药可治的时代已经一去不复返了。
02
百亿美元大市场
截至目前,研究领域对NAFLD、NASH的发病机制依旧没有统一的认识。根据最新研究,NAFLD/NASH的发病由最初的二重打击学说发展为多重打击学说。
二重打击学说认为,脂肪堆积带来的胰岛素抵抗是一次打击,在此基础上,脂肪酸的过氧化所产生了炎症和氧化应激反应形成二次打击,最终诱导形成NAFLD/NASH。
而多重打击学说认为,除了上述两个核心因素,还有多个因素,包括但不限于胰岛素抵抗、慢性炎症、纤维化、免疫和肠道菌紊乱,氧化应激、激素失调等,涉及肝脏、肠道和脂肪组织中的各种细胞。
除了尚未探明的发病机制,缺乏有效的治疗目标、安全性和耐受性都治疗NASH药物迟迟不能面世的主要原因。NASH没有像糖尿病那样明确的生物标志物,可以用来监测药物治疗的效果,通常需要使用肝活检等昂贵并且具有侵入性的方法来评估药物的疗效,这使得临床试验更加复杂和昂贵。另外,肝脏是药物代谢的主要器官,因此任何影响肝脏的药物都在安全性方面如履薄冰。
当前全球NASH新药在研项目仍然主要集中在小分子、多肽和单抗等传统药物,Arrowhead、Ionis和Alnylam公司也在探索多款RNA疗法。被广泛研究的NASH靶点主要分为5类,分别是(1)针对脂质代谢的靶点包括PPAR、FGF19/21、FASN;(2)糖代谢靶点GLP-1、FGF21等;(3)胆固醇代谢靶点THR-β、FXR、FGF19;(4)抗炎靶点CCR2/5和ASK1;(5)抗纤维化靶点如ASK1、LOXL-2、Gal-3等。
NASH治疗相关的作用机制和靶点
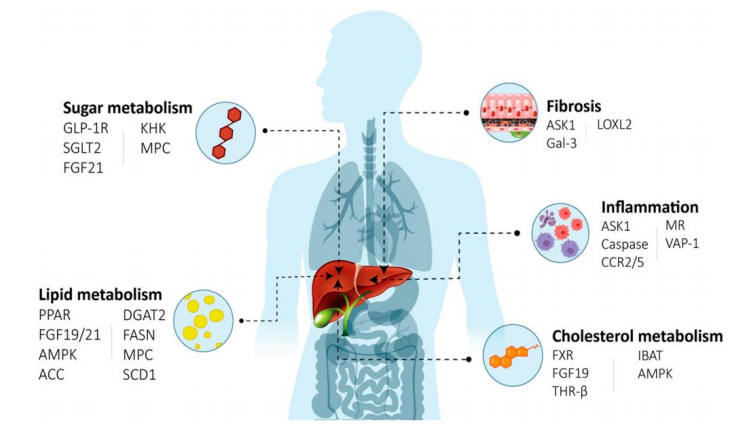
图片来源:中信证券研报
但是,NASH相关药物研发至今已接近40年,却进展寥寥。
2020年,曾经被认为是最有希望成为第一个NASH新药的FXR激动剂奥贝胆酸上市申请被FDA拒绝,推测原因为相对安慰剂疗效不够显著且副作用明显。吉利德、诺华、Genfit和Albireo等公司也纷纷在NASH研究中遭遇挫折。
此外,还有不少药物在NASH研究中遭遇挫折,包括ACC抑制剂Firsocostat、Gal-3抑制剂Belapectin、caspase抑制剂Emricasan和SSAO/VApor-1抑制剂BI1467335等针对不同机制的靶向药物,受挫的原因或是TG升高、或是无效、或是界面肝炎等。
部分NASH相关失败药物
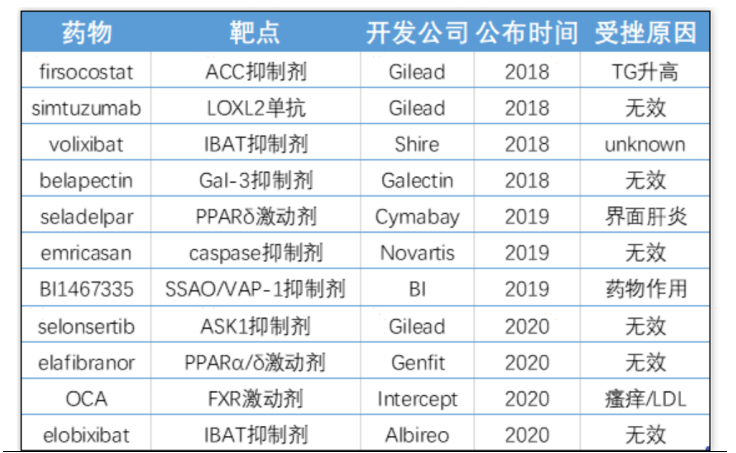
图片来源:光大证券研报
根据Cell上发表的文章统计,全球有接近1/4的人群受NAFLD影响。弗若斯特沙利文数据显示,全球NAFLD人群稳步增长,预计2030年将达到24.3亿人,对应NASH患者则将达到4.9亿人,NASH治疗药物的全球市场规模有望在2030年突破300亿美元。
中国由于老龄化、糖尿病、肥胖等多种因素驱动,NAFLD及NASH人群将以更快的速度增长,NAFLD已成为我国第一大慢性肝病,严重危害我国人民生命健康,预计到2030年NAFLD及NASH患病人数将增至2.78/0.56亿人,NASH治疗市场也将在2030年突破300亿人民币。
面对这么一块处女地,不论是跨国大药企还是Biotech都虎视眈眈,相继投入重金研发。根据药渡数据,目前全球共有435个NASH在研药物,涉及300家企业,其中国IND以上研发阶段的药物共计201个,占比达到46%。
03
种子选手
在国内,目前布局NASH药物的企业不在少数,有歌礼制药、众生药业、正大天晴、四环医药、石药集团、拓臻生物、微芯生物、雅创医药、圣和药业、豪森药业等等。
中国药企NASH研发进程
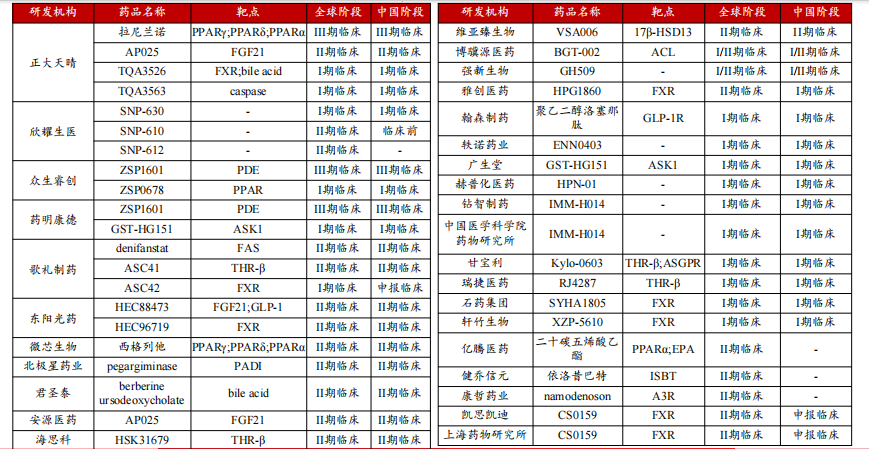
图片来源:方正证券研报
THR-β(甲状腺受体)激动剂
THR-β是在肝细胞中高度表达的甲状腺激素受体,被激活后可以促进甲状腺激素生成,同时调节血脂。由于NASH患者中观察到甲状腺衰退以及较低的THR-β活动水平,因此研究者发起了对THR-β激动剂的研究。根据研究,THR-β激动剂可以通过五种途径保持肝脏健康:控制脂肪合成;调解脂肪氧化;调解线粒体活动;控制胆固醇合成;直接抑制炎症和纤维化。
在国内,进度最快的THR-β激动剂是歌礼制药的ASC41,目前处在临床II期。此前在已经完成的临床I期试验中,经过14天或28天每日口服10mg药物的患者,在血清各项指标出现明显改善。
2024年1月,歌礼制药公布了ASC41片用于治疗经肝穿活检证实的非酒精性脂肪性肝炎(NASH)患者的52周II期临床试验取得积极期中结果。
期中结果显示:经磁共振成像质子密度脂肪分数(MRI-PDFF)评估,患者服用ASC41片12周后,肝脏脂肪含量较基线的相对降幅平均值高达68.2%,且肝脏脂肪含量、肝脏炎症生物标志物ALT和AST及血脂数据均较基线出现显著降低。其中,高达93.3%的患者肝脏脂肪含量较基线相对降低30%及以上。凭借以上临床数据,ASC41有望成为同类最 佳的THR-β激动剂。
海思科自主研发的HSK31679也是一种高选择性甲状腺激素β受体(THR-β)激动剂。根据药渡数据,HSK31679正在开展一项II期临床研究,旨在评估HSK31679片在中国NASH患者中的有效性与安全性。
PPAR激动剂
PPAR是一种调解代谢的转录因子,包括PPARα、PPARβ/δ和PPARγ三种亚型。PPARα在肝脏中高度表达,其活化可以降低肝部甘油三酯的水平。PPARβ/δ的活化则可以促进脂肪代谢,并抑制巨噬细胞介导的炎症反应。PPARγ的活化则可以减少自由脂肪酸在肝脏的堆积,同时抑制肝细胞纤维化。激活所有的PPAR靶点可以全方位改善NASH疾病。
Inventiva的Lanifibranor是一种泛PPAR激动剂,可以激活全部的PPAR靶点,也是目前唯一一个处于临床阶段的泛PPAR激动剂。Lanifibranor在2021年9月开展临床III期试验,并在2022年9月被中国生物制药引进到中国开展临床试验,正大天晴拥有该药在大中华区的独家许可。
此前在关键临床II期中,接受每日1200mg药物治疗的患者达到了降低SAF评分(达到主要终点,脂肪变性活动性纤维化评分)改善的主要终点,以及NASH消退、纤维化无恶化的次要终点。在安全性上,安慰剂组、800mg治疗组合1200mg治疗组没有统计学差异,不过相较于FXR激动剂和THR-β激动剂,该试验中出现了患者体重增加和四肢水肿的副作用。根据药渡数据显示,Lanifibrano正在中国开展一项多中心、随机、双盲、安慰剂对照扩展治疗的III期研究。
FGF21类似物
成纤维细胞生长因子21(FGF21)是一种肝细胞因子,是主要通过肝脏分泌的多肽类 激素,通过FGF21受体调解糖代谢、脂代谢、胰岛素抵抗等生理活动。FGF21主要和细胞膜受体β-klotho及FGF受体家族结合,在临床前模型中可以改善肥胖、糖尿病、NASH等疾病症状,具有明显的体重控制和血糖控制的效果。
国内布局的企业有正大天晴、安源医药和东阳光药。TQA2225是正大天晴开发的一款超长效注射用重组人FGF21-Fc融合蛋白,目前正在进行临床II期试验;AP025是安源医药自研的用构建融合蛋白的连接肽技术研发的一款长效重组人FGF21-Fc融合蛋白,也是全球第一款进入临床的全人源长效FGF21蛋白,目前在国内也处于II期。
GLP-1受体激动剂
GLP-1是一种小肠分泌的内源性激素,可以加强胰岛素分泌并抑制胰高血糖素分泌,是重要的血糖平衡调节因子。目前GLP-1受体激动剂代表产品有利拉鲁肽、索玛鲁肽、司美格鲁肽,已成为重要的减肥药和糖尿病治疗药物。由于这类药物对于控制体重和血糖具有良好效果,因此也被用于开发NASH适应症。
目前进展最快司美格鲁肽已经公布临床II期数据,并在2021年启动临床III期试验,该国际多中心III期临床研究目前也已经在中国启动。
在临床II期试验中,受试者按1:1:1:1比例随机分配接受司美格鲁肽0.1mg、0.2mg、0.4mg或安慰剂每日一次皮下注射,治疗72周。结果表明,以上四组受试者中达到主要终点的比例分别为40%、36%、59%、17%,三组治疗组均较安慰剂组产生显著差异;而达到次要终点的比例则分别为49%、32%、43%、33%,并无显著差异。
司美格鲁肽临床2期单药数据
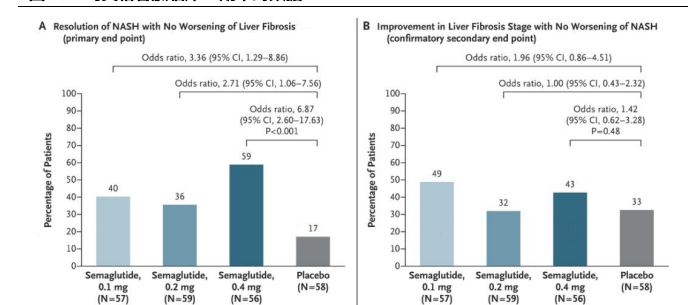
图片来源:光大证券研报
翰森制药、华东医药、东阳光药和派格生物/天士力等国内药企也布局了治疗NAFLD/NASH的GLP-1类药物。
FASN(脂肪酸合成酶)抑制剂
脂肪酸合成酶主要驱动脂肪酸的从头合成,并介导了炎症及纤维化的信号传导。在NAFLD/NASH患者中,肝部FASN的活跃程度明显比健康人要高,并明显地更多合成了棕榈酸酯。棕榈酸酯进一步代谢,则可能生成脂肪导致肝脂肪变性,或支持成纤维化细胞生长,或代谢为促炎症/促纤维化的脂氧素,造成脂毒性,因此抑制FASN的活性是治疗NAFLD/NASH的一个潜在方法。
目前,歌礼制药的FASN抑制剂ASC40是我国进度最快的NASH治疗药物之一,仅次于正大天晴的的Lanifibranor。ASC40是歌礼制药通过对Sagimet的战略投资取得的。
在2023年6月的欧洲肝病学会年会上,Sagimet公布了ASC40治疗NASH患者IIb期临床试验的中期数据:治疗组患者的甘油三酯、LDL、肝脏脂肪分数、ALT、增强纤维化评分、FGF21等指标均有明显的改善,有半数以上的患者肝脏脂肪分数下降了超过50%,显著的临床结果无疑进一步推高了其未来市场预期。Sagimet将于今年第一季度公布Denifanstat(ASC40)用于NASH的II期临床肝穿活检数据。
除以上,国内布局NASH进展较快的项目还包括众生药业的PDE抑制剂ZSP1601、君圣泰的小檗碱熊去氧胆酸盐(HTD1801)、维亚臻生物的靶向肝细胞内羟基类固醇17-β脱氢酶13(HSD17β13)等等。
04
结语
首 款治疗NASH药物的获批固然可喜,但是在尚未完全明确病因的情况下,这些药物的开发也仅仅只能缓解,离真正的成功还有十分遥远的距离。不过在百亿美元市场的刺激下,百花齐放的局面令人欣慰,无数科学家不懈的努力,在未来更先进研发手段的加持下,NASH这一难题总有一天会被攻克。后续发展如何,药渡还将持续关注。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030