https://www.cphi.cn 2018-01-11 10:33 و¥و؛گï¼ڑ转载 ن½œè€…ï¼ڑç³»ç»ںهگ›
ن¸€م€پو¦‚è؟°
1984ه¹´ه›½ن¼ڑé€ڑè؟‡ن؛†م€ٹèچ¯ه“پن»·و ¼ç«ن؛‰ه’Œن¸“هˆ©وœںن؟®و£و،ˆم€‹ï¼ˆHatch-Waxman Amendment),ن؟®è®¢هگژ çڑ„م€ٹèپ”邦é£ںه“پم€پèچ¯ه“په’ŒهŒ–ه¦†ه“پو³•و،ˆم€‹505部هˆ†ن¸؛و–°èچ¯ç”³è¯·وڈگن¾›ن؛†ن¸‰و،è·¯ه¾„ï¼ڑ
505(b)(1)ï¼ڑ申请هŒ…هگ«ه®Œو•´ه®‰ه…¨و€§ه’Œوœ‰و•ˆو€§ç ”究وٹ¥ه‘ٹ
505(b)(2)ï¼ڑ申请هŒ…هگ«ه®Œو•´ه®‰ه…¨و€§ه’Œوœ‰و•ˆو€§ç ”究وٹ¥ه‘ٹ,ن½†è‡³ه°‘وœ‰éƒ¨هˆ†ن؟،وپ¯و¥و؛گن؛ژé申请者ه¼€ه±•وˆ–申请者و— وƒه¼•ç”¨çڑ„ç ”ç©¶م€‚
505(j) ï¼ڑ申请هŒ…هگ«ن؟،وپ¯è¯پوکژو‹ں申وٹ¥èچ¯ç‰©ن¸ژهڈ‚و¯”هˆ¶ه‰‚وœ‰ç€ه®Œه…¨ç›¸هگŒçڑ„و´»و€§وˆگهˆ†م€په‰‚ه‹م€پ规و ¼م€پç»™èچ¯é€”ه¾„م€پو ‡ç¾ن؟،وپ¯م€پè´¨é‡ڈم€پ特و€§ه’Œé€‚ه؛”ç—‡ç‰م€‚
505(b)(1)ه’Œ505(b)(2)被称ن¸؛و–°èچ¯ç”³è¯·ï¼ˆNDA),而505(j)هˆ™è¢«ç§°ن¸؛简略و–°èچ¯ç”³è¯·ï¼ˆANDA)م€‚505(b)(2)申وٹ¥هŒ…و‹¬و–°é€‚ه؛”ç—‡م€پو–°ç»„هگˆم€پو–°ه¤„و–¹م€پو–°ه‰‚ه‹ç‰ï¼Œç±»ن¼¼ن؛ژه›½ه†…هŒ–ه¦و³¨ه†Œو–°هˆ†ç±»çڑ„و”¹è‰¯ه‹و–°èچ¯م€‚
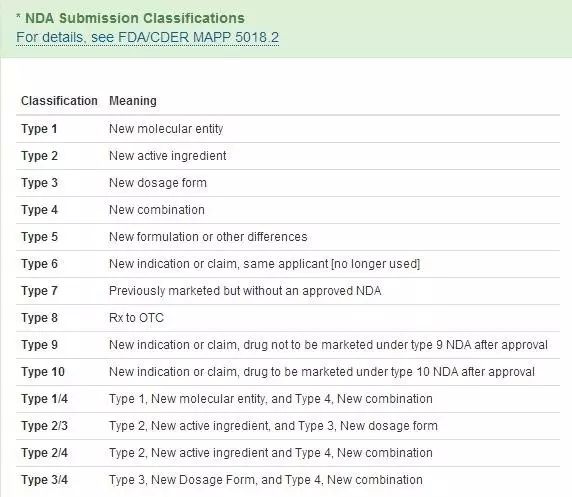
وچ®و±¤و£®è·¯é€ڈوٹ¥éپ“,و”¹è‰¯ه‹و–°èچ¯ç›®ه‰چه·²ç»ڈوˆگن¸؛ه…¨çگƒو–°èچ¯ç ”هڈ‘çڑ„趋هٹ؟م€‚ن»¥ç¾ژه›½ن¸؛ن¾‹ï¼Œن»ژ2002ه¹´هˆ°2015ه¹´FDAو‰¹ه‡†çڑ„و–°èچ¯ç±»هˆ«هڈٹو•°é‡ڈو¥çœ‹ï¼Œهœ¨2010ه¹´ه‰چهگژهڈ‘ç”ںن؛†وکژوک¾çڑ„هڈکهŒ–م€‚2010ه¹´ن¹‹ه‰چ,505(b)(1)هچ ن¸»ه¯¼ï¼Œ2010ه¹´ن¹‹هگژ,505(b)(2)é€گو¸گه‘ˆن¸ٹهچ‡è¶‹هٹ؟,ه¹¶é€گو¸گ赶超505(b)(1),2015ه¹´505(b)(2)ن»¥46:37çڑ„و¯”ن¾‹è¶…è؟‡505(b)(1)م€‚
ن؛Œم€پ2017ه¹´FDAو‰¹ه‡†çڑ„و–°ه‰‚ه‹ن؛§ه“پ
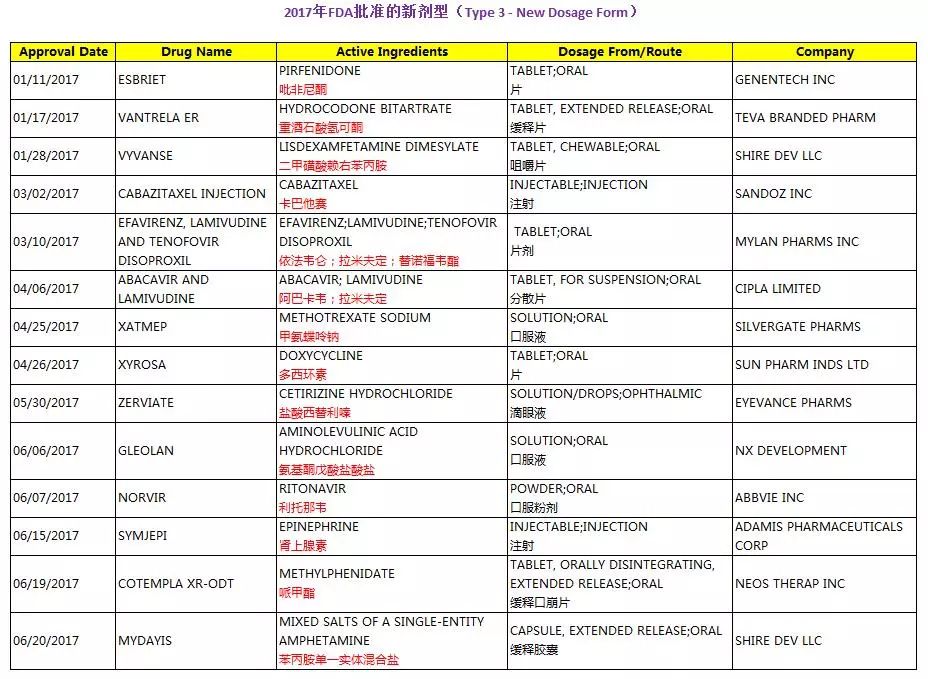
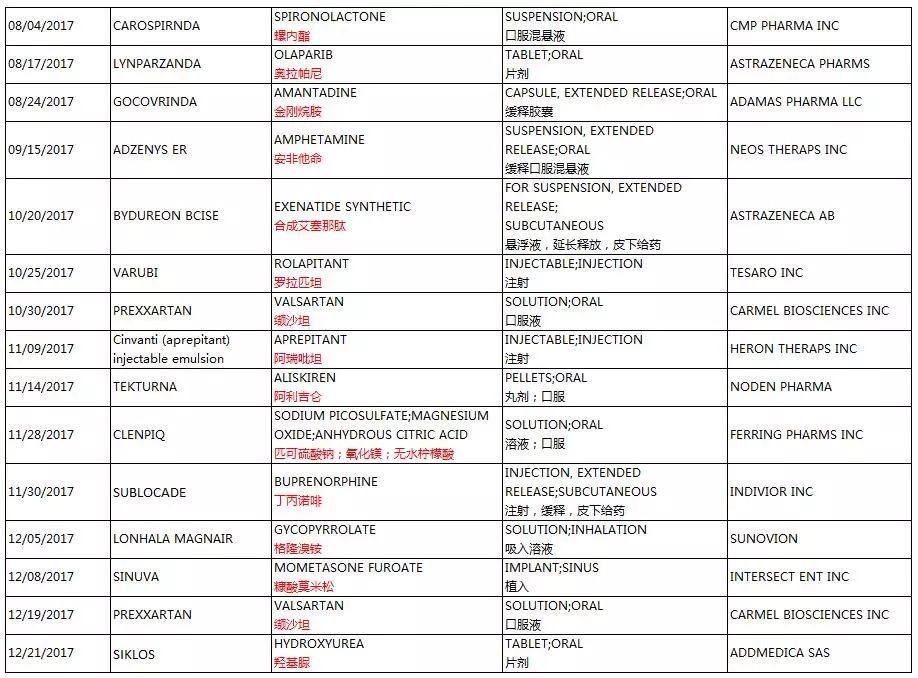
2017ه¹´ه؛¦ï¼ŒFDAن¸€ه…±و‰¹ه‡†ن؛†29ن¸ھو–°ه‰‚ه‹çڑ„و–°èچ¯ç”³è¯·ï¼ˆType 3 - New Dosage Form)م€‚
ن¸‰م€پ部هˆ†و–°ه‰‚ه‹ç®€ن»‹
1م€پVantrela ER(é‡چé…’çں³é…¸ن؛Œو°¢**酮缓é‡ٹ片)
Vantrela ERوک¯ç”±ن»؟هˆ¶èچ¯ه·¨ه¤´و¢¯ç“¦ï¼ˆTeva)ه…¬هڈ¸ه¼€هڈ‘çڑ„ه…·وœ‰و»¥ç”¨ه¨پو…‘特و€§çڑ„é•؟و•ˆéک؟ 片类و¢ç—›èچ¯ï¼Œè¯¥èچ¯é‡‡ç”¨و¢¯ç“¦ن¸“هˆ©و€§çڑ„و»¥ç”¨ه¨پو…‘وٹ€وœ¯ه¼€هڈ‘,هڈ¯éک²و¢èچ¯ç‰©وˆگهˆ†é€ڑè؟‡3ç§چوœ€ه¸¸è§پçڑ„途ه¾„و»¥ç”¨ï¼ڑهڈ£وœچم€پé¼»ه†…م€پé™è„‰و³¨ه°„م€‚
Vantrela ER适用ن؛ژ疼痛ن¸¥é‡چهˆ°éœ€è¦پو—¥ه¸¸çڑ„م€په…¨ه¤©ه€™çڑ„م€پé•؟وœںçڑ„éک؟ 片类èچ¯ç‰©و²»ç–—م€پن»¥هڈٹ采用ه…¶ن»–镇痛èچ¯و— و³•وœ‰و•ˆوژ§هˆ¶ç–¼ç—›çڑ„ç®،çگ†ï¼Œن½†è¯¥èچ¯ن¸چ适用ن؛ژن»…هœ¨éœ€è¦پو—¶ن¸´و—¶وœچ用م€‚
و¢¯ç“¦ه…¨çگƒç‰¹ç§چèچ¯ه“پ部门و€»è£په…¼é¦–ه¸و‰§è،Œه®کRob Koremansè،¨ç¤؛,该ه…¬هڈ¸و·±هˆ»çگ†è§£ه¤„و–¹èچ¯و»¥ç”¨é£ژ险وک¯ه½“ه‰چهŒ»ç–—ن؟هپ¥ن¸“ن¸ڑن؛؛ه‘کهœ¨و²»ç–—و…¢و€§ç–¼ç—›و–¹é¢و‰€é¢ه¯¹çڑ„é‡چه¤§وŒ‘وˆکم€‚ه°½ç®،و²،وœ‰ه“ھç§چوٹ€وœ¯هڈ¯ن»¥ه®Œه…¨و¶ˆé™¤و»¥ç”¨ï¼Œن½†è¯¥ه…¬هڈ¸ه¼€هڈ‘çڑ„و»¥ç”¨-ه¨پو…‘ن؛§ه“پن»چوک¯ن¸€ن¸ھé‡چè¦پçڑ„è؟›و¥ï¼Œه°†ن¸؛ه¤„و–¹هŒ»ه¸ˆوڈگن¾›é‡چè¦پçڑ„选و‹©ï¼Œو¥ه¸®هٹ©éک»و¢وˆ–ه‡ڈه°‘و»¥ç”¨ï¼ŒهگŒو—¶è®©وœ€éœ€è¦پéک؟ 片类و²»ç–—èچ¯ç‰©çڑ„و‚£è€…能ه¤ںèژ·هڈ–هˆ°و‰€éœ€çڑ„镇痛èچ¯ç‰©م€‚
2م€پVyvanse(ن؛Œç”²ç£؛酸赖هڈ³è‹¯ ن¸™ èƒ؛ه’€هڑ¼ç‰‡ï¼‰
2017ه¹´1وœˆ28و—¥ï¼ŒFDAو‰¹ه‡†ن؛†Shireه…¬هڈ¸çڑ„و–°ه‰‚ه‹Vyvanseه’€هڑ¼ç‰‡ï¼ˆن؛Œç”²ç£؛酸赖هڈ³è‹¯ ن¸™ èƒ؛ه’€هڑ¼ç‰‡ï¼‰ï¼Œç”¨ن؛ژو²»ç–—و³¨و„ڈç¼؛é™·ه¤ڑهٹ¨éڑœç¢چ(ADHD)ه’Œن¸ه؛¦è‡³é‡چه؛¦وڑ´é£ں症(BED)م€‚
ن½؟用ن؛Œç”²ç£؛酸赖هڈ³è‹¯ ن¸™ èƒ؛و²»ç–—,و‚£è€…وœ€ه¸¸è§پçڑ„ن¸چ良هڈچه؛”هŒ…و‹¬ï¼ڑهڈ£ه¹²ï¼Œه¤±çœ ,ه؟ƒçژ‡هٹ ه؟«ï¼Œن¸چه®‰ï¼Œن¾؟ç§کهڈٹ焦虑م€‚
2007ه¹´ï¼ŒFDAو‰¹ه‡†ن؛Œç”²ç£؛酸赖هڈ³è‹¯ ن¸™ èƒ؛胶ه›ٹ(赖و°¨é…¸ه®‰éن»–ه‘½ï¼Œه¸Œé›·ï¼ˆShire)ه…¬هڈ¸ï¼‰ç”¨ن؛ژو²»ç–—6ه²پهڈٹن»¥ن¸ٹه„؟ç«¥çڑ„و³¨و„ڈهٹ›ç¼؛é™·ن¼´ه¤ڑهٹ¨éڑœç¢چم€‚
2015ه¹´ï¼ŒFDAو‰¹ه‡†Vyvanse胶ه›ٹ用ن؛ژن¸ه؛¦è‡³é‡چه؛¦وڑ´é£ں症(BED)çڑ„و²»ç–—,è؟™وک¯ç¬¬ن¸€ç§چèژ·FDAو‰¹ه‡†çڑ„用ن؛ژو²»ç–—و¤ç±»ç–¾ç—…çڑ„èچ¯ç‰©م€‚该病هœ¨ç¾ژه›½وœ‰250ن¸‡ه·¦هڈ³çڑ„و‚£è€…,وک¯è¯¥و²»ç–—领هںںçڑ„首èچ¯ï¼Œè§£ه†³ن؛†و— èچ¯هڈ¯و²»çڑ„é—®é¢کم€‚ن¸ه›½ه†œو‘ه¥³و€§وڑ´é£ںç—‡هڈ‘ç—…çژ‡ن¸؛10ن¸‡هˆ†ن¹‹7,هںژه¸‚ه¥³و€§ن¸ن¸؛10ن¸‡هˆ†ن¹‹16.7,而هœ¨ن؛؛هڈ£è¶…è؟‡10ن¸‡çڑ„ه¤§هںژه¸‚,è؟™ن¸€و•°ه—ن¸؛10ن¸‡هˆ†ن¹‹25.5,و‰€ن»¥è؟™ن¸ھèچ¯ç‰©éه¸¸ه€¼ه¾—ه…³و³¨م€‚
2016ه¹´4وœˆ14و—¥ï¼ŒShireه…¬هڈ¸ه®£ه¸ƒهگ‘FDAوڈگن؛¤Vyvanseو–°و›؟ن»£هˆ¶ه‰‚ه’€هڑ¼ç‰‡çڑ„و–°èچ¯ç”³è¯·ï¼Œè¯¥هˆ¶ه‰‚适ن؛ژهگه’½وˆ–و‰“ه¼€èƒ¶ه›ٹوœ‰ه›°éڑ¾çڑ„و‚£è€…م€‚Vyvanse胶ه›ٹهڈ¯و•´ç²’هگه’½وˆ–و‰“ه¼€ه°†ه†…ه®¹ç‰©و··ه…¥و°´ï¼Œو©™و±پوˆ–é…¸ه¥¶ن¸وœچ用م€‚Vyvanseه’€هڑ¼ç‰‡ه°†ن¸؛و‚£è€…وڈگن¾›هڈ¦ن¸€é€‰و‹©م€‚هœ¨ç¾ژه›½ï¼ŒVyvanse胶ه›ٹ适用ن؛ژه…ه²پهڈٹن»¥ن¸ٹو³¨و„ڈهٹ›ç¼؛é™·/ه¤ڑهٹ¨éڑœç¢چو‚£è€…ه’Œوˆگن؛؛ن¸è‡³é‡چه؛¦وڑ´é£ںç—‡çڑ„و²»ç–—م€‚
3م€پXATMEP(甲و°¨è¶ه‘¤هڈ£وœچو¶²ï¼‰
Silvergate Pharmaceuticalsه®£ه¸ƒï¼Œ2017ه¹´4وœˆ25و—¥ç¾ژه›½FDAو‰¹ه‡†XATMEP(甲و°¨è¶ه‘¤ï¼‰هڈ£وœچو؛¶و¶²ن¸ٹه¸‚,è؟™وک¯é¦–ن¸ھç»ڈFDAو‰¹ه‡†çڑ„甲و°¨è¶ه‘¤هڈ£وœچو؛¶و¶²م€‚XATMEP用ن؛ژو²»ç–—ه„؟科و‚£è€…çڑ„و€¥و€§و·‹ه·´ç»†èƒو€§ç™½è،€ç—…(ALL)ه’Œه¤ڑه…³èٹ‚و€§é’ه°‘ه¹´ç‰¹هڈ‘و€§ه…³èٹ‚ç‚ژ(pJIA)م€‚
XATMEPوک¯ن¸€ç§چهڈ¶é…¸ç±»ن¼¼ç‰©ن»£è°¢وٹ‘هˆ¶ه‰‚,适用ن؛ژه¤ڑه…³èٹ‚و€§é’ه°‘ه¹´ç‰¹هڈ‘و€§ه…³èٹ‚ç‚ژ(pJIA)çڑ„ه„؟科و‚£è€…çڑ„و´»è·ƒو€§ç–¾ç—…ç®،çگ†ï¼Œن»–ن»¬ه¯¹ه…¨ه‰‚é‡ڈé甾ن½“وٹ—ç‚ژèچ¯ï¼ˆNSAID)çڑ„ن¸€ç؛؟و²»ç–—هڈچه؛”ن¸چ足وˆ–ن¸چè€گهڈ—ï¼›ن¹ں适用ن؛ژو²»ç–—و€¥و€§و·‹ه·´ç»†èƒç™½è،€ç—…(ALL)çڑ„ه„؟科و‚£è€…,ن½œن¸؛ه¤ڑوœںèپ”هگˆهŒ–ç–—ç»´وŒپو–¹و،ˆçڑ„ن¸€éƒ¨هˆ†م€‚
XATMEP(甲و°¨è¶ه‘¤ï¼‰هڈ£وœچو؛¶و¶²çڑ„ه¼€هڈ‘ن¸»è¦پوک¯ن¸؛ن؛†و»،足ن¸ٹè؟°é€‚ه؛”ç—‡çڑ„需è¦پم€‚ه®ƒوک¯ن¸€ç§چهچ³ç”¨ه‹2.5 mg/mLن؛§ه“پ,ن¾؟ن؛ژèچ¯ه“په‰‚é‡ڈçڑ„ه‡†ç،®و€§ه’Œوک“ن؛ژو–½ç”¨م€‚هœ¨و¤ن¹‹ه‰چ,و²،وœ‰ç»ڈFDAو‰¹ه‡†çڑ„甲و°¨è¶ه‘¤هچ³ç”¨ه‹هڈ£وœچو¶²ن½“هˆ¶ه‰‚هڈ¯ن¾›ه„؟科و‚£è€…ن½؟用م€‚هŒ»ه¸ˆéœ€è¦پن½“è،¨é¢ç§¯ï¼ˆBSA)给èچ¯ï¼Œè€Œو‚£è€…ه±•ç¤؛ن؛†هگه’½ن¸چن¾؟م€پن¸چ能وœچ用片ه‰‚م€پن»¥هڈٹé’ˆهˆ؛وپگوƒ§ç—‡ç‰ه›°éڑ¾م€‚XATMEPو ¹وچ®FDA规ه®ڑهœ¨CGMPن¸‹ç”ںن؛§م€‚ه®ƒو¶ˆé™¤ن؛†ه¯¹é’ˆه¤´و³¨ه°„م€پ粉ç¢ژوˆ–هˆ†è£‚片ه‰‚م€په°†ç‰‡ه‰‚ه¤چهگˆوˆگو¶²ن½“هˆ¶ه‰‚çڑ„è؟›ن¸€و¥هˆ¶ه¤‡éœ€è¦پم€‚
Silvergate Pharmaceuticalsو€»è£په…¼é¦–ه¸و‰§è،Œه®کçڑ„Frank Segraveه…ˆç”ں说ï¼ڑ“XATMEPوک¯ن¸€é،¹ن»¤ن؛؛و؟€هٹ¨çڑ„ن؛§ه“پ,ه®ƒن¸؛ه„؟ç«¥و‚£è€…وڈگن¾›ن؛†FDAو‰¹ه‡†çڑ„هچ³ç”¨ه‹ç”²و°¨è¶ه‘¤هڈ£وœچو¶²ï¼Œه†چو— 需针ه¤´م€پ粉ç¢ژ片ه‰‚وˆ–و··هگˆوˆگو¶²ن½“هˆ¶ه‰‚م€‚ن½œن¸؛ن¸€ه®¶هˆ¶èچ¯ه…¬هڈ¸ï¼Œوˆ‘ن»¬ç»§ç»ن¸“و³¨ن؛ژه¼€هڈ‘ه®‰ه…¨وœ‰و•ˆه¹¶ن¸”وک“ن؛ژو–½ç”¨çڑ„ه„؟科èچ¯ç‰©م€‚”
XATMEPوک¯ن¸€ç§چé€ڈوکژçڑ„黄色至و©™è‰²هڈ£وœچو؛¶و¶²ï¼Œو¯ڈو¯«هچ‡هگ«وœ‰2.5و¯«ه…‹ç”²و°¨è¶ه‘¤ï¼ˆç›¸ه½“ن؛ژ2.74و¯«ه…‹و°¨ç”²ه–‹ه‘¤é’ /و¯«هچ‡ï¼‰م€‚ éو´»و€§وˆگهˆ†هŒ…و‹¬ï¼ڑç؛¯هŒ–و°´ï¼Œوں وھ¬é…¸é’ ,وں وھ¬é…¸ï¼Œه¯¹ç¾ںهں؛è‹¯ç”²é…¸ç”²é…¯é’ ï¼Œه¯¹ç¾ںهں؛苯甲酸ن¸™é…¯é’ ه’Œن¸‰و°¯è”—ç³–م€‚هگ«وœ‰و°¢و°§هŒ–é’ وˆ–ç›گé…¸pHè°ƒèٹ‚ه‰‚م€‚
4م€پZERVIATE(ç›گé…¸è¥؟و›؟هˆ©ه—ھو»´çœ¼و¶²ï¼‰
2017ه¹´5وœˆ30و—¥ï¼ŒFDAو‰¹ه‡†ن؛†وٹ—组èƒ؛èچ¯è¥؟و›؟هˆ©ه—ھçڑ„首ن¸ھه±€éƒ¨çœ¼éƒ¨هˆ¶ه‰‚(ZERVIATE,ç›گé…¸è¥؟و›؟هˆ©ه—ھو»´çœ¼و¶²ï¼‰ï¼Œç”¨ن؛ژو²»ç–—ن¸ژè؟‡و•ڈو€§ç»“膜ç‚ژ相ه…³çڑ„眼部çک™ç—’م€‚
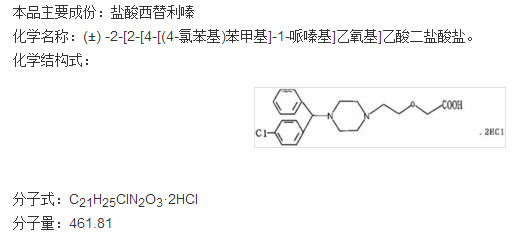
ç›گé…¸è¥؟و›؟هˆ©ه—ھç”±ه¼؛ç”ںç ”هڈ‘,ه¹¶ن؛ژ1995ه¹´12وœˆ8و—¥èژ·ç¾ژه›½é£ںه“پèچ¯ه“پ监ç£ç®،çگ†ه±€ï¼ˆFDA)و‰¹ه‡†ن¸ٹه¸‚,ه•†ه“پهگچن¸؛Zyrtec,ه‰‚ه‹ن¸؛片ه‰‚م€‚
ZERVIATE(ç›گé…¸è¥؟و›؟هˆ©ه—ھو»´çœ¼و¶²ï¼‰ç”±و³•ه›½ه…¬هڈ¸NICOXç ”ç©¶ه¼€هڈ‘م€‚ZERVIATEن¸؛و— èڈŒçœ¼ç”¨هˆ¶ه‰‚,规و ¼ن¸؛0.24%,و¯ڈmLهگ«è¥؟و›؟هˆ©ه—ھ2.40 mg(ç‰هگŒن؛ژ2.85 mgç›گé…¸è¥؟و›؟هˆ©ه—ھ),辅و–™ç»„وˆگن¸؛ï¼ڑ苯و‰ژو°¯é“µ0.010%(éک²è…گه‰‚); ç”کو²¹ï¼›ç£·é…¸و°¢ن؛Œé’ ; EDTA-2Naï¼›èپڑن¹™ن؛Œé†‡400ï¼› èپڑه±±و¢¨é…¯80ï¼›ç¾ںن¸™ç”²ç؛¤ç»´ç´ ï¼›ç›گé…¸/و°¢و°§هŒ–é’ ï¼ˆè°ƒèٹ‚pH); ه’Œو³¨ه°„用و°´م€‚ ZERVIATEو؛¶و¶²çڑ„pHه€¼ç؛¦7.0,و¸—é€ڈهژ‹ç؛¦300mOsm / kgم€‚هŒ…装规و ¼ï¼ڑ5mL/瓶;7.5mL瓶م€‚Zerviateوژ¨èچگه‰‚é‡ڈن¸؛1و»´ï¼Œو¯ڈه¤©2و¬،,间éڑ”ç؛¦8ه°ڈو—¶م€‚
5م€پCaroSpir(è؛ه†…é…¯هڈ£وœچو‚¬وµ®و¶²ï¼‰
2017ه¹´8وœˆ4و—¥ï¼Œç¾ژه›½FDAوœ€ç»ˆو‰¹ه‡†ن؛†CMP Pharmaه…¬هڈ¸çڑ„و–°èچ¯ç”³è¯·CaroSpir(è؛ه†…é…¯هڈ£وœچو‚¬وµ®و¶²ï¼Œ25mg/5mL),è؟™وک¯ç¬¬ن¸€ن¸ھن¹ںوک¯ه”¯ن¸€çڑ„FDAو‰¹ه‡†çڑ„هˆ©ه°؟ه‰‚çڑ„هڈ£وœچو¶²ن½“ه‰‚ه‹م€‚
CaroSpir(è؛ه†…é…¯هڈ£وœچو‚¬وµ®و¶²ï¼‰ç”¨ن؛ژو²»ç–—NYHAIII-IVه‹ه؟ƒهٹ›è،°ç«ه¹¶é™چن½ژه°„è،€هˆ†و•°ن»¥ه¢هٹ هکو´»çژ‡ï¼Œç®،çگ†و°´è‚؟ه¹¶ه‡ڈه°‘ن½ڈ院و²»ç–—ه؟ƒهٹ›è،°ç«çڑ„需è¦پ,ه¹¶ن¸”é€ڑه¸¸ن¸ژه…¶ن»–ç–—و³•èپ”هگˆن½؟用م€‚CaroSpirن¹ں被用ن½œو²»ç–—é«کè،€هژ‹çڑ„附هٹ و²»ç–—,é™چن½ژه…¶ن»–èچ¯ç‰©ن¸چ能ه……هˆ†وژ§هˆ¶çڑ„وˆگه¹´و‚£è€…çڑ„è،€هژ‹ï¼Œه¹¶ن½œن¸؛综هگˆو€§ه؟ƒè،€ç®،é£ژ险ç®،çگ†çڑ„ن¸€éƒ¨هˆ†م€‚وœ€هگژ,CaroSpir用ن؛ژç®،çگ†وˆگه¹´è‚ç،¬هŒ–و‚£è€…çڑ„و°´è‚؟,ه½“و°´è‚؟ه¯¹و¶²ن½“ه’Œé’ é™گهˆ¶و— هڈچه؛”و—¶م€‚
CMP Pharmaه…¬هڈ¸é¦–ه¸و‰§è،Œه®کGerald Sakowski说ï¼ڑ“CaroSpirه°†ن¸؛وˆگه¹´و‚£è€…,هŒ…و‹¬هگه’½ه›°éڑ¾وˆ–ن¸چ能هگه’½çڑ„و‚£è€…وڈگن¾›و–¹ن¾؟م€پوœ‰و•ˆçڑ„و¶²ن½“و²»ç–—选و‹©م€‚هˆ°ç›®ه‰چن¸؛و¢ï¼Œè؟™ن؛›و‚£è€…ç»ڈه¸¸وژ¥هڈ—ç”±هŒ»é™¢é…چهˆ¶çڑ„è؛ه†…é…¯و¶²ن½“ه½¢ه¼ڈèچ¯ç‰©و²»ç–—,è؟™ن¸ھه¤چهگˆو¶²ن½“çڑ„ç»™èچ¯ن¸چن¸€è‡´ï¼Œé•؟وœںن»¥و¥ن¸€ç›´وک¯هŒ»ç”ںçڑ„وŒپç»وŒ‘وˆکم€‚”
6م€پMydayis( 苯 ن¸™ èƒ؛هچ•ن¸€ه®ن½“و··هگˆç›گ缓é‡ٹ胶ه›ٹ)
2017ه¹´6وœˆ20و—¥ï¼ŒFDAو‰¹ه‡†ن؛†è‹±ه›½هˆ¶èچ¯ه•†Shireçڑ„é•؟و•ˆèچ¯ç‰©Mydayis( SHP465,苯 ن¸™ èƒ؛هچ•ن¸€ه®ن½“و··هگˆç›گن؛§ه“پ),用ن؛ژ13ه²پهڈٹن»¥ن¸ٹو³¨و„ڈç¼؛é™·ه¤ڑهٹ¨éڑœç¢چ(ADHD)و‚£è€…çڑ„و²»ç–—م€‚Mydayisوک¯ن¸€ç§چو¯ڈو—¥ن¸€و¬،çڑ„èچ¯ç‰©ï¼ŒهŒ…هگ«3ç§چن¸چهگŒç±»ه‹çڑ„èچ¯ç‰©ç¼“é‡ٹçڈ ,该èچ¯ن¸چ适用ن؛ژ12ه²پهڈٹن»¥ن¸‹ه„؟ç«¥ADHDو‚£è€…م€‚Shire预è®،,ه°†هœ¨ن»ٹه¹´ç¬¬ن¸‰ه£ه؛¦ه°†Mydayisوژ¨هگ‘ç¾ژه›½ه¸‚هœ؛م€‚
Shireه…¬هڈ¸é¦–ه¸و‰§è،Œه®کFlemming Ornskovè،¨ç¤؛,Mydayisوک¯è¯¥ه…¬هڈ¸وŒپç»è€•è€کADHD领هںں20ه¹´و¥çڑ„وœ€و–°هˆ›و–°ن؛§ه“پ,و¤و¬،و‰¹ه‡†ï¼Œه°†ن¸؛ADHD群ن½“وڈگن¾›ن¸€ç§چو¯ڈو—¥ن¸€و¬،çڑ„و²»ç–—选و‹©ï¼ڑو‚£è€…و¯ڈو—¥وœچ用ن¸€é¢—Mydayis胶ه›ٹ,ن»ژوœچèچ¯هگژ2-4ه°ڈو—¶ه¼€ه§‹è§پو•ˆï¼Œه¹¶ن¸”ç–—و•ˆوŒپç»و—¶é—´èƒ½é•؟è¾¾16ه°ڈو—¶م€‚
7م€پLynparza(ه¥¥و‹‰ه¸•ه°¼ç‰‡ه‰‚)
2017ه¹´8وœˆ17و—¥ï¼Œç¾ژه›½FDAه®£ه¸ƒو‰¹ه‡†éک؟و–¯هˆ©ه؛·ï¼ˆAstraZeneca)çڑ„Lynparza(olaparib)片ه‰‚(规و ¼100mgه’Œ150mg),用ن؛ژه¤چهڈ‘و€§ن¸ٹçڑ®هچµه·¢ç™Œم€پ输هچµç®،癌م€پوˆ–هژںهڈ‘و€§è…¹è†œç™Œوˆگن؛؛و‚£è€…çڑ„ç»´وŒپو²»ç–—م€‚è؟™ن؛›و‚£è€…هœ¨ه…ˆه‰چوژ¥هڈ—é“‚ç±»هŒ–ç–—هگژ,و£ه¤„ن؛ژه®Œه…¨وˆ–部هˆ†ç¼“解وœںم€‚
Lynparzaوک¯ن¸€ç§چه¤ڑèپڑن؛Œç£·é…¸è…؛è‹·و ¸ç³–èپڑهگˆé…¶ï¼ˆPARP)وٹ‘هˆ¶ه‰‚,ه®ƒهڈ¯éک»و–هڈ‚ن¸ژن؟®ه¤چهڈ—وچںDNAçڑ„é…¶م€‚è؟™و¬¾èچ¯ç‰©é€‚用ن؛ژé«که؛¦é¢„ه¤„çگ†çڑ„ن¸ژBRCAهں؛ه› ç¼؛陷相ه…³çڑ„هچµه·¢ç™Œم€‚و—©هœ¨2014ه¹´Lynparza胶ه›ٹه‰‚(50mg)ه·²è¢«FDAو‰¹ه‡†ï¼Œو¤و¬،و‰¹ه‡†çڑ„وک¯و–°ç‰‡ه‰‚ه‰‚ه‹م€‚
胶ه›ٹه‰‚وژ¨èچگçڑ„ه‰‚é‡ڈوک¯400و¯«ه…‹ï¼Œو¯ڈه¤©وœچ用ن¸¤و¬،م€‚هڈ¯è§په¯¹ن؛ژ规و ¼هڈھوœ‰50mgçڑ„胶ه›ٹه‰‚而言,و‚£è€…需è¦پو¯ڈه¤©وœچ用16粒胶ه›ٹم€‚ه¦‚وœه¢هٹ 胶ه›ٹه‰‚çڑ„规و ¼ï¼Œèƒ¶ه›ٹن½“积ه°†هڈکçگ†و›´ه¤§ï¼Œو›´ن¸چهˆ©ن؛ژو‚£è€…çڑ„وœچ用,وˆ–许وک¯ه‡؛ن؛ژè؟™ن¸ھé—®é¢کçڑ„考虑,و–°ه‰‚ه‹ç‰‡ه‰‚ه…·وœ‰هچ•ن½چهˆ¶ه‰‚çڑ„ه‰‚é‡ڈو›´ه¤§ï¼Œن½“积و›´ه°ڈçڑ„ن¼کهٹ؟م€‚
“هŒ»ç”ںن»¬هœ¨Lynparzaçڑ„ن½؟用ن¸ٹه·²ç»ڈوœ‰ن؛†ه؟«3ه¹´çڑ„ç»ڈéھŒم€‚ن»ٹه¤©وˆ‘ن»¬ه¾ˆé«که…´ه¸¦و¥è؟™ن¸€é‡چè¦پèچ¯ç‰©çڑ„و–°هˆ¶ه‰‚ه½¢ه¼ڈï¼Œé€ ç¦ڈو›´ه¹؟ه¤§çڑ„ه¦‡ه¥³ç¾¤ن½“,”éک؟و–¯هˆ©ه؛·ه…¨çگƒهŒ»èچ¯ه¼€هڈ‘و‰§è،Œه‰¯و€»è£په…¼é¦–ه¸هŒ»ه¦ه®کSean Bohenهچڑه£«è¯´éپ“ï¼ڑ“ن»ٹو—¥çڑ„و‰¹ه‡†éھŒè¯پن؛†Lynparza背هگژ10ه¤ڑه¹´çڑ„è¾›ه‹¤ç ”究م€‚è؟™و¬¾ه…¨çگƒé¦–ن¸ھPARPوٹ‘هˆ¶ه‰‚能让è‚؟çک¤ه¦ه®¶هœ¨و²»ç–—选و‹©ن¸ٹوœ‰و›´ه¤§çڑ„çپµو´»و€§م€‚هں؛ن؛ژوœ€è؟‘ن¸ژé»کو²™ن¸œï¼ˆMSD)çڑ„هگˆن½œï¼Œوˆ‘ن»¬ه°†è؟›ن¸€و¥ن¸؛و‚£è€…ه¸¦و¥و›´ه¤ڑو²»ç–—و–¹و،ˆم€‚”
8م€پAMANTADINE(金هˆڑ烷èƒ؛缓é‡ٹ胶ه›ٹ)
2017ه¹´8وœˆ24و—¥ï¼Œç¾ژه›½FDAو‰¹ه‡†ن؛†Adamas Pharmaceuticalsçڑ„و–°èچ¯Gocovri(amantadine,金هˆڑ烷èƒ؛,و›¾ç”¨هگچADS-5102)缓é‡ٹ胶ه›ٹ,用ن؛ژو²»ç–—هœ¨وژ¥هڈ—ه·¦و—‹ه¤ڑه·´و²»ç–—çڑ„ه¸•é‡‘و£®ç—…و‚£è€…çڑ„è؟گهٹ¨éڑœç¢چم€‚è؟™وک¯FDAو‰¹ه‡†çڑ„首و¬¾م€پن¹ںوک¯ه”¯ن¸€ن¸€و¬¾ç”¨ن؛ژو¤é€‚ه؛”ç—‡çڑ„èچ¯ç‰©م€‚
Gocovriوک¯ن¸€و¬¾وœ‰و½œهٹ›و”¹ه–„è؟™ن¸€çٹ¶ه†µçڑ„èچ¯ç‰©م€‚ه®ƒهگ«وœ‰é«که‰‚é‡ڈ(274 mg)çڑ„金هˆڑ烷èƒ؛,و¯ڈه¤©ç،ه‰چوœچ用ن¸€و¬،هڈ¯ن»¥وڈگن¾›وŒپç»ن¸€ه¤©çڑ„é«کو°´ه¹³é‡‘هˆڑ烷èƒ؛,用ن؛ژو²»ç–—ن¸€ه¤©ن¸ن¼ڑه‡؛çژ°çڑ„è؟گهٹ¨éڑœç¢چم€‚
“Gocovriçڑ„èژ·و‰¹وک¯ه¸•é‡‘و£®ç—…و²»ç–—领هںںçڑ„ن¸€ن¸ھé‡چه¤§è؟›ه±•ï¼Œه®ƒوک¯é¦–ن¸ھèژ·FDAو‰¹ه‡†çڑ„用ن؛ژو²»ç–—ه¸•é‡‘و£®ç—…و‚£è€…çڑ„è؟گهٹ¨éڑœç¢چçڑ„èچ¯ç‰©ï¼Œ”ه ھèگ¨و–¯ه¤§ه¦هŒ»ه¦ن¸ه؟ƒçڑ„ç¥ç»ڈه¦و•™وژˆه…¼ه ھèگ¨و–¯ه¤§ه¦ هŒ»ç–— ç³»ç»ںه¸•é‡‘و£®ç—…هچ“è¶ٹن¸ه؟ƒن¸»ن»»Rajesh Pahwaهچڑه£«è،¨ç¤؛ï¼ڑ“ه€¼ه¾—و³¨و„ڈçڑ„وک¯ï¼ŒGocovriوک¯é¦–و¬¾هœ¨ن¸´ه؛ٹ试éھŒن¸è¢«è¯پوکژهڈ¯ن»¥هگŒو—¶ه‡ڈه°‘هœ¨وœچ用ه·¦و—‹ه¤ڑه·´çڑ„ه¸•é‡‘و£®ç—…و‚£è€…çڑ„è؟گهٹ¨éڑœç¢چه’Œ‘ه…³é—’وœںçڑ„èچ¯ç‰©م€‚è؟گهٹ¨éڑœç¢چه’ŒOFFو—¶é—´çڑ„و²»ç–—هœ¨ه¸•é‡‘و£®ç—…هŒ»ç–—ç®،çگ†ن¸ن»چوک¯وœھ被و»،足çڑ„需و±‚,Gocovriçڑ„èژ·و‰¹وک¯وœè؟™ن¸ھو–¹هگ‘è؟ˆه‡؛çڑ„é‡چè¦پن¸€و¥م€‚”
ه¦‚وœè؟™ç¯‡و–‡ç« ن¾µçٹ¯ن؛†و‚¨çڑ„وƒهˆ©ï¼Œè¯·èپ”ç³»وˆ‘ن»¬م€‚
وٹ•ç¨؟هگˆن½œèپ”ç³»و–¹ه¼ڈï¼ڑ Kelly.Xiao@imsinoexpo.com 021-33392297
هœ°ه€ï¼ڑن¸ٹوµ·ه¸‚ه¾گو±‡هŒ؛虹و،¥è·¯355هڈ·هںژه¼€ه›½é™…ه¤§هژ¦7-8و¥¼ 200030