https://www.cphi.cn 2018-05-07 13:38 来源:医药经济报
首仿获批
都有优先审评资质
正大天晴2015年申报的醋酸加尼瑞克注射液终于获得首仿上市。2016年10月该品曾获得优先审评,同年11月发补;2017年4月才进入补充资料任务公示,5月底补充资料审评完成,12月才进入审批阶段。
石药集团欧意以化药新分类直接报产注射用紫杉醇(白蛋白结合型),并以“临床急需、市场短缺、首仿”为由获得优先审评。Abraxis BioScience公司已在我国上市100mg注射用紫杉醇(白蛋白结合型)。2005年1月,由Abraxis BioScience公司开发的注射用紫杉醇(白蛋白结合型)被美国FDA批准上市。2010年新基以29亿美元首付款收购Abraxis公司。新基去年7月在与百济神州的交易中,将注射用紫杉醇(白蛋白结合型)在中国的市场权益授予了百济神州。百济神州将全面接管新基在中国的商业团队,负责注射用紫杉醇(白蛋白结合型)在中国的商业推广和销售。值得注意的是,恒瑞也以首仿的理由获得优先审评,预计短期内也会获批。
武汉大安的氟比洛芬酯注射液也进入了优先审评,理由是“申请人主动撤回并改为按与原研药质量和疗效一致的标准完善后重新申报的仿制药注册申请”。武汉大安的氟比洛芬酯注射液曾是第一批自查核查的产品,2015年第255号公告撤回以后,以化学药注册分类新3类重新申报,从2017年6月30日进入CDE审评中心,同年9月4日获得优先审评,9月13日进入第九批临床自查核查名单(2017年第109号),10月10日被列入药物临床试验数据现场核查计划公告(第15号),11月29日通知生产厂家资料发补,2018年1月5日补交资料,3月12日获批上市。氟比洛芬酯注射液2017年医院样本市场已超过11亿元,首仿产品上市将争夺现有产品的市场份额。
恒瑞2013年申报的帕立骨化醇注射液和2014年申报的顺苯磺酸阿曲库铵注射液,分别以“待审评的首仿品种名单”和“同一生产线生产,已在美国上市,申请国内上市的仿制药”为由获得优先审评,并在2018年上市成功。两个产品在获得优先审评之前,申报耗时最多的是排队。由此可反映出首仿药获得优先审评的重要性。
技术转移
落地仍在进行
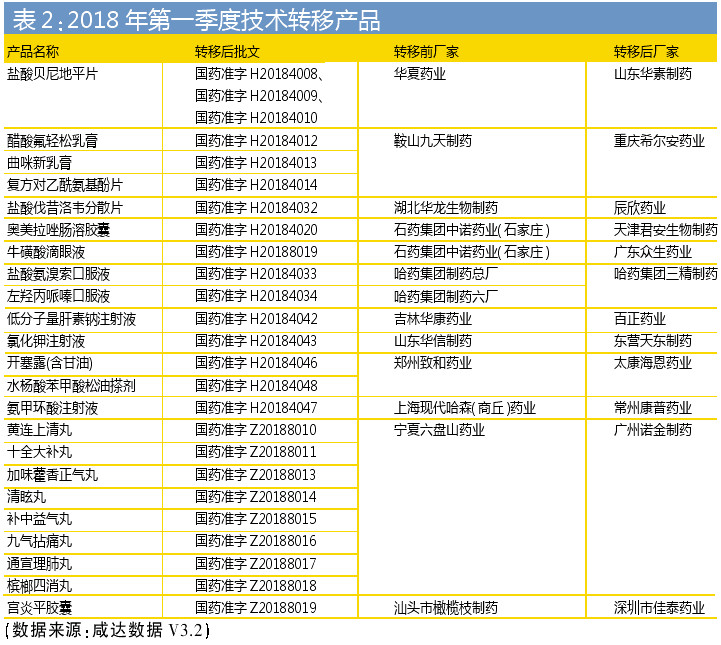
2018年第一季度,一些产品的技术转移终于落地。以盐酸贝尼地平为例。2013年1月,北京中关村四环医药开发有限责任公司之控股子公司北京华素制药股份有限公司(简称“华素制药”)与华夏药业集团有限公司(简称“华夏药业”)共同投资设立山东华素医药科技有限公司(简称“山东华素”,其中华素制药持有其80%股份,华夏药业持有其20%股份),山东华素以1亿元对价向华夏药业购买其所属的盐酸贝尼地平、盐酸贝尼地平片(商品名“元治”)、格列吡嗪分散片(商品名“元坦”)药品及包装涉及的相关药品生产技术、专利、注册商标。时隔五年,产品的技术转移才完成。
集团内的生产线整合,如哈药集团制药总厂和哈药集团制药六厂的口服液产品转移到哈药集团三精制药有限公司,这意味着哈药集团的口服液生产线有可能整合到哈药集团三精制药有限公司。
生化药的转移在2018年一季度也有案例,如吉林华康药业股份有限公司的低分子量肝素钠注射液,转移到百正药业股份有限公司。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030