12月20日,CDE官网显示,礼来pirtobrutinib片(匹妥布替尼片)的上市申请拟纳入优先审评,拟定适应症:单药适用于既往接受过布鲁顿氏酪氨酸激酶(BTK)抑制剂治疗的复发或难治性套细胞淋巴瘤(MCL)成人患者。
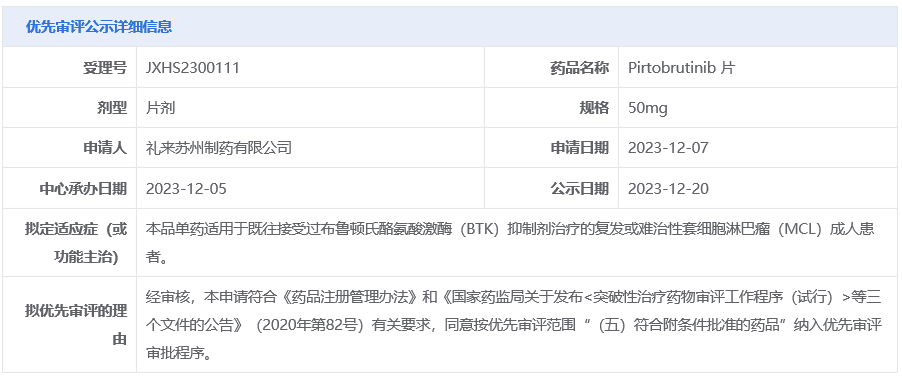
FDA批准的首 个可逆BTK抑制剂
Pirtobrutinib原研公司为Redx Pharma,是一款可口服的高选择性可逆BTK抑制剂,通过与BTK以及三磷酸腺苷结合区内水分子的广泛相互作用网络结合BTK,而不是与C481位点直接结合发挥作用,显示出克服对共价BTKI耐药性的潜力,对野生型和C481获得性耐药突变型BTK均有抑制效果。
2017年7月,Loxo Oncology(后被礼来收购)以4000万美元将pirtobrutinib收入囊中。2022年3月,信达生物以4500万美元的首付款获得了pirtobrutinib在中国的商业化权益的优先谈判权。
2023年1月,FDA加速批准 pirtobrutinib上市,用于治疗接受过BTK抑制剂在内的至少2线系统治疗的、复发或难治性细胞淋巴瘤(MCL)患者,商品名为Jaypirca。2023年12月,FDA再次加速批准pirtobrutinib新适应症,用于慢性淋巴细胞白血病或小淋巴细胞淋巴瘤(CLL/SLL)成人患者的治疗,这些患者既往接受过至少2线包括BTK抑制剂和BCL-2抑制剂在内的治疗。
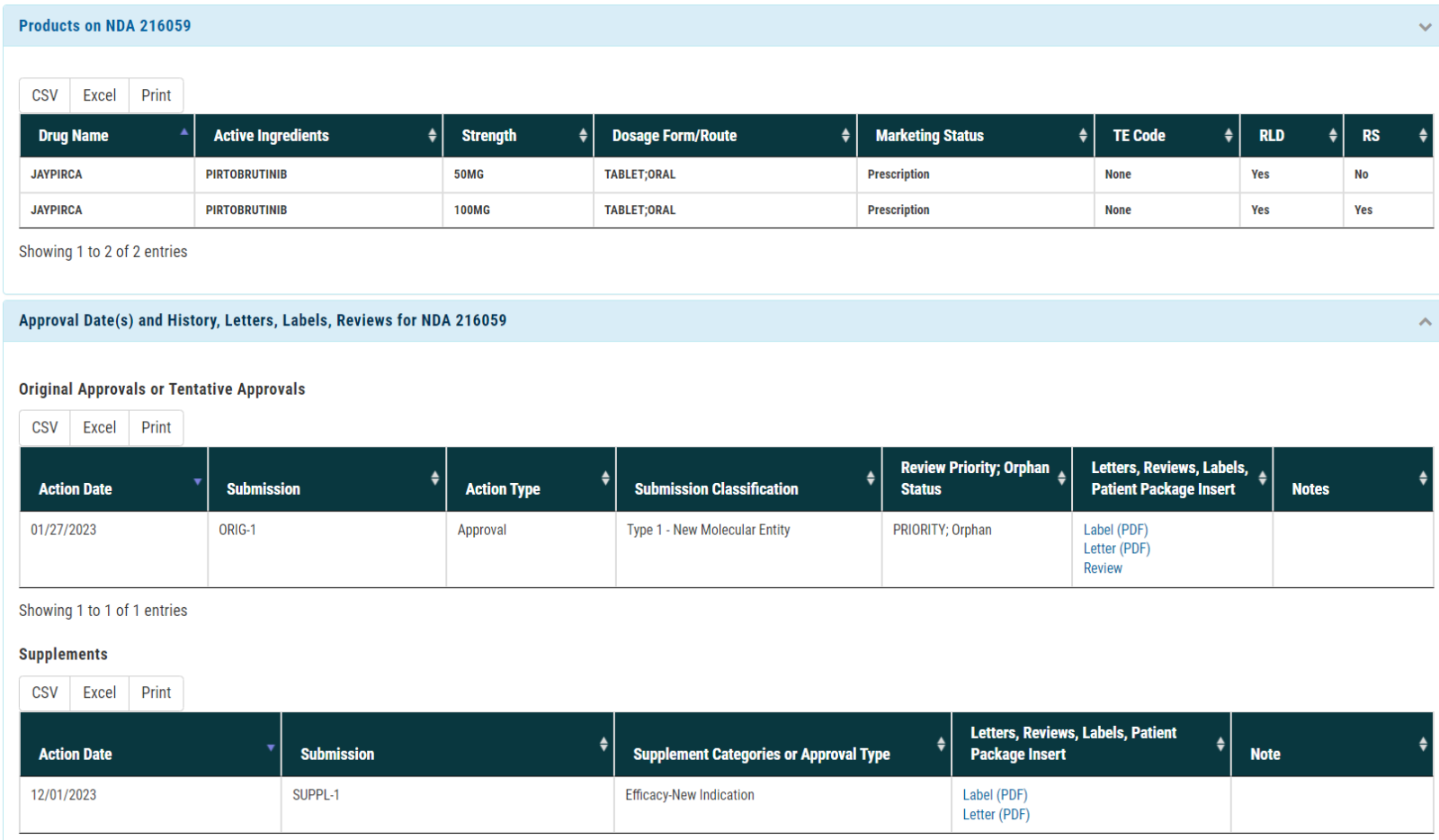
(资料来源:FDA官网)
据相关新闻报道,pirtobrutinib是获FDA批准的首 个逆转BTK抑制剂,同时也是首 个获批用以治疗已对BTK共价抑制剂产生抗性的MCL患者的BTK抑制剂。与此前批准的BTK抑制剂(如伊布替尼、阿卡替尼)相比,pirtobrutinib对BTK的选择性超过300倍。
2023年10月,礼来pirtobrutinib申报上市,均纳入优先审评。
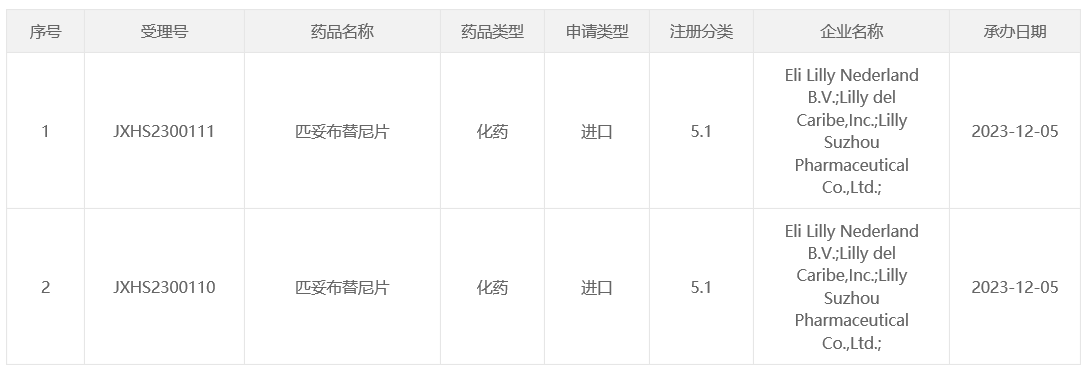
(资料来源:CDE官网)
全球共有6款BTK抑制剂上市
截至目前,全球共有6款BTK抑制剂上市,另有6款处于III期研究阶段。除Pirtobrutinib外,其他已上市BTK抑制剂均为一代BTK抑制剂,不可避免地存在C481S突变导致的获得性耐药等问题。Pirtobrutinib是FDA批准的全球首 个、且唯一一款非共价(可逆)的BTK抑制剂。
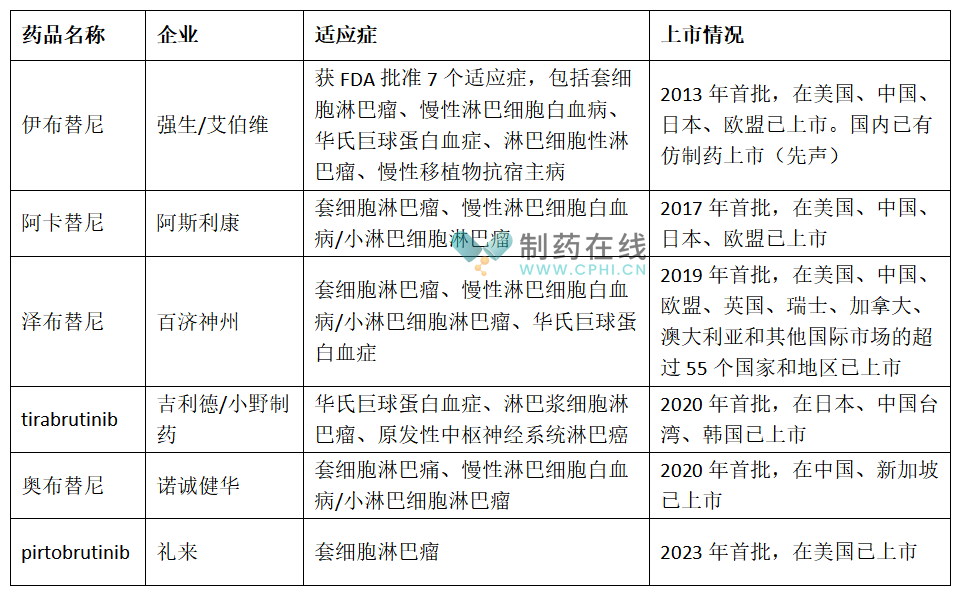
(根据公开资料整理)
据相关业内人士预测,到2025年,中国BTK市场规模将达到131亿元,2030年扩大至225亿元。但如此内卷的情况下,BTK抑制剂到底能获得多少收益,还需要时间来告知答案。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57