同样作为拥有广大患者数量的适应症,阿尔茨海默病与肥胖症的医药开发似乎处于完全不同的两条赛道之上,给人一种“君向潇湘我向秦”的感觉。减肥药市场一片百舸争流的大干快上景象,不仅已经上市的Wegovy和Zepbound令诺和诺德和礼来两大制药商领略到了“山顶千门次第开”的感受,为数众多的追随者也在“一波才动万波随”地争取跻身这个庞大的市场。而另一边,以阿尔茨海默病为代表的中枢神经系统疾病,尽管面对着同样庞大的商业机会,制药商们却一直在“多歧路,今安在”的道路上龃龉其中。2025年,阿尔茨海默病疗法开发能像肥胖症药物一样迎来“花开堪折直须折”的自由境界吗?
1.阿尔茨海默病疗法开发的2024困顿
阿尔茨海默病与肥胖症疗法开发的一个相似点,就是这两种适应症的致病机理人们仍然没有完全搞清楚,在开发过程中都给人一种摸着石头过河的感觉。索性肥胖症疗法的开发得益于二型糖尿病GLP-1疗法开发过程中的“意外”发现,实现了截弯取直的快速发展。同样作为病理复杂的适应症,阿尔茨海默病不仅在生物标志物方面还存在争议,还面临着如何实现脑部递送的巨大的挑战。除此之外,以Aduhelm,Leqembi和Kisunla为代表的靶向脑部Aβ (β-amyloid,β淀粉样蛋白)的抗体药物,还存在着ARIA (Amyloid-Related Imaging Abnormalities,淀粉样蛋白相关的成像异常)的黑框警告,包括脑水肿和脑出血,这为阿尔茨海默病疗法的开发增加了极大的挑战。反观GLP-1药物,副作用大多数恶心和呕吐这样相对轻微的表现,在安全性方面的门槛要低很多。
2024年,阿尔海默病疗法开发遭遇的挫折几乎就是减肥药成功的镜相对照。
2024年1月底,当年顶着巨大争议上市的首 款抗Aβ抗体阿尔茨海默病药物Aduhelm (aducanumab) 被其开发商渤健宣布撤市,而此前渤健已经撤回了Aduhelm向EMA递交的上市申请。Aduhelm“其兴也勃焉,其亡也忽焉”的故事为制药行业留下了众多的话题和思考。
2021年6月,FDA在先前的专家咨询委员会会议压倒性的1票支持、8票反对,2票弃权的情况下,仍然一意孤行地批准了Aduhelm的上市申请(专家咨询委员会投票结果对于FDA最终决定不具备约束性影响)。顶着巨大争议上市的Aduhelm的商业化效果并不理想,不仅过高的标价成为了业界诟病的问题(渤健最初将Aduhelm的年度治疗成本定价为56000美元),而且在有效性和安全性方面的争议已然不绝于耳,最终渤健做出了将Aduhelm撤市的决定,转而重点运作另一款获得FDA批准的阿尔茨海默病抗Aβ抗体疗法Leqembi(lecanemab)上。渤健强调,撤市的决定并不在于Aduhelm的安全性和有效性,而是出于战略考量,有一点“此天意,非战之罪”的姿态。
Aduhelm的“尔曹身与名俱灭”,似乎是很多兴勃亡忽的中枢神经系统疾病疗法殊途同归的命运。
罗氏在2024年10月宣布了终止与UCB共同开发阿尔茨海默病候选药物bepranemab的决定,这也是罗氏2024年第三次放弃阿尔茨海默病项目。早在1月,罗氏就将两项合作开发的阿尔茨海默病资产归还给了AC Immune。
罗氏与UCB于2020年达成的合作原本包括1.2亿美元的预付款和高达20亿美元的潜在里程碑付款。这项合作的关注点,在于靶向tau蛋白的bepranemab。Tau蛋白同β-淀粉样蛋白一样被视为阿尔茨海默病的生物标志物。tau蛋白的水平和磷酸化状态常被用作生物标志物。Tau蛋白不仅是阿尔茨海默病的关键生物标志物,也是开发新治疗方法的潜在靶点,其靶向药物的命运在一定程度也昭示着目前阿尔茨海默病疗法开发能够走出Aβ的圭臬樊笼。然而bepranemab的IIa期临床试验结果却令罗氏兴致阑珊,最终决定将该药物的开发权交还给UCB。
值得注意的是,虽然罗氏终止了与UCB的合作, 但他们仍对tau靶向疗法开发保持了浓厚兴趣。罗氏仍在试图针对 tau 蛋白开发阿尔茨海默病疗法,包括与 Sangamo Therapeutics Inc. 建立的临床前合作,两家公司于 2024年8 月签署了 一项价值5000 万美元预付款的协议。 在罗氏的管线中,有一款“嫡出”的抗tau蛋白抗体资产trontinemab。它采用罗氏的“脑穿梭(Brainshuttle)”技术,以蛋白质之躯跨越血脑屏障,靶向并抑制β淀粉样蛋白。这种技术允许大分子在不触发对周围细胞的免疫反应的情况下穿过血脑屏障。
2.阿尔茨海默病疗法开发,病入新年感物华
虽然阿尔茨海默病疗法在过往岁月更多以“命运多舛”的形象示人,但在这个领域仍然给众多开发者“桃花又是一年春”的希冀,包括渤健、卫材、礼来、罗氏和诺和诺德在内的制药公司依然加大了这个领域的投资力度,任何临床试验的成功或药物批准的突破都可能对股价产生重大影响。投资者高度重视以阿尔茨海默病为代表的中枢神经系统疾病的潜在商业价值。根据Bloomberg预测,到 2030 年阿尔茨海默病的市场规模可能达到 130 亿美元。
渤健和卫材的上市药物Leqembi 目前的递送方式为静脉输注,但他们也在开发一种能够在家给药的Leqembi皮下注射版本。渤健和卫材已于2024年11月向FDA递交了这款Leqembi的BLA申请。皮下自动注射器用于每周维持给药,此前已获得 FDA 快速通道资格。
这款皮下注射版本的Leqembi如果获得 FDA 批准,患者可以在家中或者医疗机构中完成给药,注射过程只需要15秒钟。相比之下,Leqembi的静脉输注制剂每两周给药一次,每次的注射时间大约在1小时左右。根据卫材公布的数据,皮下注射Leqembi治疗产生的淀粉样斑块清除率高于每两周静脉注射。Leqembi皮下注射版本是否能在2025年获得FDA的批准,这成为了阿尔茨海默病开发领域和投资者关注的焦点之一。
礼来公司的 抗Aβ抗体药物Kisunla(donanemab) 2024 年 7 月获得 FDA 批准,Kisunla未来是否将与Leqembi颉颃前行还是脱颖而出,也是阿尔茨海默病疗法投资者关注的重点。
除了Kisunla之外,礼来的管线中还有一款阿尔茨海默病资产remternetug,可以通过静脉或皮下的途径给药。Remternetug是一款抗焦谷氨酸Aβ抗体药物正处于临床III期阶段。据Bloomberg称,Remternetug的III期试验将评估其淀粉样斑块清除率和安全性,以判断其在有效性上是否胜过已上市的donanemab。Remternetug 的试验结果可能会在今年年底或 2026 年初公布。
罗氏在做出了终止了与USB共同开发bepranemab的合作之后,并没有在开发阿尔茨海默病疗法的道路上选择“行至水穷处,坐看云起时”的姿态,而是独自开发了他们自己的trontinemab。值得注意的是,罗氏在开发trontinemab的项目中使用了可穿越血脑屏障的技术平台Brainshuttle,如果成功,将为中枢神经系统疾病疗法的开发引入革命性的影响。巴克莱银行认为罗氏针对trontinemab的开发不会半途而废,而将继续进行中后期的研究。之所以这么说,是因为trontinemab本质上是 gantenerumab 的更新版本,gantenerumab 是罗氏之前对阿尔茨海默病的重大赌注,但最终未能减缓认知能力下降。
尽管罗氏从bepranemab的合作项目中抽身而出,但开发它的比利时制药巨头UCB预计仍将在bepranemab的开发道路中继续上下求索。在去年的一项II期临床研究中,bepranemab未能达到主要临床终点,但的确减缓了认知能力的下降和生物标志物tau蛋白在大脑中的积累速度。一些分析师指出,bepranemab 具有相对较强的安全性数据,应该具备与其它疗法组成联合疗法治疗阿尔茨海默病的潜力。
3.GLP-1药物能否“达则兼济天下”?
阿尔茨海默病未来疗法开发的一个重要看点,在于病理机制的深入研究是否能够突破目前囿于Aβ蛋白清除的樊笼。除了Aβ蛋白之外,tau蛋白也是一个重要的生物标志物,但也有很多公司在开发道路上选择了与这两个“部分存疑”的生物标志物不同的途径。进行GLP-1药物开发的公司,包括诺和诺德在内的几家制药商已经押注于此类药物治疗阿尔茨海默症的潜力。例如丹麦公司Kariya 正在开发 KP405,这是一种GLP-1/GIP双受体共激动剂,与礼来的tirzepatide师出同门。KP405最初用于治疗帕金森病,未来可能针对阿尔茨海默病进行研究。KP405的特别之处在于,它并没有使用semaglutide和tizepatide的脂化技术,而是在药物结构中添加了细胞膜受体识别的 TAT 序列,这使得药物分子可能穿越血脑屏障而进入大脑病灶。
诺和诺德在2型糖尿病和肥胖症上大获成功的GLP-1药物semaglutide也在针对阿尔茨海默病进行研究。去年的一项研究表明,服用semaglutide的患者被诊断出患有阿尔茨海默病的风险显著降低。诺和诺德目前正在测试semaglutide是否能使早期阿尔茨海默病患者受益,预计将从两项大型 III 期试验 EVOKE 和 EVOKE Plus 中读取结果,测试semaglutide对阿尔茨海默病患者的作用。预计EVOKE将于 2025 年 9 月公布顶线数据,而EVOKE Plus则将在2026年10月读数。
使用 GLP-1 治疗阿尔茨海默病的想法并非空穴来风。人们一直对用于治疗糖尿病和针对代谢疾病和内分泌疾病途径的药物是否会对阿尔茨海默病产生影响感兴趣。虽然关于阿尔茨海默病的真正病因存在很多争论,糖尿病和肥胖症与阿尔茨海默病之间可能存在交集。事实上,有几项研究表明胰岛素抵抗与阿尔茨海默病之间存在联系。导致有些人将阿尔茨海默病称为“3 型糖尿病”。多项观察性研究和荟萃分析也建立起了 2 型糖尿病与阿尔茨海默病的风险增加。
随着年龄的增长,整个身体的胰岛素抵抗都会增加,这意味着细胞无法吸收足够的葡萄糖。当葡萄糖水平不理想而且高度活跃的神经元无法获得足够的能量时,它们就会出现功能障碍并最终慢性死亡。这种内在关联是具有一定道理的。如果胰岛素抵抗确实是阿尔茨海默病的一个诱因,那么 GLP-1 可能有助于延缓这种疾病,因为它通过刺激胰岛素分泌和减缓胰高血糖素释放来发挥作用。
此前GLP-1药物利拉鲁肽(liraglutide)的一项II 期试验的结果支持了这样的假设。那项研究在英国多个地点随机对 204 名受试者进行安慰剂或利拉鲁肽治疗。结果发现,在一年的治疗中,利拉鲁肽组的认知功能下降速度比安慰剂组慢 18%。研究人员指出,脑容量损失速度较慢表明利拉鲁肽可以保护大脑,就像他汀类药物可以保护心脏一样。利拉鲁肽可以减少脑部炎症、降低胰岛素抵抗、改善神经细胞通讯并限制淀粉样蛋白β和 tau 的危害。
尽管某些研究出现了积极的迹象,但专家们一致认为,GLP-1 仍有很长的路要走,才能证明其在阿尔茨海默病治疗中的价值,这需要在随机对照试验中对大量患者进行分析,这其实是一项非常艰巨的工作。
4.直捣黄龙,药物递送的突破
相对于稍显踯躅的病理研究,阿尔茨海默病疗法递送领域的开发已经取得了明显的突破,最主要的表现在于新一代的药物分子开始注重直接穿越血脑屏障的能力。例如前面提到的罗氏开发的trontinemab,就利用了最新技术平台Brainshuttle技术。Brainshuttle是凭借与TfR(Transferrin Receptor转铁蛋白受体)的作用实现血脑屏障的跨越。Trontinemab将抗TfR抗体模块与阿尔茨海默病抗体Gantenerumab(罗氏上一代的阿尔茨海默病抗体候选药)融合,与血脑屏障上皮细胞上的TfR受体结合。这种结合产生内体隔室,内体隔室穿过细胞质并通过转胞吞作用进入大脑(图1)。因此从本质上说,trontinemab是一款2 + 1 双特异性单体,可双价结合 Aβ蛋白,单价结合人 TfR1。
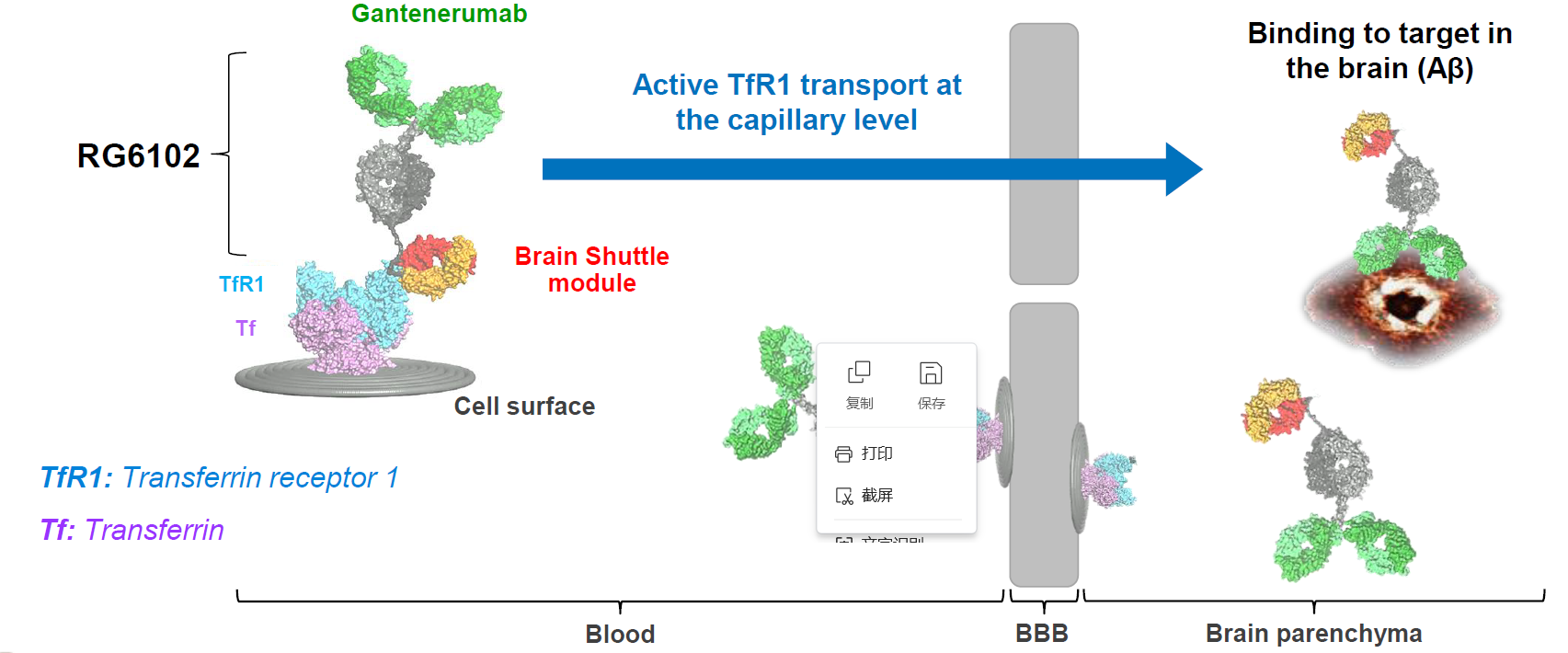
图1. Brainshuttle技术支持的trontinemab穿越血脑屏障机制。(图片来源:Neuron)
艾伯维通过14亿美元收购Aliada Therapeutics获得的关键资产阿尔茨海默病候选药物ALIA-1758也利用了类似的递送机制。ALIA-1758是一款抗β淀粉样蛋白(焦谷氨酸β淀粉样蛋白(3pE-Aβ))抗体药物。ALIA-1758通过专有技术Modular Delivery (MODEL) 平台设计,可以穿越血脑屏障而不触发神经毒性。
MODEL平台将抗TfR抗体模块与阿尔茨海默病抗体融合,与血脑屏障上皮细胞上的TfR受体结合。这种结合产生内体隔室,内体隔室穿过细胞质并通过转胞吞作用进入大脑。MODEL平台不仅可以携带抗体,也可以携带寡核苷酸、多肽、酶和其它蛋白,通过结合TfR或CD98的方式跨越血脑屏障。
礼来与卫材最近也在利用各自的专有技术开发可穿越血脑屏障的中枢神经系统疾病疗法。礼来使用的是QinoTrans平台,通过工程化蛋白结合血脑屏障上的受体,以此穿越该屏障。卫材去年与瑞典生物技术公司BioArctic达成协议,获得了后者的BioArctic BrainTransporter技术的使用权限,开发通过与血脑屏障受体结合而抵达大脑的阿尔茨海默病药物。
5.面壁十年图破壁
阿尔茨海默病疗法的开发虽然面临巨大挑战,但与当前方兴未艾的减肥药领域有相似之处。减肥药市场在过去几年中因肥胖问题日益严重而加速发展,相关药物的需求不断攀升,促使制药公司加大研发力度,推出了如GLP-1受体激动剂等新型疗法,取得了显著成果。同样,阿尔茨海默病的全球影响力随着人口老龄化迅速扩大,使得开发有效疗法的需求愈发迫切。然而,阿尔茨海默病疗法的开发复杂性远超减肥药,因为其涉及多种致病机制,且有效治疗手段尚不成熟。
尽管如此,正如减肥药领域通过技术突破和市场推动取得了进展,阿尔茨海默病疗法也有望迎来关键性突破,推动其开发进入新的高度,为患者带来实际疗效。精准医学的发展以及生物标志物的应用,将使早期诊断和个性化治疗成为可能,大幅提高治疗的有效性。同时,全球老龄化加剧意味着市场对阿尔茨海默病疗法的需求日益增长,类似减肥药市场的繁荣景象或将在阿尔茨海默病领域重现。尽管开发过程中仍存在诸多科学和临床障碍,但通过创新技术、跨学科合作以及更有效的临床研究设计,未来阿尔茨海默病疗法有望实现重大突破,实现面壁十年图破壁的真正飞跃。
Ref.
Constantino, A. K. Biogen drops controversial Alzheimer’s drug Aduhelm to focus on Leqembi, experimental treatments. CNBC. 31. 01. 2024.
Merrill, J. Biogen Closes The Book On The Aduhelm Saga. Pink Sheet. 31. 01. 2024.
Armstrong, A. Roche Trims Another Alzheimer’s Prospect, Ending UCB Collabortion. Biospace. 22. 10. 2024.
Jackson, M. UCB Assessing Bepranemab’s Future After Roche/Genentech Ends Partnership. Scrip. 22. 10. 2024.
Kresge, N. et al. Roche CEO Is Optimistic on Coming Alzheimer’s Trial Results. Bloomberg. 23. 10. 2024.
Eisai Completes Rolling Submission to US FDA for LEQEMBI® (lecanemab-irmb) Biologics License Application for Subcutaneous Maintenance Dosing for the Treatment of Early Alzheimer’s Disease Under the Fast Track Status. Eisai Press Release. 01. 11. 2024.
McKenzie, H. Evidence Mounts for Potential of GLP-1s in Alzheimer’s Disease.
Taylor, N. P. AbbVie inks $1.4B Aliada buyout, landing ex-J&J Alzheimer's drug to leap the blood-brain barrier. Fierce Biotech. 28. 10. 2024.
Alpert, B. AbbVie’s Deal for Alzheimer’s Antibody Raises Curtain for Roche News on Wednesday. Barron’s. 29. 10. 2024.
Qinotto and Lilly Enter Research Collaboration and License Agreement. Globe Newswire. 08. 10. 2024.



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57