https://www.cphi.cn 2018-07-26 16:22 来源:健康界 作者:杨瑞静
过去,国内缺医少药,本着让民众有药可吃的原则,药品审评标准定的很低,上市的仿制药质量参差不齐。中国医药质量管理协会副会长孙新生曾表示,每一次仿制都带来20%的误差累积,最终越仿越低,与原研药药效相去越远。
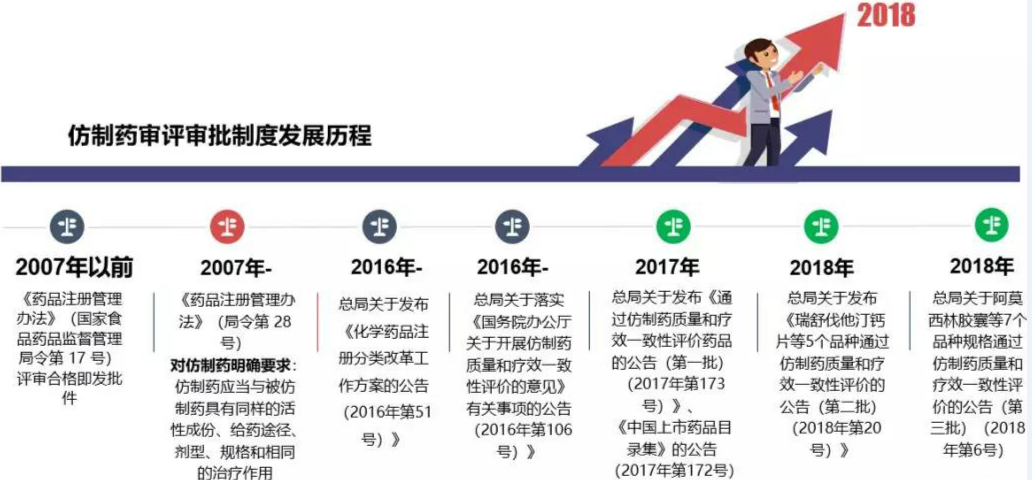
此时,国家提出了开展仿制药一致性评价工作。即,对已经批准上市的仿制药,按与原研药品质量和疗效一致的原则,分期分批进行质量一致性评价,仿制药需在质量与药效上达到与原研药一致的水平。
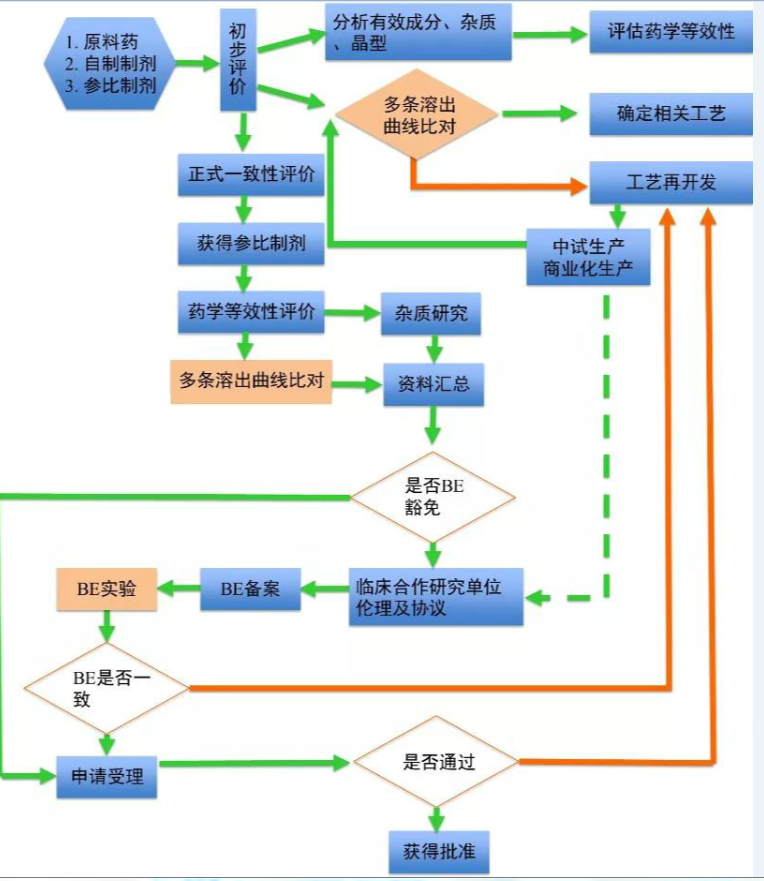
一致性评价流程
能通过一致性评价而生产相同高技术含量和高质量的药品并不容易,这对企业的技术能力和资金实力提出了较高的要求,只有行业的龙头企业才能够同时具备以上的条件。甚至,一些著名药厂的仿制药,也没有通过中国的一致性评价。
仿制药的2018
随着一致性评价推进,中国仿制药行业的格局也将出现重大变化。
2016年,国务院办公厅发布了《关于开展仿制药质量和疗效一致性评价的意见》(下称意见),为国产仿制药完成一致性评价规定了时限。根据要求,2007年10月之前批准上市的国家基本药物目录(2012版)中化学药品仿制药的口服固体制剂品种,必须在2018年底完成一致性评价,不通过则直接注销药品批准文号。
根据药监局审批中心最新公布的信息,目前共有四批共41个品规通过仿制药一致性评价。不过,在289个基药目录的仅有11个。随着2018年大限将至,这也意味着或还有上万个批文会在今年年底面临淘汰风险。
除了面临被淘汰的压力,即使药品过了一致性评价,在临床使用上,决定权依然在临床医生。就临床应用来说,有医生直接表示,并不信任仿制药的疗效。上升到医院层面,取消药品加成后,用原研药和仿制药没有盈利上的差别,医院自然倾向选择更放心的药。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030