Part 1
国内仿制药研发批准动态
01
新注册分类品种首家批准上市情况
根据药渡数据调研,本次统计周期(2024.02.24-03.01)新增3个新注册分类首家过评受理号,涉及2个品种,包括1个胶囊剂,1个滴眼剂。与上次统计周期相比,本周增加1个新注册分类首家过评品种。
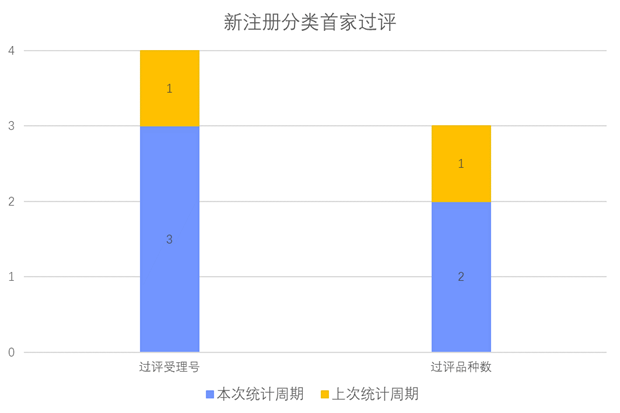
新注册分类品种过评情况
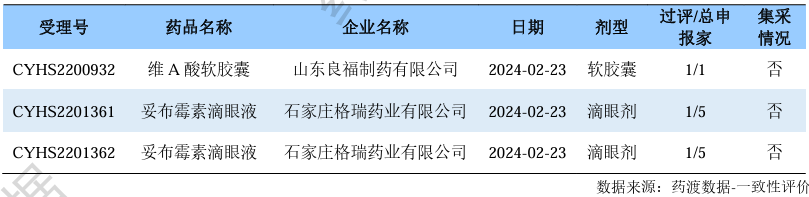
妥布霉素滴眼液
妥布霉素是诺华原研的一种氨基糖苷类抗生素,属于广谱抗生素,抗菌谱较广,对铜绿假单胞菌、革兰阳性菌、革兰阴性菌等均有效。妥布霉素滴眼液临床上主要用于因敏感细菌感染所致的外眼以及附属器疾病,如泪囊炎、睑缘炎、结膜炎、角膜炎、葡萄膜炎以及眼部手术后的预防性感染。
1980年诺华开发妥布霉素滴眼液首次获FDA批准上市,商品名托百士(Tobrex)。1999年,南京恒生制药的妥布霉素滴眼液首次获NMPA批准在在国内上市。
药渡数据-仿制药库调研,包括原研企业诺华在内,国内共有40家企业拥有妥布霉素滴眼液的生产批文。

药渡数据库-中国销量库统计数据显示,近年来,全国医院、药店等销售终端眼科抗感染药物销售额稳步增长,多家企业布局该眼科药物领域。
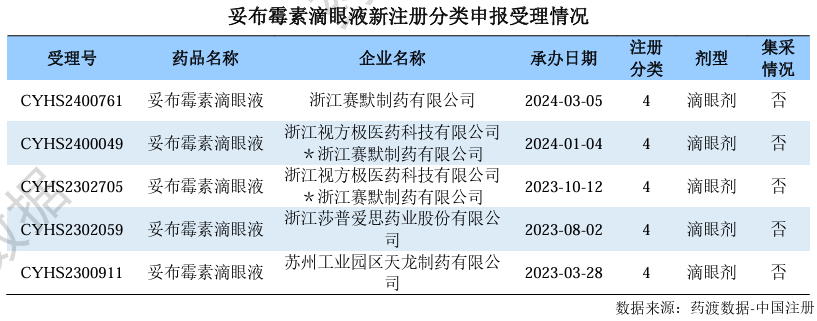
药渡数据-中国注册库信息显示,国内共有8家企业递交了妥布霉素滴眼液的新4类报产申请。其中,天津金耀药业的报产申请于2月“沉沙”,石家庄格瑞药业的报产申请于本周视同过评,成为妥布霉素滴眼液的“首家”过评企业。其他6家企业的报产申请已受理或在审评审批中。
02
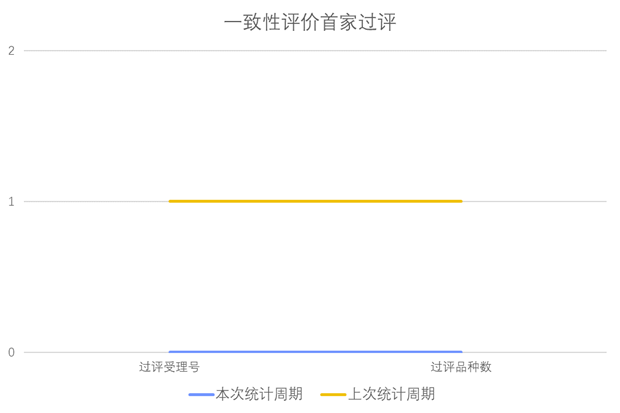
一致性评价品种首家批准上市情况
根据药渡数据调研,本次统计周期(2024.02.24-03.01)无新增一致性评价首家过评受理号。与上次统计周期相比,本次减少1个一致性评价首家过评品种。
03
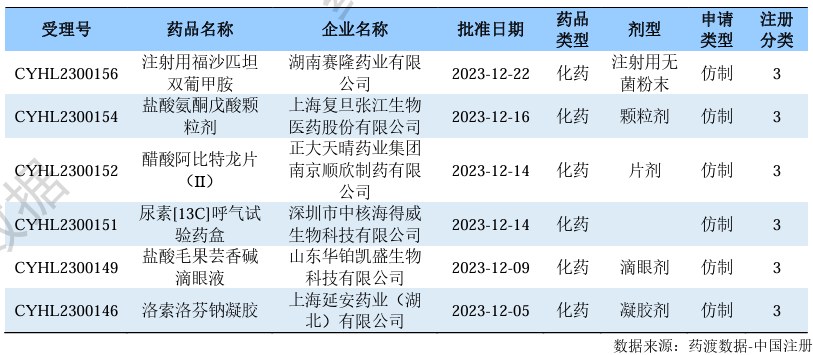
新注册分类品种批准上市情况
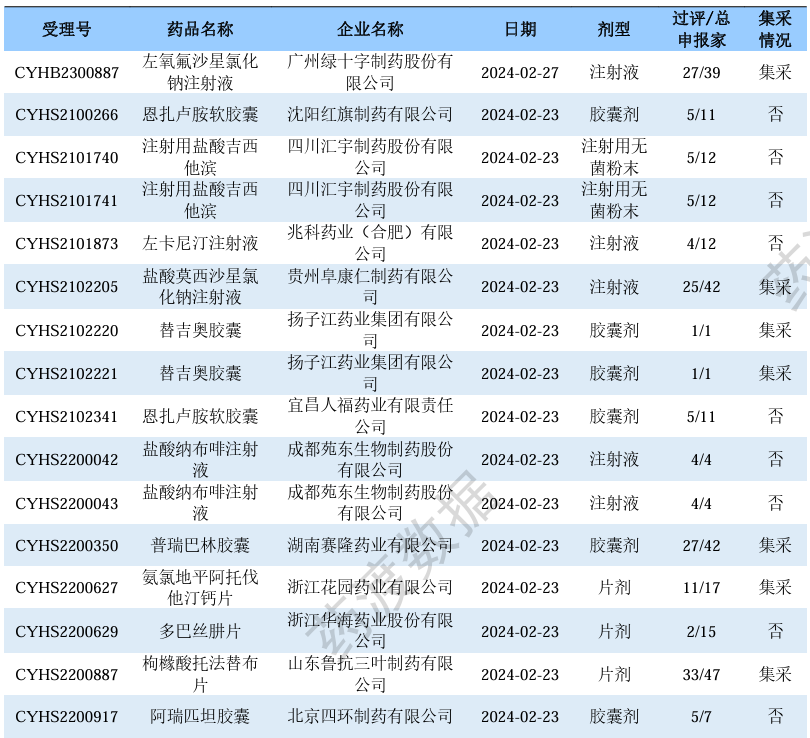
根据药渡数据调研,本次统计周期(2024.02.24-03.01)新注册分类新增40个过评受理号,涉及32个品种,包含1个滴眼剂,8个胶囊剂,1个颗粒剂,1个口服溶液剂,7个片剂,1个吸入溶液剂,13个注射剂。与上次统计周期相比,本次增加4个新注册分类过评品种。
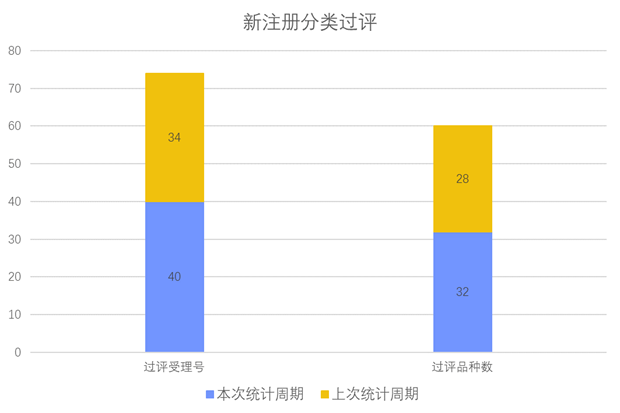
新注册分类品种过评情况(部分)
04
一致性评价品种批准上市情况
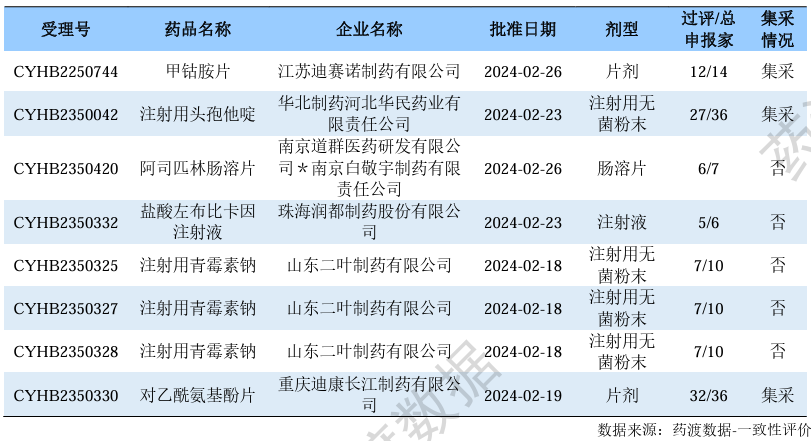
根据药渡数据调研,本次统计周期(2024.02.24-03.01)一致性评价新增8个过评受理号,涉及6个品种,包括3个注射剂,3个片剂。与上次统计周期相比,本次减少8个一致性评价过评品种。
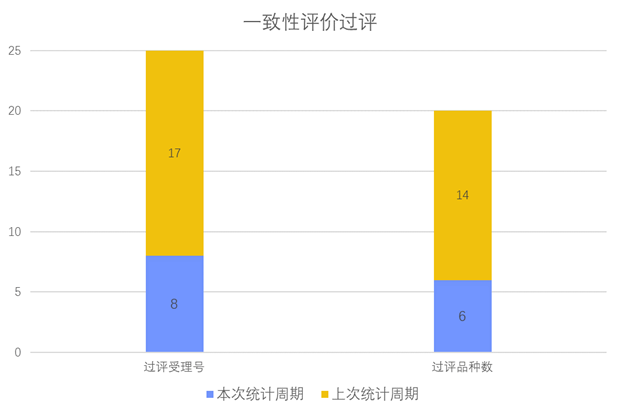
一致性评价品种过评情况
05
仿制药品种批准临床情况
Part 2
国内仿制药研发批准动态
01
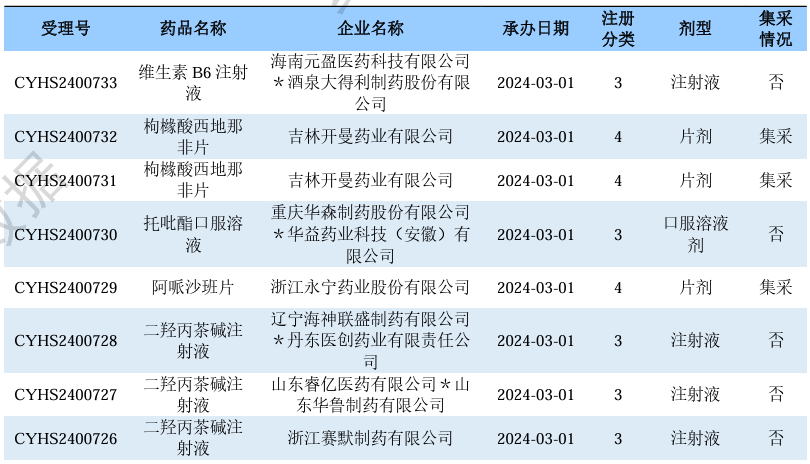
新注册分类品种申报上市情况
根据药渡数据调研,本次统计周期(2024.02.24-03.01)新注册分类数据新增72个新报受理号,涉及57个品种,包括1个搽剂,2个滴眼剂,2个干混悬剂,3个胶囊剂,3个颗粒剂,5个口服溶液剂,22个片剂,1个软膏剂,1个贴剂,17个注射剂。与上次统计周期相比,本次减少21个新注册分类申报品种。
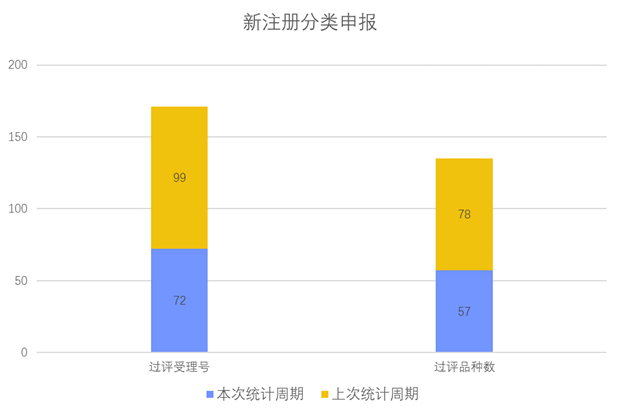
新注册分类品种申报受理情况(部分)
02
一致性评价品种申报上市情况
根据药渡数据调研,本次统计周期(2024.02.24-0.01)一致性评价数据新增19个新报受理号,涉及15个品种,包括2个干混悬剂,2个片剂,11个注射剂。与上次统计周期相比,本次减少1个一致性评价申报品种。
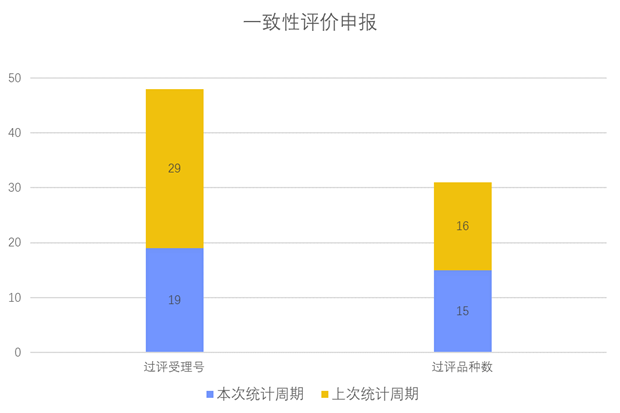
一致性评价申报受理情况(部分)
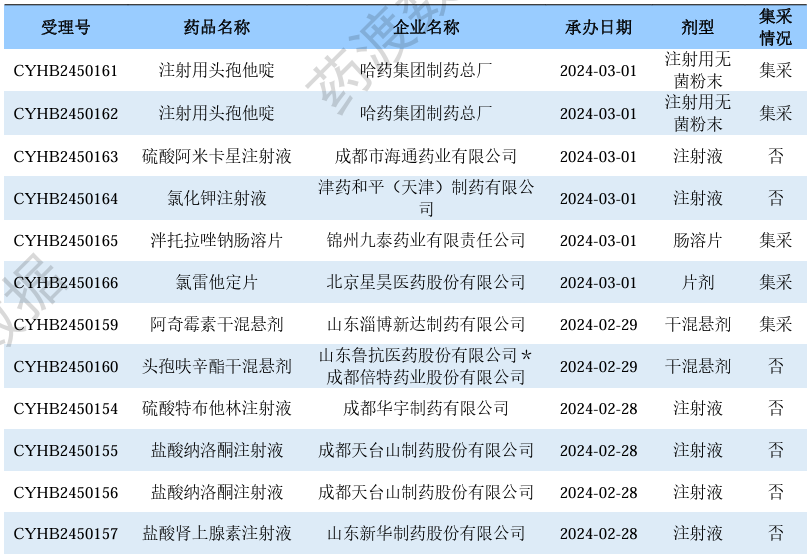
03
仿制药补充申请情况
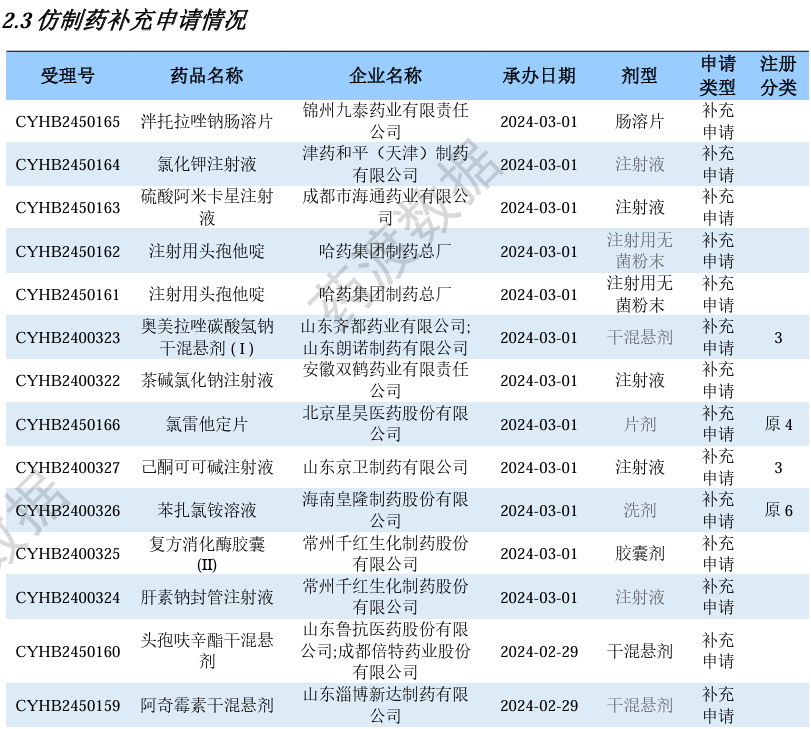
04
仿制药申报上市专利声明信息汇总
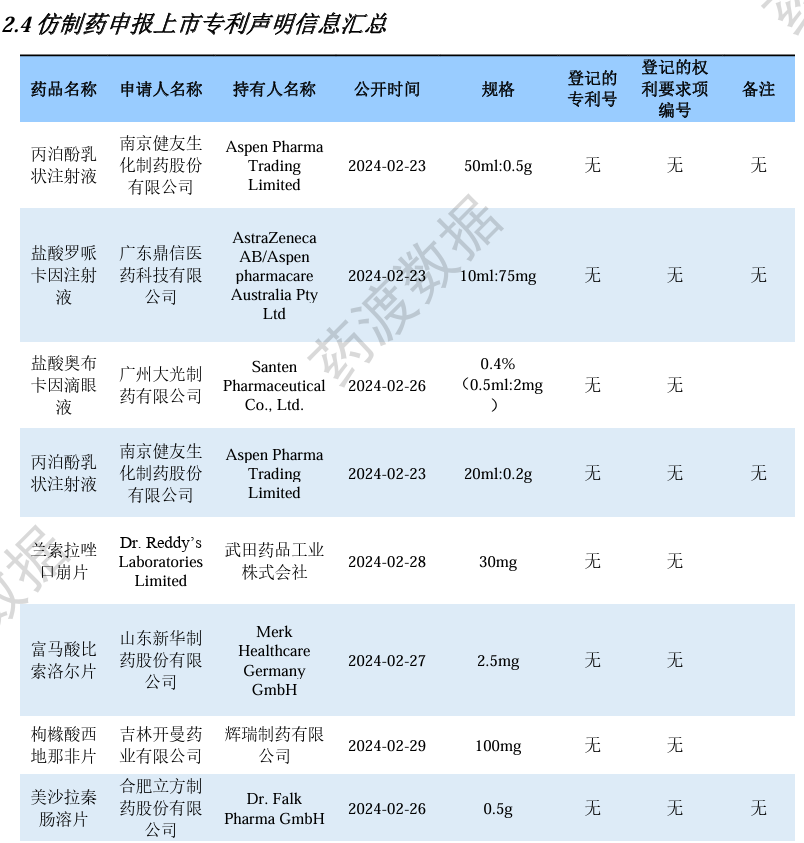
Part 3
国内仿制药研发领域热点聚焦
01
国内仿制药研发领域政策法规相关动态
关于更新电子申报资料制作软件的通知
为保障药品注册申请电子申报工作的稳步推进,更好地服务申请人,提升电子申报资料质量,我中心根据近期收集的业界反馈意见以及电子申报资料使用中存在的问题,经充分评估后,对2023年12月11日发布的电子申报资料制作软件进行了优化更新,以进一步提高电子申报资料制作软件的易用性,提升用户体验。
本次更新内容主要包括增加文件数量统计和同名文件提示功能,完善临床试验数据库子文件夹创建功能,优化扩展文件夹命名规则,以及结合实际业务需要,细化软件中电子申报资料类型和对应的文档结构。相关电子申报资料制作软件及配套文档说明请查看原文。
02
国内仿制药研发领域热点新闻
海正药业:浙江海正药业股份有限公司关于全资子公司磷酸奥司他韦原料药获得《化学原料药上市申请批准通知书》的公告
2024年2月29日,浙江海正药业股份有限公司发布公告称,公司全资子公司海正药业南通有限公司于2024年2月28日收到国家药品监督管理局核准签发的磷酸奥司他韦原料药的《化学原料药上市申请批准通知书》。现就相关情况公告如下:
一、该药品的基本情况
化学原料药名称:磷酸奥司他韦
登记号:Y20220000102
通知书编号:2024YS00159
化学原料药注册标准编号:YBY61842024
包装规格:3kg/袋 申请事项:境内生产化学原料药上市申请
生产企业:海正药业南通有限公司
审批结论:根据《中华人民共和国药品管理法》,经审查,本品符合仿制药审批的有关规定,批准生产本品。
二、该药品的相关情况
磷酸奥司他韦是其活性代谢产物(奥司他韦羧酸盐)的前体药物,奥司他韦羧酸盐是选择性的流感病毒神经氨酸酶抑制剂,用于成人和1岁及1岁以上儿童的甲型和乙型流感治疗,以及成人和13岁及13岁以上青少年的甲型和乙型流感的预防。其原研厂家为罗氏。目前,磷酸奥司他韦原料药国内主要生产厂商有湖南欧亚药业有限公司、杭州福斯特药业有限公司等。
据统计,磷酸奥司他韦原料药2022年全球销售量约为41,116.11公斤,其中国内销售量约为14,088.78公斤;2023年1-9月全球销售量约为41,598.09公斤,其中国内销售量约为 22,930.91 公斤(数据来源于IQVIA 数据库)。
2022年6月13日,国家药监局受理了海正南通公司递交的磷酸奥司他韦原 料药的注册申请。2024年2月28日,海正南通公司磷酸奥司他韦原料药通过国家药品监督管理局药品审评中心技术审评,在CDE原辅包登记信息平台上显示状态为“A”。截至目前,公司在该药品研发项目上已投入约 1,411 万元人民币。
三、对上市公司影响及风险提示
本次海正南通公司磷酸奥司他韦原料药通过 CDE 技术审评,证明该原料药已符合国家相关药品审批技术标准,可进行生产销售,有利于进一步丰富公司的产品线,提升市场竞争力。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57