https://www.cphi.cn 2019-08-29 14:34 来源:CPhI制药在线 作者:Dopine
喜讯,罗氏的TRK抑制剂Rozlytrek(entrectinib)近日喜获FDA批准用于治疗神经营养性原肌球蛋白受体激酶(NTRK)融合阳性,局部晚期或转移性实体肿瘤的成人和儿童患者,以及ROS1阳性、转移性非小细胞肺癌(NSCLC)患者。这意味Rozlytrek成为FDA批准的第二款TRK抑制剂,以及继Merck的Keytruda、Loxo Oncology和Bayer的Vitrakvi之后FDA批准的第三款不限癌种疗法。
关于entrectinib
entrectinib是一种新型、口服有效的、具有中枢神经系统(CNS)活性的酪氨酸激酶抑制剂,靶向治疗携带NTRK1/2/3(编码TRKA/TRKB/TRKC)、ROS1和ALK融合基因突变的实体瘤患者。此外,entrectinib可以通过血脑屏障,临床上已被证明对原发性和转移性中枢神经系统(CNS)疾病具有疗效,并且还没有不良的脱靶活性。
entrectinib最初由美国聚焦肿瘤领域精准治疗药物的Ignyta 公司研发,后于2017年12月被罗氏以每股27美元、总价17亿美元收购。2017年5月entrectinib被FDA授予治疗既往已接受治疗但病情进展或没有可接受标准疗法的NTRK融合基因阳性、局部晚期或转移性实体瘤儿科患者和成人患者的突破性药物资格(BTD),同年11月被EMA授予上述相同患者群体的优先药物资格(PRIME)。今年6月份率先在日本获批用于治疗神经营养性酪氨酸受体激酶(NTRK)基因融合阳性的晚期复发实体瘤成人和儿童患者,且用于治疗ROS1基因融合阳性的局部晚期或转移性NSCLC的适应症正在接受日本MHLW的审评。
此次entrectinib获批是基于多项临床试验的结果。这些试验数据的汇总分析显示:entrectinib对10多种不同类型的NTRK融合阳性实体瘤患者均有治疗效果,客观缓解率(ORR)达57.4%,中位缓解持续时间(DOR)达10.4个月。且对于脑转移的实体瘤患者,entrectinib也能达到54.5%的颅内客观缓解率,其中有四分之一患者达到完全缓解。
目前获批三种不限癌种疗法
截至目前,已经有三款不限癌肿疗法获批,分别是Merck的Keytruda、Loxo Oncology和拜耳(Bayer)的Vitrakvi和罗氏的Rozlytrek,具体获批时间和适应症如下表:
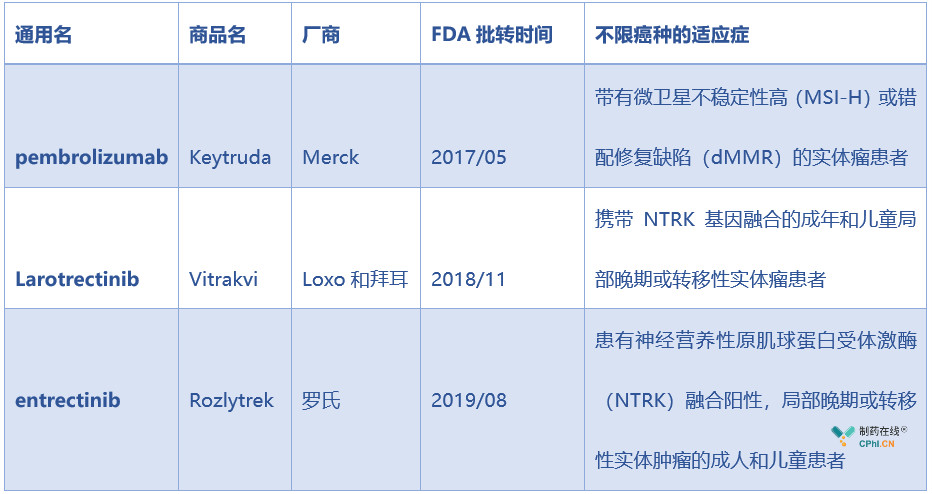
上述不限癌种疗法药物中,Keytruda 是一种人源化的PD1单抗,目前已被FDA批准非小细胞肺癌(NSCLC)、小细胞肺癌(SCLC)、头颈癌、肝细胞癌、肾癌等10多种适应症,2018年的全球销售额高达71.71亿美元。另外两款不限癌种疗法药物Vitrakvi和Rozlytrek都是泛癌种的化学靶向药,且均属于TRK抑制剂,其中Vitrakvi是FDA批准的第一款"不限癌种"针对多种携带NRTK基因变异的实体瘤的创新疗法,今年年初欧洲药品管理局(EMA)人用医药产品委员会(CHMP)建议批准其用于治疗患有神经营养性酪氨酸受体激酶(NTRK)基因融合的实体瘤儿童和成人患者,并且我国药品审评中心也已经受理以"硫酸Larotrectinib胶囊"为名称的IND申请。鉴于Vitrakvi在临床研究中疗效数据,行业分析师预测,到2024年其销售额有望达到10亿美元以上。Rozlytrek虽然较Vitrakvi获批晚,但是它能通过血脑屏障,是临床上唯一一种被证明针对原发性和转移性脑疾病具有疗效的TRK抑制剂,并且没有不良的脱靶活性,并且Rozlytrek也可以用于ROS1融合阳性NSCLC患者。
在研TRK抑制剂有哪些?
除了上述已经获批的TRK抑制剂,目前还有十多款在研的TRK抑制剂(详见下表)。其中最值得提的是LOXO-195,它也最初由Loxo Oncology研发,但是在今年年初礼来以80亿美元并购Loxo Oncology时,拜耳行使选择权,获得了LOXO-195和Vitrakvi在全球的开发和推广权。为什么要提LOXO-195 ?这主要是因为LOXO-195可以解决现有TRK抑制剂产生获得性抗性的问题。目前LOXO-195已经获得FDA授予的孤儿药资格,处于1/2期临床试验阶段,预计有望在2021年递交监管申请,2022年上市。
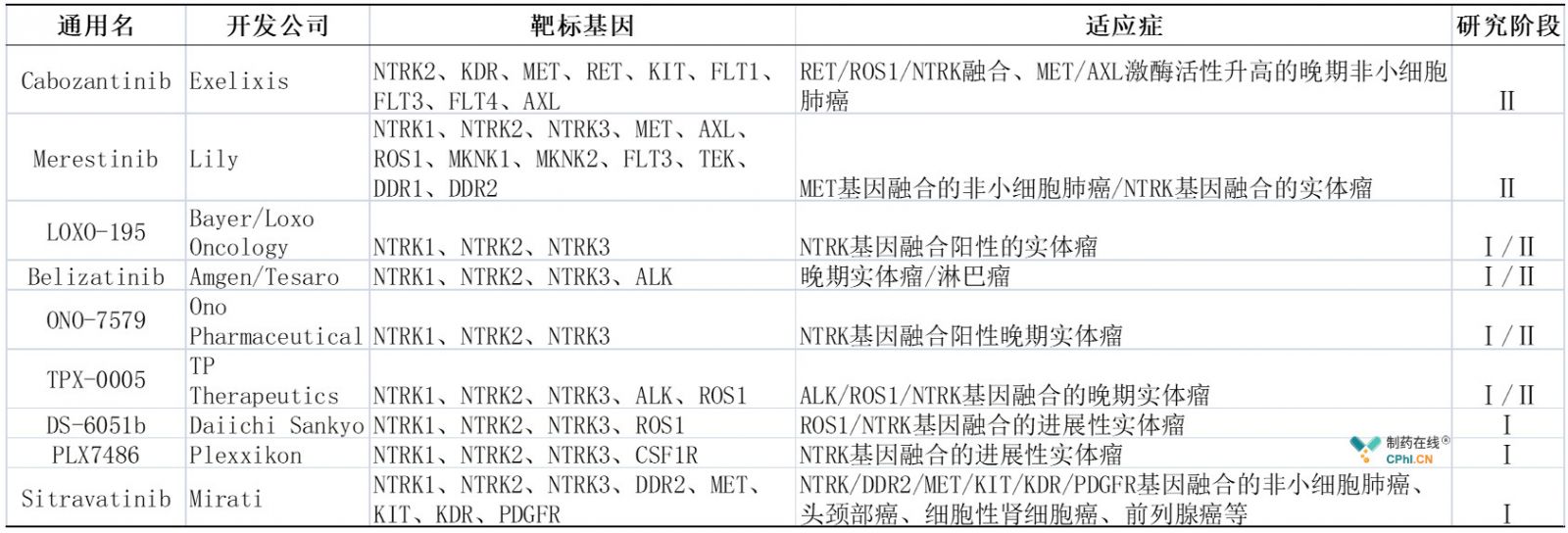
然而目前获批TRK抑制剂--Vitrakvi治疗成本特别高,30天的胶囊,费用高达32800美元,而Rozlytrek刚获批,价格未定, 估计也是价格不菲。最后衷心希望有更多的TRK抑制剂获批,以相对亲民的价格造福更多患者。
参考资料:
[1] FDA approves third oncology drug that targets a key genetic driver of cancer, rather than a specific type of tumor [2] FDA Approves Genentech's Rozlytrek (entrectinib) for People With ROS1-Positive, Metastatic Non-Small Cell Lung Cancer and NTRK Gene Fusion-Positive Solid Tumors
[2] Bayer to obtain full rights to global development and commercialization of oncology compounds Vitrakvi® (larotrectinib) and BAY 2731954 (LOXO-195). Retrieved February 15, 2019
[3] David Hyman et al. CT127 - Phase I and expanded access experience of LOXO-195 (BAY 2731954), a selective next-generation TRK inhibitor (TRKi)
版权所有,未经允许,不得转载。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030