https://www.cphi.cn 2019-10-11 14:28 来源:火石创造 作者:王跃
四、我国病毒清除/灭活验证技术服务机构
目前,进行病毒清除验证研究有三种方式:企业自验证、第三方验证、中检院验证(中国食品药品检定研究院)。限于建设生物安全二级实验室的高昂成本,以及在构建符合国内外申报标准的病毒清除/灭活验证体系方面的困难,比如获得相应的指示病毒株,为控制成本考虑,大多数生物制药企业主要提交中检院或者第三方机构开展病毒清除灭活验证。
近年来,单克隆抗体和重组蛋白类等生物制品研发热火朝天,在众多生物制药企业的迫切需求之下,第三方技术服务机构逐渐增多,并逐步接轨国际标准。目前,国内第三方检测机构有苏州药明康德检测检验、中科世生、义翘神州、苏州良辰、武汉珈创、南京钟鼎等。
表5 国内病毒清除/灭活验证技术第三方机构简介

以年均开展病毒清除业务批次为统计指标进行分析,南京钟鼎和药明检测在第三方服务市场中各占三分之一,北京义翘神州则排在第三位(占19%)。从地域分布上,第三方验证机构主要分布在北京和长三角等地区,华南和西部地区还是一片空白。
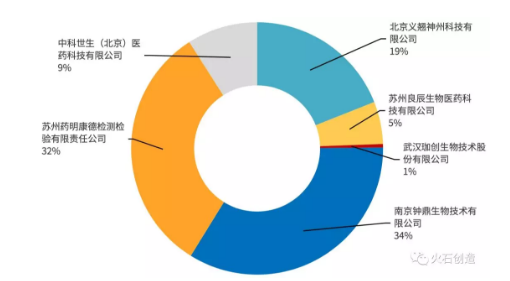
图 六家服务企业在第三方病毒清除验证市场份额
五、小结
目前生物制品病毒清除/灭活验证机构屈指可数,有些机构验证使用的方法或采用的指示病毒不同,其报告并不被国外评审机构认可,而申报国外的话,有时只能转战国外机构。由此可见,我国病毒清除验证领域还需深耕,亟待借鉴国际先进理念和经验,科学开展研究等提高行业实力。
参考文献/资料:
[1] 国家药品监督管理局.血液制品去除灭活病毒技术方法及验证指导原则[S].2002.
[2] FDA. Processvalidation: general principles and practives [S]. 2011.
[3] EMEA. Guideline onprocess validation [S]. 2012.
[4] EMEA. Guideline onprocess validation for manufacture of biotechnology-derived active substancesand data to be provided in the regulatory submission [M]. 2016.
[5]李敏,郭秀侠,刘伯宁.关于生物制品工艺验证的审评实践与思考[J]. 中国生物制品学杂志,2017,30(6):664-668,672.
[6]病毒去除/灭活验证国内外申报差异[EB/OL]. (2019-04-08).http://www.biodiscover.com/news/research/733716.html.
[7] 刘秋琳.生物制药安全的除病毒策略及新发现[EB/OL].https://www.docin.com/p-1441296290.html.
如需转载,请联系火石创造沟通授权事宜。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030