https://www.cphi.cn 2018-04-23 09:47 来源:赛柏蓝 作者:张自然
2018年4月12日,国务院总理在国务院常务会议上宣布“对创新化学药设置6年的数据保护期,保护期内不批准同品种上市。对在中国与境外同步申请上市的创新药给予最长5年的专利保护期限补偿”,业界为之振奋,标志着中国药品专利制度取得了实质性进展,再次彰显了国家对药物创新的强力支持。
实际上早在2017年5月出台的55号文就明确提出“建立药品专利链接制度”,10月发布的两办文件(42号文)提出“探索建立药品专利链接制度”,今年4月3日国务院发布的20号文件也提出“完善药品知识产权保护”。
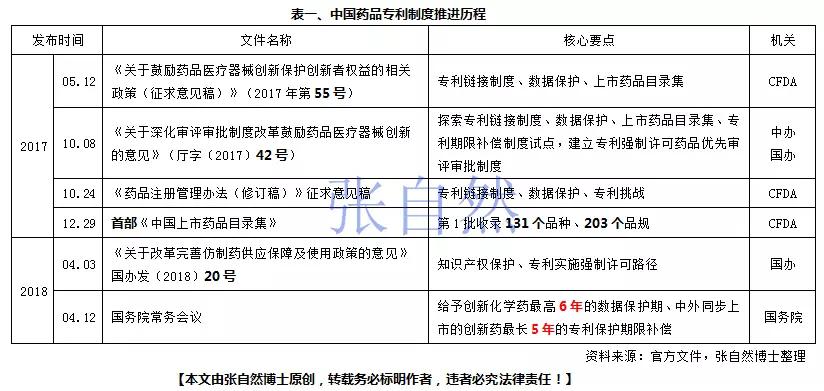
所谓“药品专利链接制度”是指将仿制药的上市批准审核(国家药监局职能)与创新药的专利期满审核(国家专利局职能)相衔接的一种制度,即仿制药注册申请应当考虑先前已上市药品的专利状况,以便在药品投放市场前就能发现可能发生的专利侵权问题,而不是等已投入了大量研发资源到产品上市后才发现有专利权纠纷。同时专利链接制度通过给予首仿药市场独占期,来鼓励专利挑战,促进仿制药的发展《张自然:我为什么极力主张开展仿制药?》,以降低医疗费用支出《药占比再加码!药企遭重创》,起到即保护创新、又鼓励仿制的双重作用。
美国的药品专利链接制度最完善(包含了橙皮书、Bolar例外、仿制药简化申请和数据保护期等制度),日本也建立了相对完善的专利连接制度,印度加入WTO后,其专利制度也基本与国际接轨。

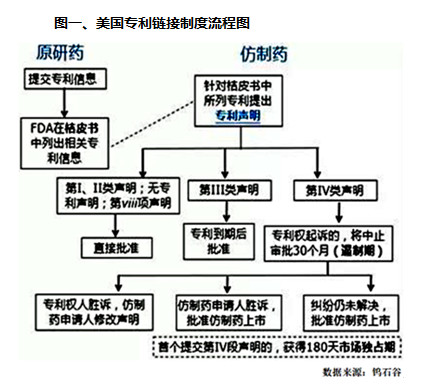
专利链接制度一般包括橙皮书、数据保护、专利期补偿、专利挑战、专利实施强制许可等。
一、橙皮书
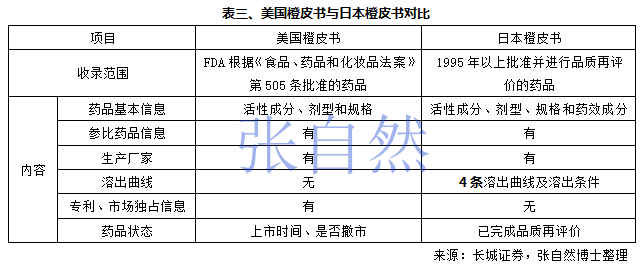
美国橙皮书(orange book)即《经过治疗等效性评价批准的药品》,收录了经由FDA审批的全部药品,尤其明确列出新药所涉及的所有专利以及市场专营保护信息。日本橙皮书(医疗用医药品品质情报集)则收录了已完成评价的部分品种(666个)的理化性质、溶出曲线、实验方法中文及日文链接等。
中国的橙皮书即《中国上市药品目录集》,于2017年12月29日首次发布,首部《中国上市药品目录集》收录了131个品种,203个品种规格,包含了专利和数据保护等信息,可为仿制者降低专利侵权风险,为实施专利链接制度提供数据支持。
二、数据保护
4月12日,国务院常务会议宣布,“对创新化学药设置6年的数据保护期,保护期内不批准同品种上市”。
所谓“数据保护”,就是通过赋予创新药企业(权利人)在数据保护期内对药品试验数据享有独占权,从而鼓励创新药研发及申报。其中独占权是指在数据保护期内,审批机构不得依赖权利人的数据批准其它申请人就已有国家标准的相同品种提出的仿制药申请。
为激励原研和首仿,FDA还给予获批药品一定时间的市场独占期(表四),在市场独占期内,FDA不会批准仿制药企业上市相应的仿制产品。

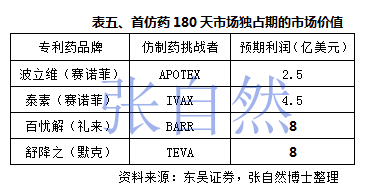
由于药物研发企业都做了充分准备,所以看似很短的180天市场独占期,实际上也可为药企赢得巨额回报,如百忧解和舒降之在180天的市场独占期内就分别为礼来和默克赚取了8亿美元的利润。
日本对部分新药专利期限最长可延长5年;
印度则为自授权日起5年和申请日起7年,以较短者为准;
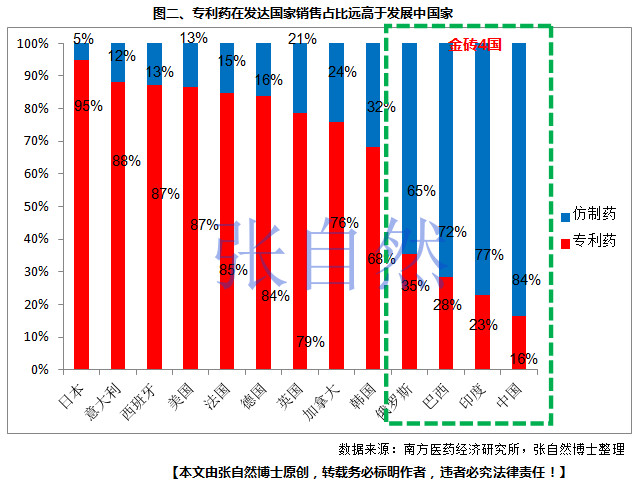
由于发达国家较完善的专利链接制度保护了研发企业的知识产权,从而确保了新药研发企业的市场预期,所以专利药在发达国家的销售占比远高于发展中国家(图二)。
中国以往在药物创新方面建树不多,主要是进口专利药在中国医药市场占据了可观的市场份额。
三、专利期补偿
4月12日,国务院常务会议宣布“对在中国与境外同步申请上市的创新药给予最长5年的专利保护期限补偿”。
所谓“专利期补偿”就是对药品和医疗器械因临床试验和行政审批所丧失的专利期予以补充的一种制度,美国对此延长的专利保护期为5年,并且延长期限加上药物上市时所剩余的专利期限之和不能超过14年。
但是,如果是申请人未尽到应有注意义务而导致专利期限耽搁的,该期限不计入延长期内。对同一药物只能申请一次专利期间延长,即使该药物有多项专利,而且仅药物的核心专利可延长,后续专利不能延长。
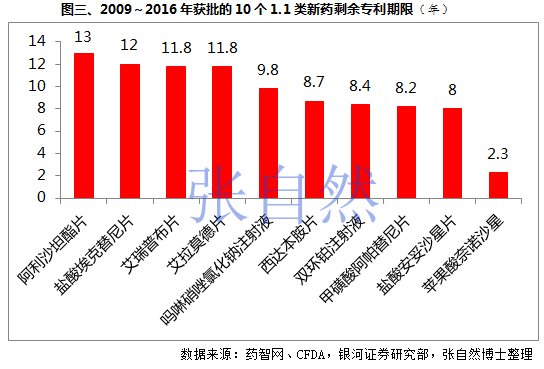
过去,中国新药审批流程较长,并且缺乏专利延期,导致无法对审批流程过长带来的损失进行补偿,专利有效期大幅缩短,如苹果酸奈诺沙星的专利期仅剩2.3年(图三),严重影响了医药企业研发的积极性和中国新药的可及性。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030