https://www.cphi.cn 2023-03-24 11:16 来源:药智数据 作者:姚姚乐
3月22日,北京奥赛康药业发布晚间公告,宣布其子公司江苏奥赛康药业有限公司的3款仿制药获得药品注册证书,分别为注射用唑来膦酸浓溶液、注射用伏立 康唑和塞瑞替尼胶囊。其中,塞瑞替尼胶囊为上市首仿药。
肿瘤相关药,1款上市首仿
奥赛康药业此次获得药品注册证书的3款药物都为仿制药,具体如下:
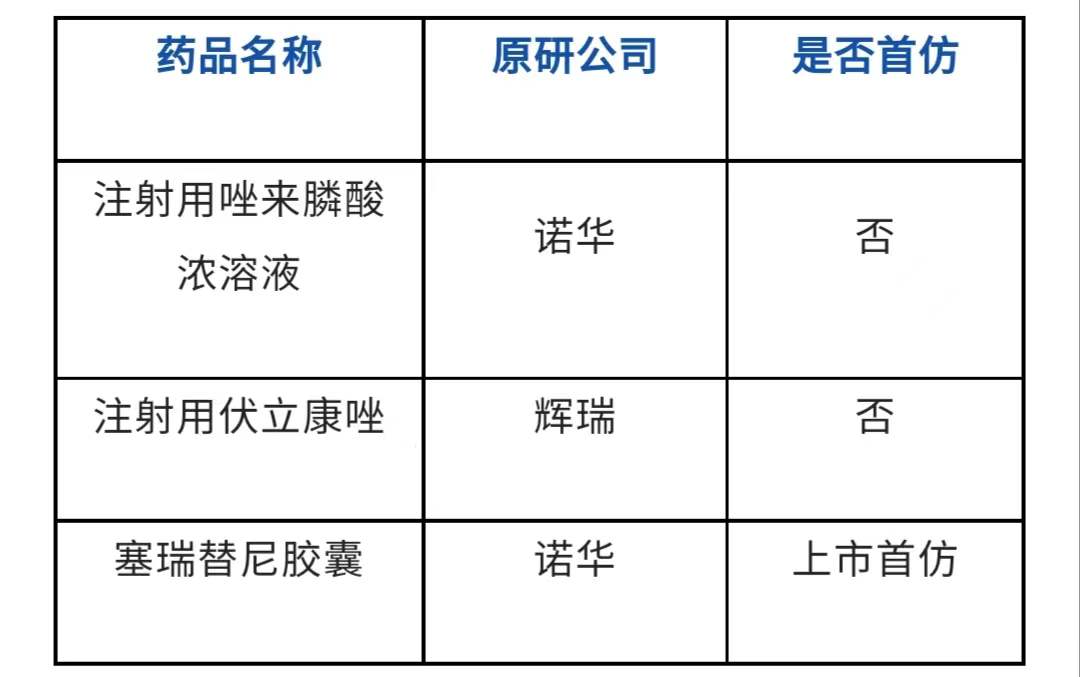
资料来源:奥赛康公告
1、注射用唑来膦酸浓溶液
唑来膦酸是一款破骨细胞活性抑制剂。根据奥赛康药业,其获批适应症为:与标准抗肿瘤药物治疗合用,用于治疗实体肿瘤骨转移患者和多发性骨髓瘤患者的骨骼损害。用于治疗恶性肿瘤引起的高钙血症(HCM)。
药智数据显示,诺华原研的唑来膦酸目前获批适应症主要有变形性骨炎、多发性骨髓瘤和绝经后骨质疏松症等。其中,变形性骨炎和绝经后骨质疏松症已在国内获批。
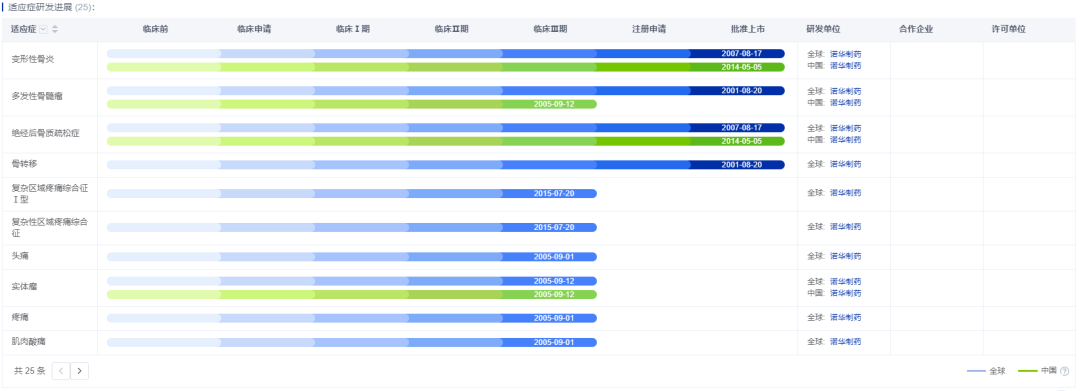
图片来源:药智数据——全球药物
2、注射用伏立 康唑
注射用伏立 康唑是一种广谱的三唑类抗真菌药。根据奥赛康药业,其适用于治疗成人和2岁及2岁以上儿童患者的下列真菌感染:
(1)侵袭性曲霉病。
(2)非中性粒细胞减少患者的念珠菌血症。
(3)对氟康唑耐药的念珠菌引起的严重侵袭性感染(包括克柔念珠菌)。
(4)由足放线病菌属和镰刀菌属引起的严重感染。
根据药智数据,辉瑞原研的伏立 康唑目前也已有中性粒细胞减少症、侵袭性曲霉病等多个适应症获批上市。值得注意的是,伏立 康唑还有治疗食管癌、非黑色素瘤皮肤癌等癌症的适应症在研。
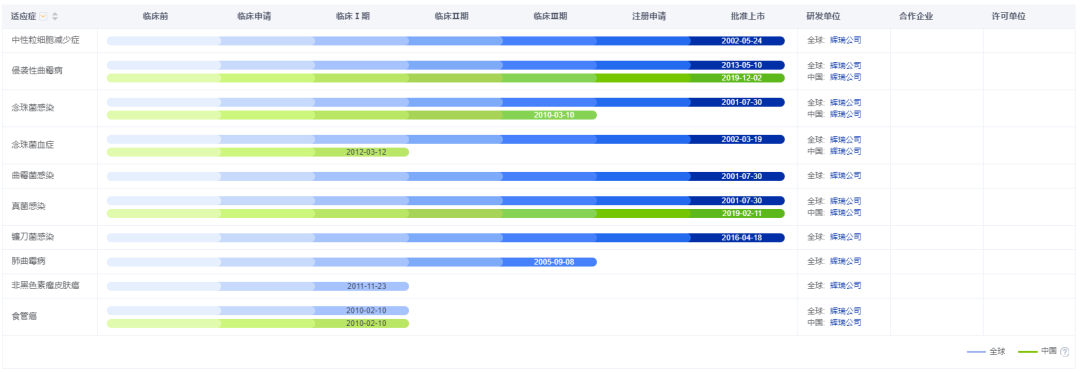
图片来源:药智数据——全球药物
3、塞瑞替尼胶囊
根据公告,奥赛康为国产首家获得塞瑞替尼胶囊生产药品注册证书的企业。
塞瑞替尼是ALK、胰岛素样生长因子1受体(I GF-1R)、胰岛素受体(InsR)2和ROS1等多靶点激酶抑制剂,适用于间变性淋巴瘤激酶(ALK)阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者的治疗。
药智数据显示,诺华原研的塞瑞替尼目前已有局部晚期非小细胞肺癌、淋巴瘤和转移性非小细胞肺癌等多个适应症获批。
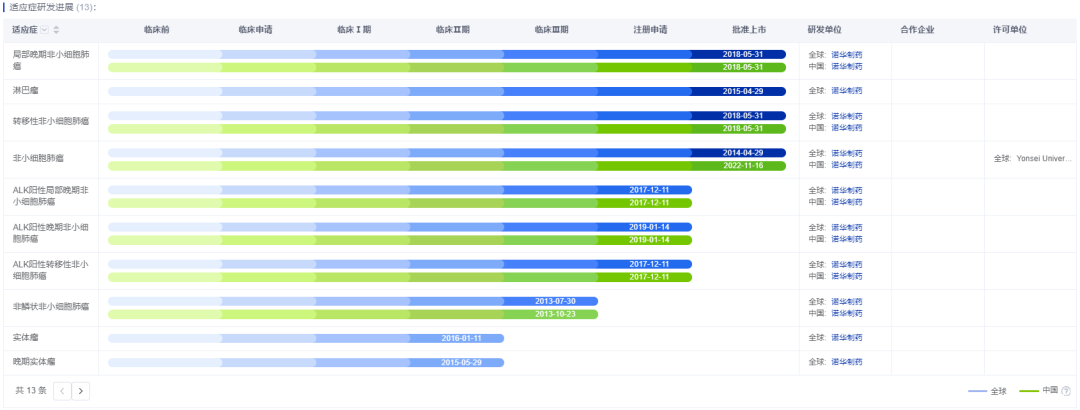
图片来源:药智数据——全球药物
虽然奥赛康为国产首家获得塞瑞替尼胶囊生产药品注册证书的企业,但是诺华原研的塞瑞替尼专利尚未到期。根据相关法律法规,目前奥赛康的塞瑞替尼胶囊尚不能上市销售。诺华的塞瑞替尼胶囊于2018年在中国上市后,短短数月便被纳入了国家医保。塞瑞替尼胶囊往年销售额可参考下图:
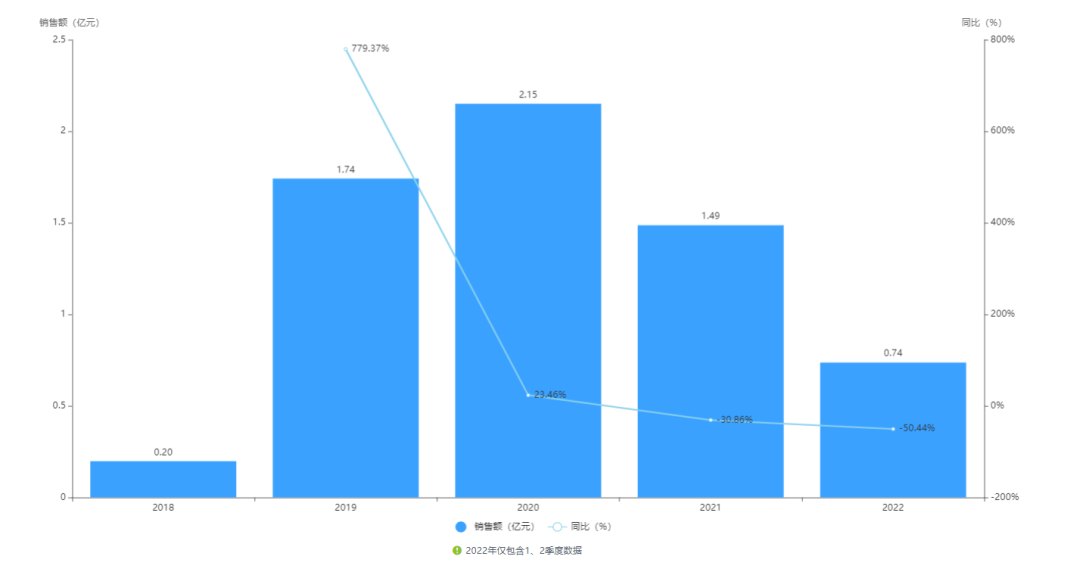
图片来源:药智数据——医院销售数据挖掘系统
由此看来,待奥赛康的塞瑞替尼胶囊上市销售后,是否可以分一块“饼”,还有待时间来证明……
小 结
奥赛康是国内PPI注 射剂龙头企业之一,细看产品管线,可以其发现仿制药实力不俗,不过创新药也“不甘示弱”。前不久,其新药注射用ASKG915临床获CDE受理,去年年末还获FDA批准开展临床试验……据相关报道,奥赛康对研发投入持续“加码”。近年来,国内企业对新药创新研发越来越重视,从Big Pharma的成长经验来看,这是药企实现可持续发展的重要因素!
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030