https://www.cphi.cn 2023-11-07 10:31 来源:上海证券交易所
近日,湖北济川药业股份有限公司(以下简称“公司”)全资子公司济川药业集团有限公司(以下简称“济川有限”)收到国家药品监督管理局(以下简称“国家药监局”)核准签发的盐酸艾司洛尔注射液《药品注册证书》和布洛芬混悬液《药品注册证书》,现将情况公告如下:
一、药品注册证书的基本情况
1、盐酸艾司洛尔注射液
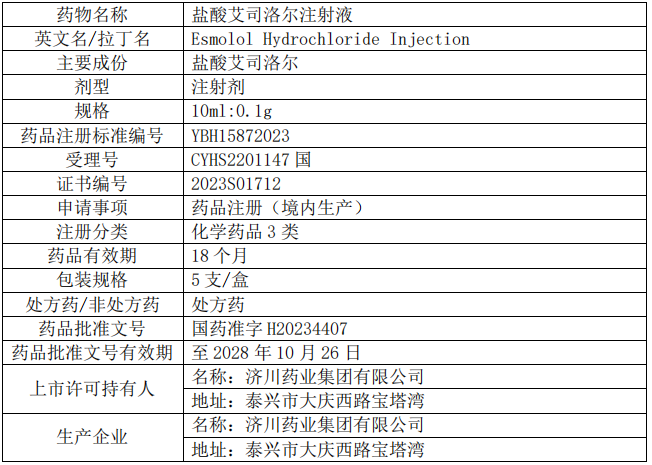

2、布洛芬混悬液
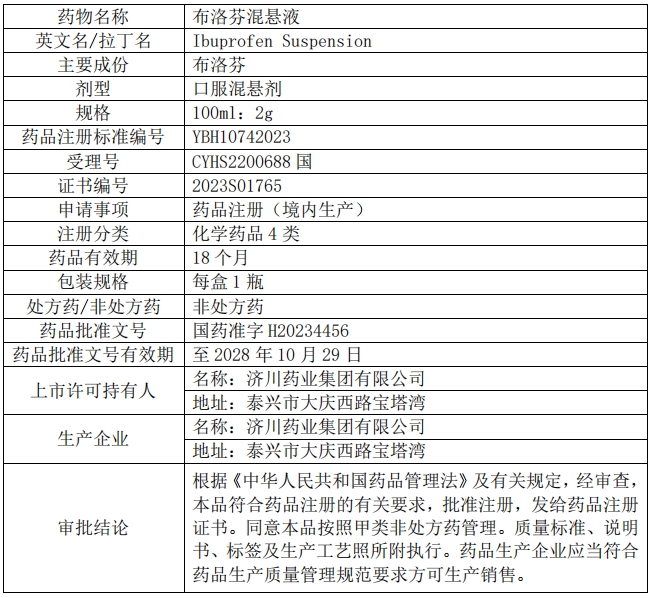
二、药物研究的相关情况
1、盐酸艾司洛尔注射液
盐酸艾司洛尔注射液用于治疗室上性心动过速或非代偿性窦性心动过速、术中及术后心动过速和/或高血压。盐酸艾司洛尔注射液最早由 Baxter HealthcareCorporation 公司研发,于 1986 年在美国上市,该品种目前已在美国、日本、德国、英国等多个国家批准上市,原研药品未在我国上市。
该产品由重庆药谷科技发展有限公司与济川有限联合研制开发,济川有限盐酸艾司洛尔注射液首次提交注册申请获得受理的时间为 2022 年 07 月 26 日。盐酸艾司洛尔注射液注册分类为化学药品 3 类,按照与参比制剂质量和疗效一致的技术要求审评并获批,批准后视同通过仿制药质量和疗效一致性评价,适应症包括室上性心动过速或非代偿性窦性心动过速、术中和术后心动过速和/或高血压。
2、布洛芬混悬液
布洛芬混悬液用于儿童普通感冒或流行性感冒引起的发热,也用于缓解儿童轻至中度疼痛,如头痛、关节痛、偏头痛、牙痛、肌肉痛、神经痛。Johnson &Johnson Consumer Inc.(强生公司)的布洛芬混悬液最早于 1992 年 07 月 31 日在德国获准上市(规格:20mg/ml 和 40mg/ml),1995 年 06 月 16 日在美国 FDA 获批上市(规格 5ml:100mg),并于 1999 年 03 月 17 日在国内上市,商品名:美 林,规格 100ml:2g,持证商为上海强生制药有限公司。
济川有限布洛芬混悬液首次提交注册申请获得受理的时间为 2022 年 04 月27 日。截至目前,该药品累计研发支出约 1,210 万元(未经审计),均已费用化。
布洛芬混悬液注册分类为化学药品 4 类,按照与参比制剂质量和疗效一致的技术要求审评并获批,批准后视同通过仿制药质量和疗效一致性评价,适应症包括用于儿童普通感冒或流行性感冒引起的发热,也用于缓解儿童轻至中度疼痛,如头痛、关节痛、偏头痛、牙痛、肌肉痛、神经痛。
三、药品的其他情况
1、盐酸艾司洛尔注射液
目前,除济川有限外,国内已有包括齐鲁制药、齐鲁制药(海南)、浙江华海药业、北京新美泰克、海南灵康、扬州中宝、杭州沐源等在内 7 家企业通过一致性评价或视同通过一致性评价获批生产盐酸艾司洛尔注射液。盐酸艾司洛尔注射液已被列入《国家基本医疗保险、工伤保险和生育保险药品目录》(2022 版)乙类药品。
据米内网数据显示,2022 年中国城市公立医院盐酸艾司洛尔注射液的销售额超 8 亿元。
2、布洛芬混悬液
目前,除济川有限外,国内已有包括湖北多瑞、华润三九(南昌)、海南万玮(新报)、新华制药(高密)、山东盛迪、黑龙江中桂等在内 6 家企业视同通过一致性评价获批生产布洛芬混悬液溶液。布洛芬混悬液已被列入《国家基本医疗保险、工伤保险和生育保险药品目录》(2022 版)乙类药品。
据米内网数据显示,2022 年中国城市公立医院布洛芬混悬液的销售额超过2 亿元;2022 年中国城市实体药店布洛芬混悬液销售额超 9 亿元。
四、药品投产上市的后续安排
盐酸艾司洛尔注射液和布洛芬混悬液的上市销售还需要进行招投标等一系列市场开发工作,公司将争取尽快推进盐酸艾司洛尔注射液和布洛芬混悬液投入生产并上市销售。
五、对公司本期业绩的影响及风险提示
此次公司获得盐酸艾司洛尔注射液以及布洛芬混悬液的《药品注册证书》,是对公司产品的进一步补充,丰富了公司产品线,预计将对公司今后的发展起到积极作用。药品的上市需要一定的市场开发周期,此外,产品销售业务易受到国内医药行业政策变动、招标采购、市场环境变化、集中采购等因素影响,存在不确定性,敬请广大投资者理性投资,注意投资风险。
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030