https://www.cphi.cn 2019-03-22 17:06 来源:米内网
国内首家提交NDA,国际化进程加快
除了研发创新,国际化也是石药集团未来的发展方向。3月5日,石药集团发布公告,公司已成功就马来酸左旋氨氯地平片向FDA提交新药上市申请,成为我国首家向FDA提交NDA的制药企业。
石药集团的马来酸左旋氨氯地平片于2003年获得国家药监局批准上市,商品名为玄宁,目前已成为公司核心产品之一。该产品于美国的临床开发是以中国的疗效数据和增强的安全性资料为根据,2018年10月与FDA进行新药上市申请前会议,同年12月完成关键性临床研究后提交新药上市申请。
表5:石药集团海外研发管线
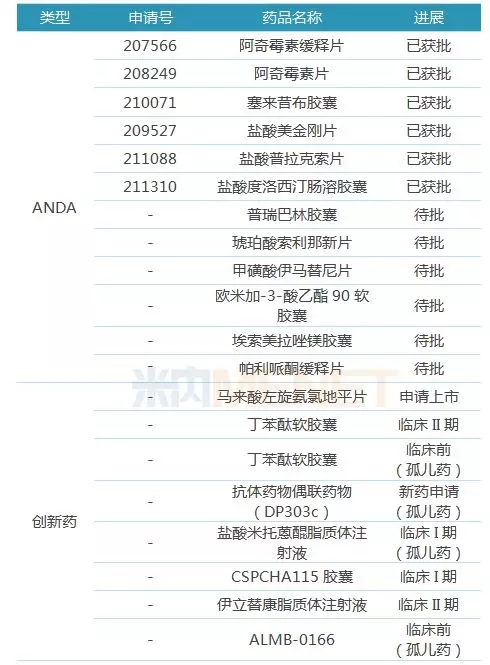
除了已经成功递交的首个NDA批文,石药集团在ANDA上也收获颇丰。报告期内收获6个ANDA,还有6个ANDA待获批,抗体药物偶联物DP303c(胃癌)、丁苯酞软胶囊(肌萎缩性脊髓侧索硬化症)、ALMB-0166(急性脊髓损伤)于美国获得孤儿药资格认定,CSPCHA115胶囊开展I期临床。
点击下图,预登记观展
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030