Part 1
全球/中国新药批准动态
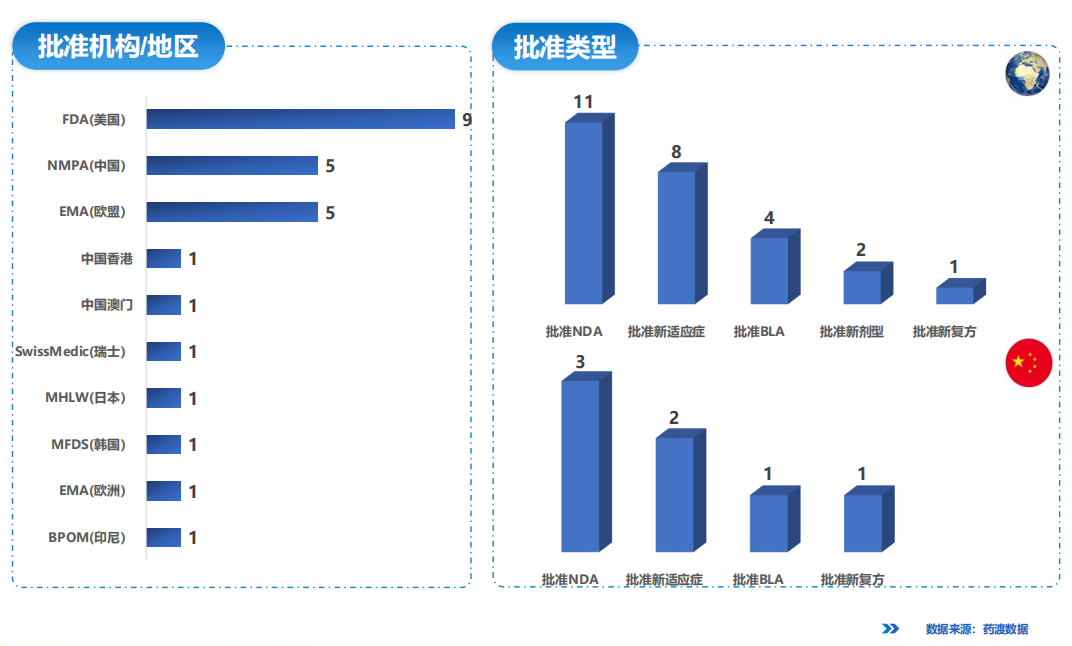
01全球/中国新药12月批准情况
2023年12月全球新药批准共计26个,其中中国新药批准共计7个。
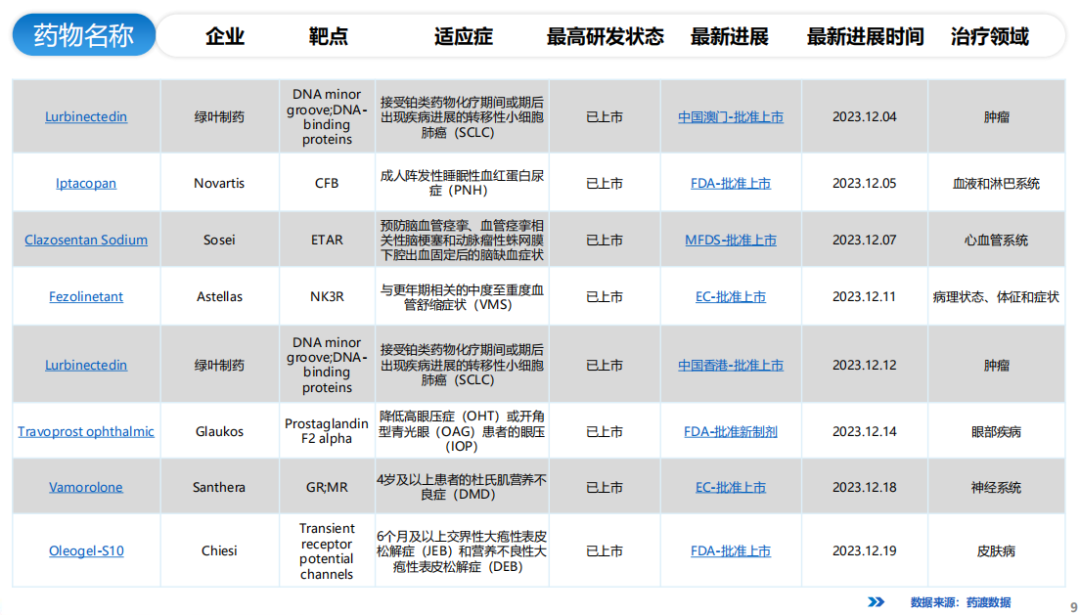
全球/中国NDA批准详情(部分)
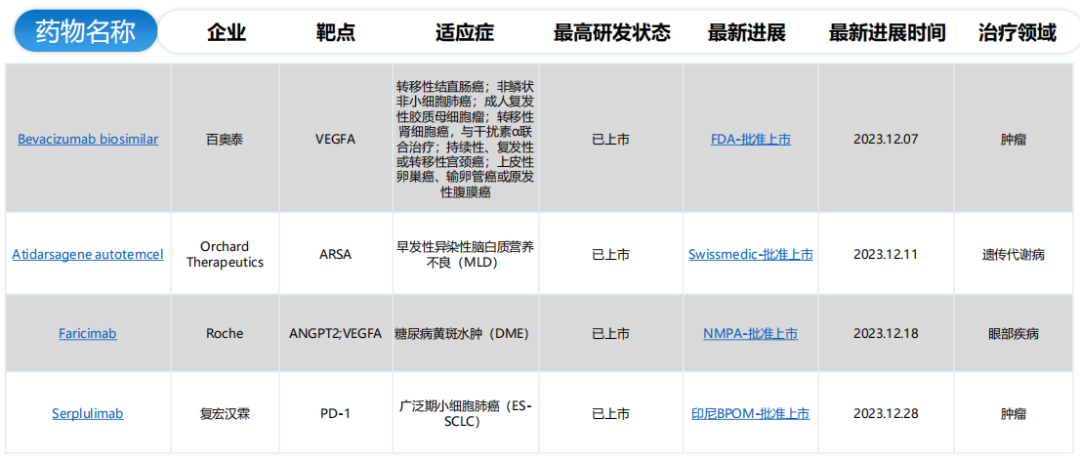
全球/中国BLA批准详情
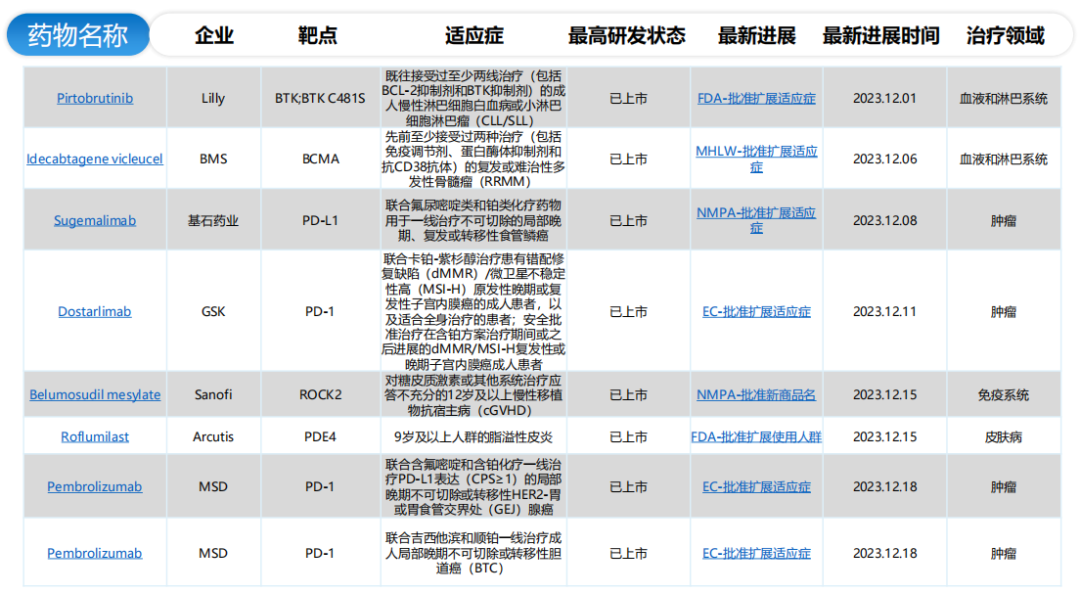
全球/中国扩展适应症批准详情(部分)
全球/中国新剂型批准详情

全球/中国新复方批准详情

02
全球/中国新药12月批准领域概览
本月全球批准新药中,肿瘤领域占比最大31%,涉及小细胞肺癌、胆道癌及胃癌等;其次是感染及血液和淋巴系统,适应症包括侵袭性念珠菌病,多发性骨髓瘤及巨细胞病毒感染等。
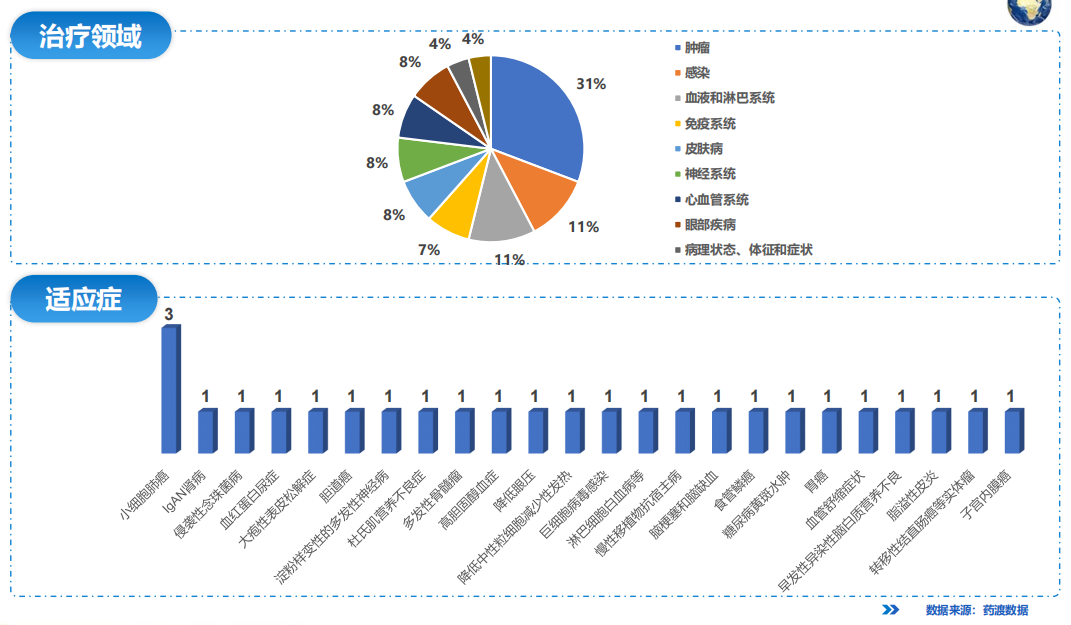
本月中国批准新药中,肿瘤领域占比最大,达43%,适应症涉及小细胞肺癌及食管癌。
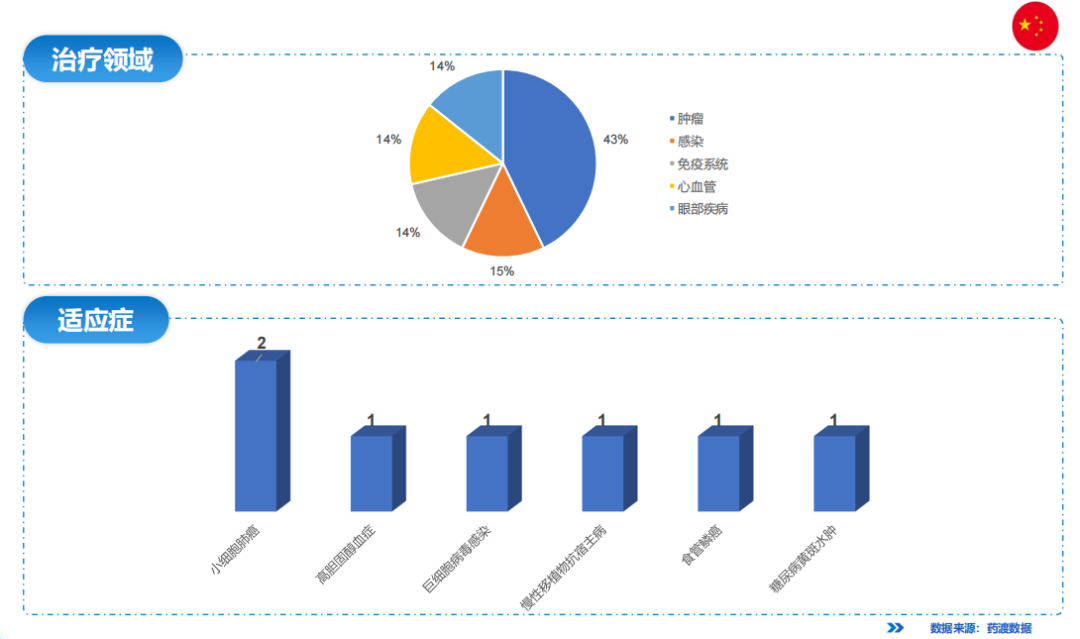
03
重磅药物解析

伊普可泮(Iptacapan)
Fabhalta是一种口服、首 创(first-in-class)、有效和选择性的补体B因子(FB)小分子抑制剂,作用于免疫系统的补体旁路途径中的近端通路,可与补体替代通路的因子B结合,调节C3的裂解、下游效应物的产生和末端通路的扩增,可全面控制血管内外的红细胞(RBC)破坏(血管内和血管外溶血[IVH和EVH])。
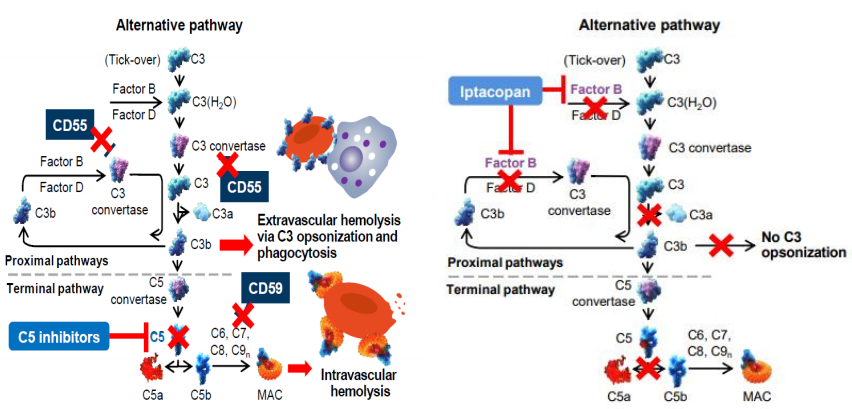
阵发性睡眠性血红蛋白尿症(PNH)是一种罕见的血液系统疾病,临床表现特征包括血管内溶血(IVH)、血栓形成和骨髓衰竭。
除PNH之外,Fabhalta目前也处于其他许多补体介导疾病的研究阶段,包括免疫球蛋白A肾病(IgAN)、C3肾小球疾病(C3G)、免疫复合物膜增殖性肾小球肾炎(IC-MPGN)和非典型溶血性尿毒症综合征(aHUS)。
Part 2
2024年1月可能获批的药物预测
2024年1月可能获批的药物预测(部分)
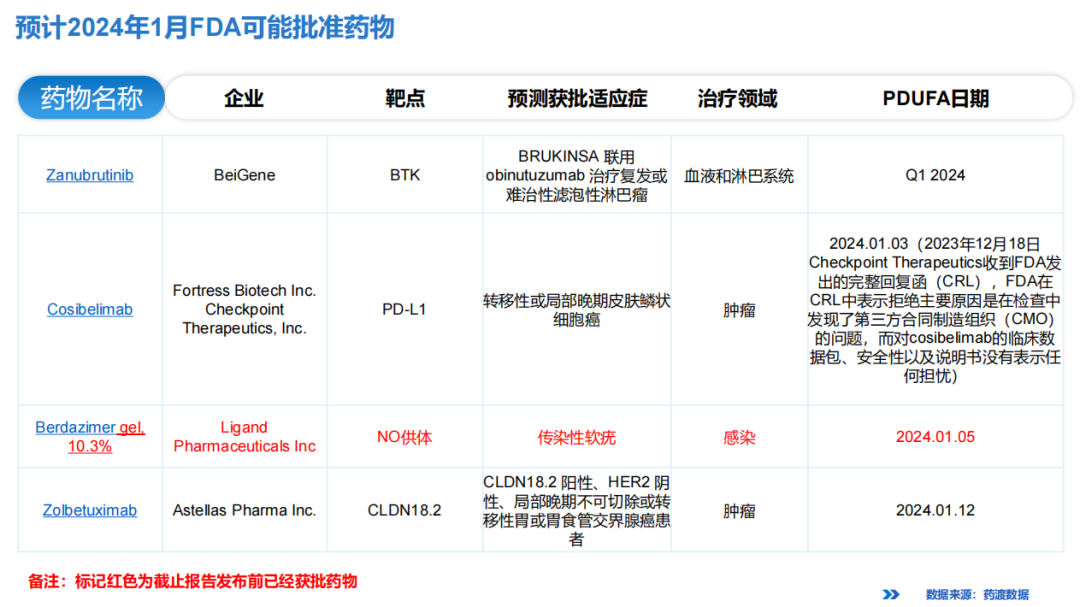
Part 3
全球/中国新药申报动态
01全球/中国新药12月申报情况
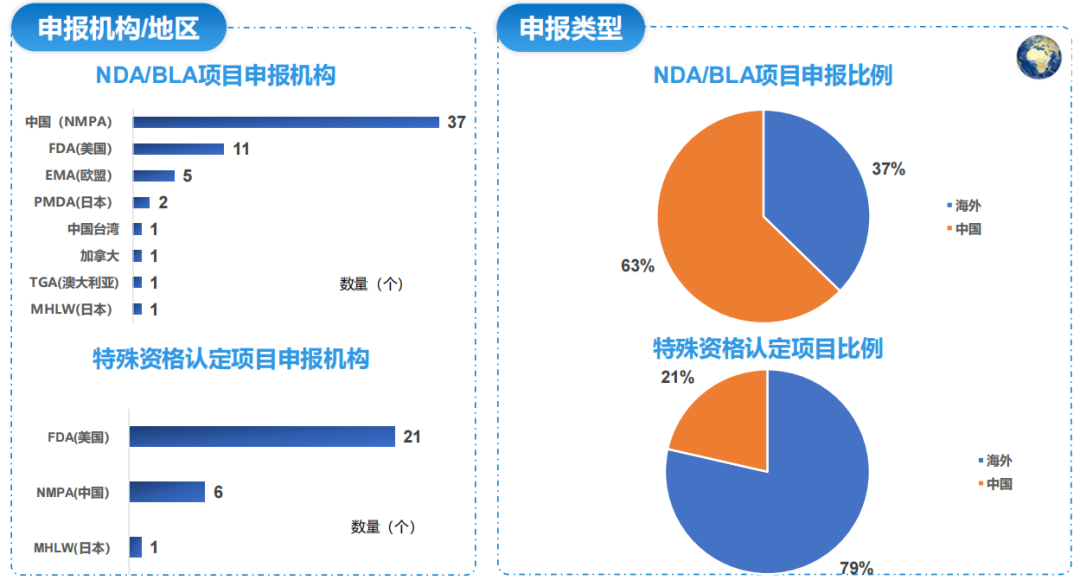
2023年12月全球新药NDA/BLA项目共计59个,其中中国NDA/BLA项目37个;特殊资格认定申报项目共计28个,其中中国申报项目6个。
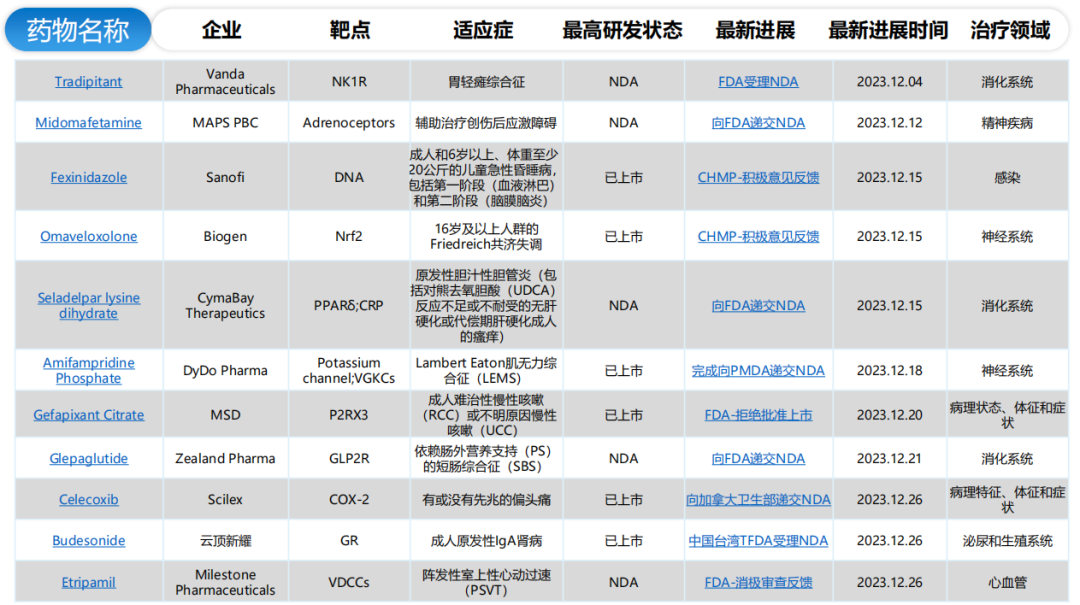
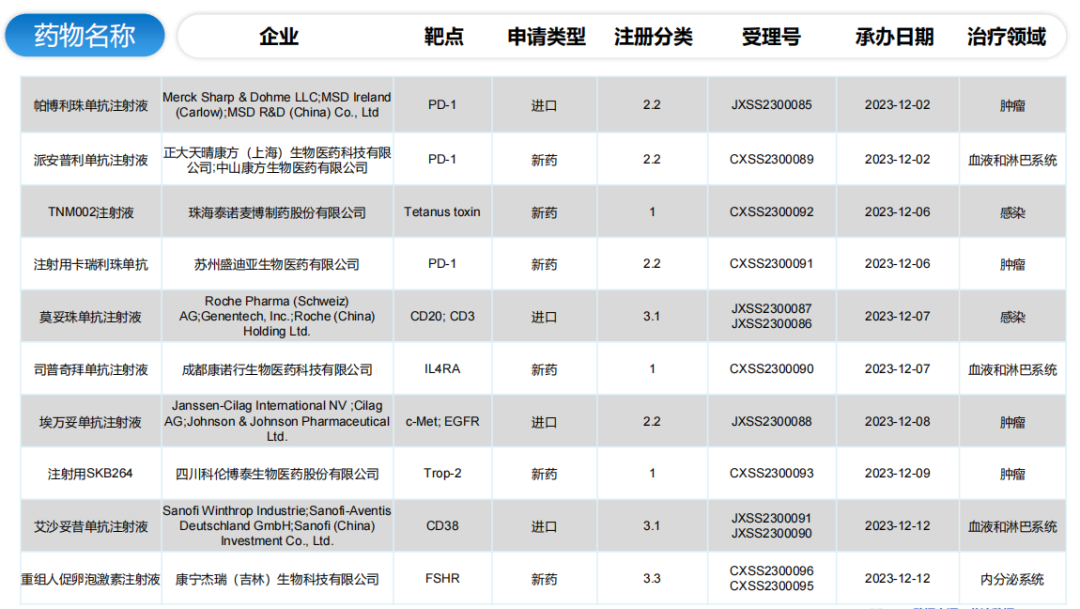
全球/中国NDA申报详情(部分)
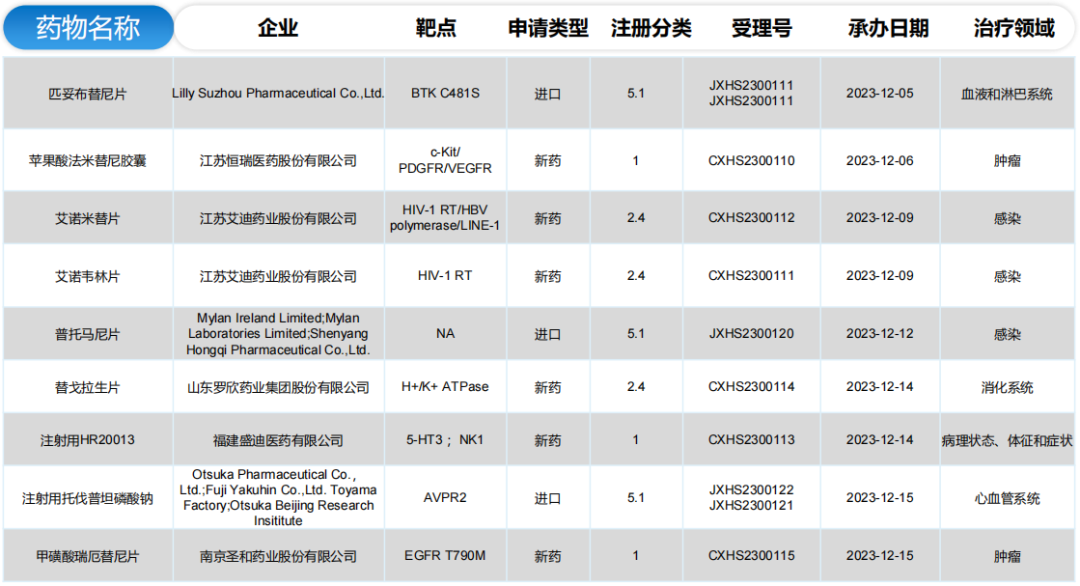
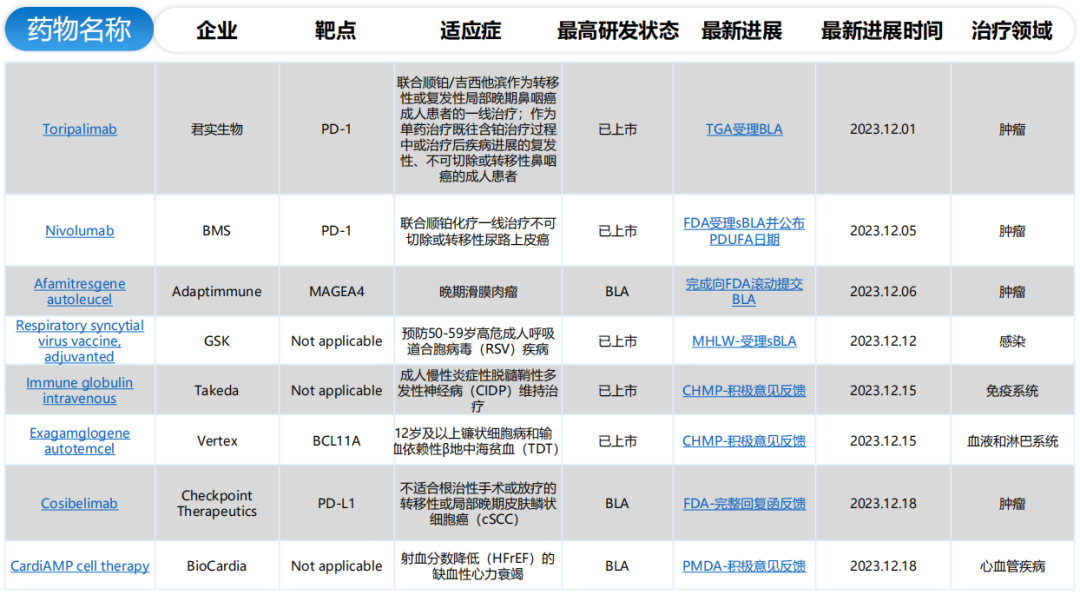
全球/中国BLA申报详情(部分)
02
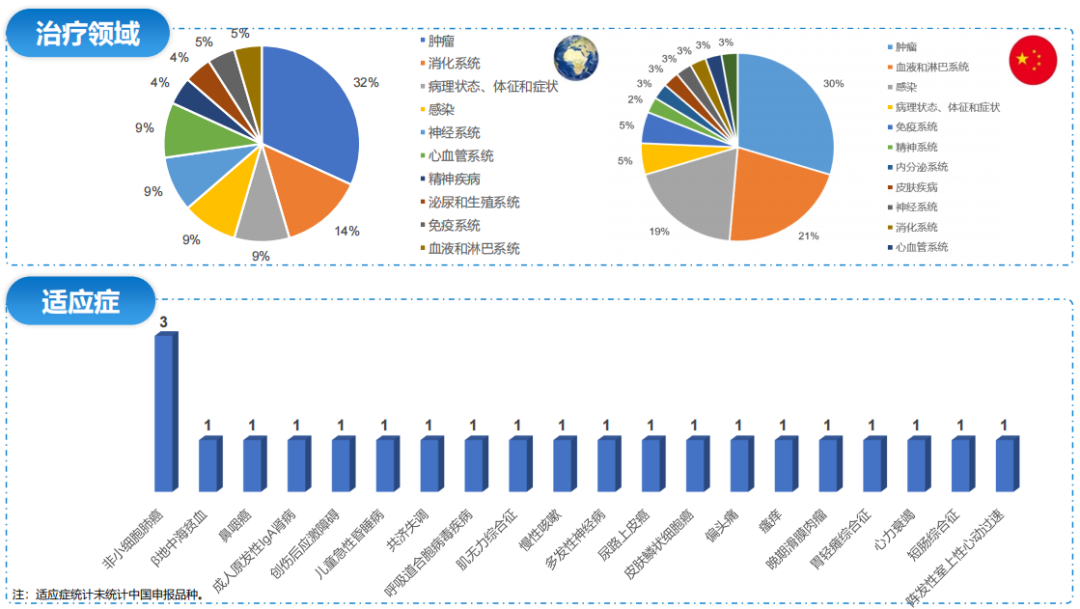
全球/中国新药12月申报领域概览
本月海外及中国NDA/BLA申报项目均主要集中血液和淋巴系统、肿瘤,及免疫系统等领域其中,肿瘤领域在海外和中国申报项目占比分别为19%及33%。
03
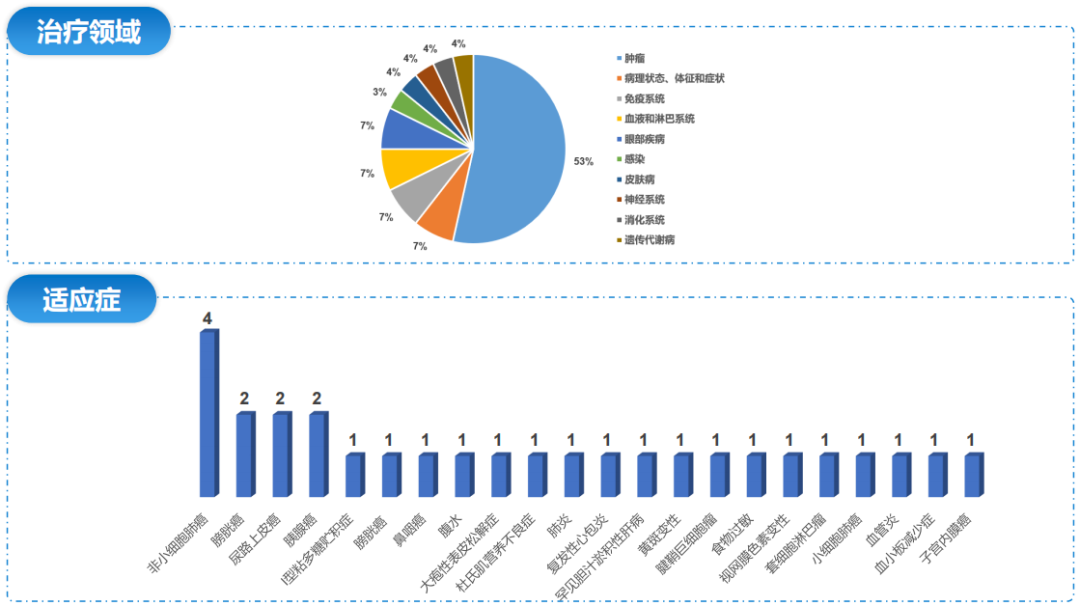
全球/中国新药特殊资格认定
本月全球特殊资格认定申报项目共计28个(中国6个),主要集中肿瘤占比为53%免疫系统、血液接淋巴系统及眼部疾病等占比均为7%,细分适应症包括非细胞肺癌,胃癌等。
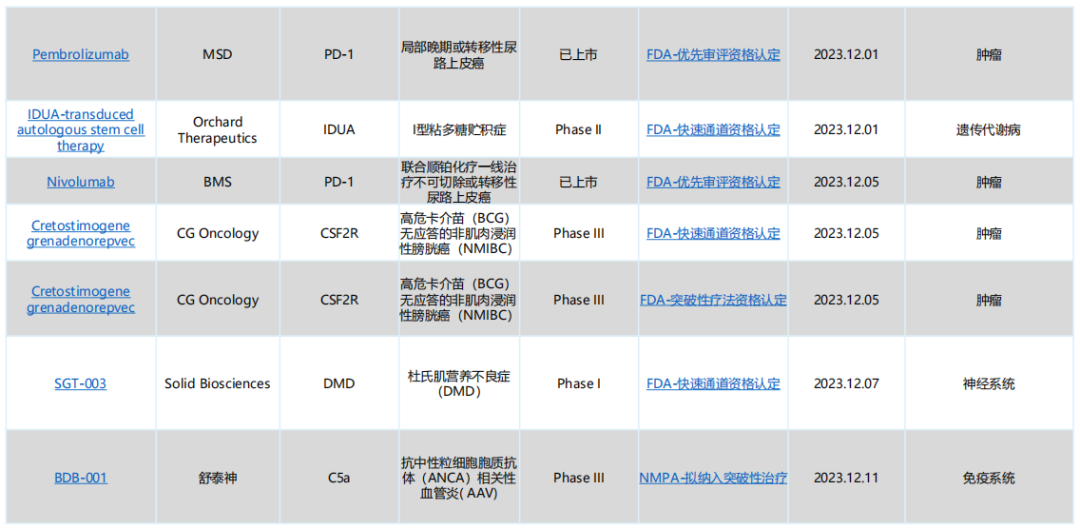
全球/中国特殊资格认定(化学药)(部分)
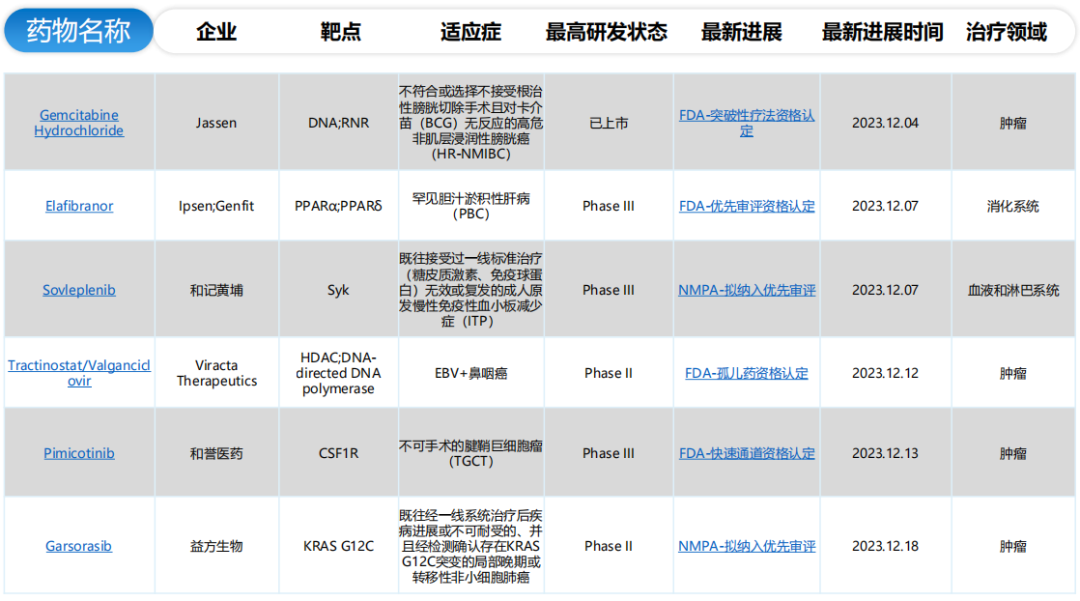
全球/中国特殊资格认定(生物药)(部分)
04
重磅药物解析

Glepaglutide
Glepaglutide是Zealand Pharma开发的一种长效GLP-2类似物,稳定状态下的有效半衰期约为88小时,通过自动注射器每周两次皮下给药。Zealand Pharma于2023年12月21日向FDA递交NDA,适应症为依赖肠外营养支持(PS)的短肠综合征(SBS)。
短肠综合征(简称SBS)是由于小肠较短,功能较弱所引起的吸收异常,主要症状是腹泻,其可导致脱水,营养不良和体重减轻。
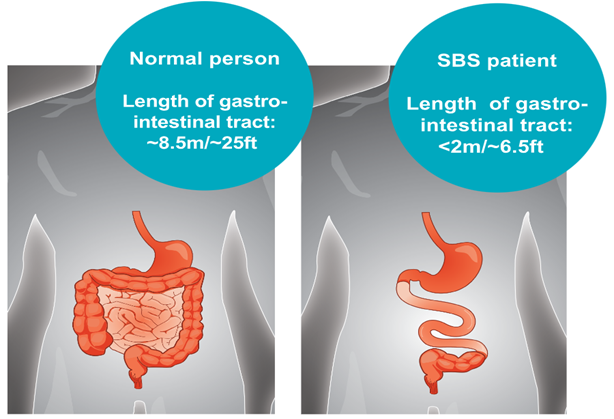
胰高血糖素样肽2 (GLP-2) 是一种33个氨基酸的多肽,GLP-2及其关类似物可用于治疗短肠综合征、克隆氏症、骨质疏松症以及作为癌症化疗期间的辅助治疗。
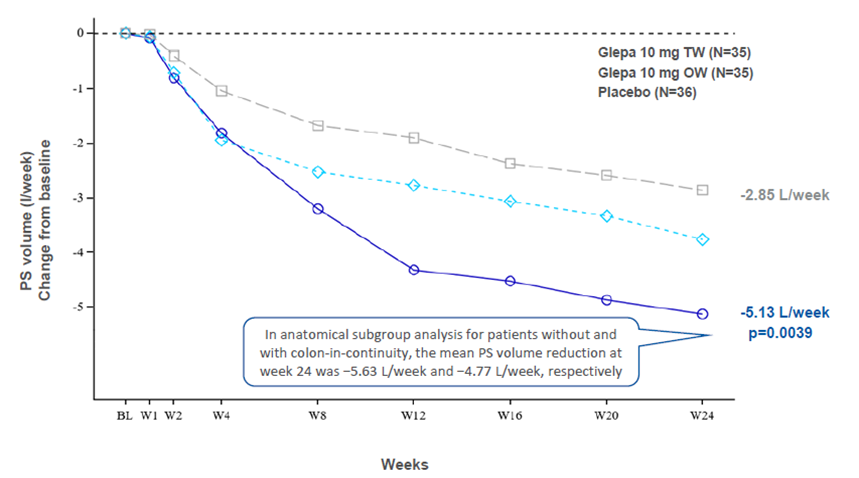
本次提交是基于关键性随机、双盲临床3期研究EASE-1(NCT03690206)的数据,研究入组了106名每周至少三天依赖肠外支持(PS)的SBS患者,评估每周一次和两次皮下注射Glepaglutide 10mg的安全性和有效性。结果显示:
与安慰剂组对比,每周两次Glepaglutide给药在第24周显著降低患者每周PS所需总液体体积:Glepaglutide组 vs 安慰剂组:5.13公升/周 vs 2.85公升/周
在无结肠连续性和有结肠连续性患者的解剖亚组分析中,第24周时的平均PS体积减少分别为-5.63L/周和-4.77L/周。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57