3月25日,据CDE官网显示,北京抗创联生物制药技术研究有限公司;石药集团中奇制药技术(石家庄)有限公司(以下简称“石药集团”)的2.2类化药新药司美格鲁肽注射液获得临床试验默示许可,适用于减少热量饮食和增加体力活动的基础上对成人超重或肥胖患者的体重管理。
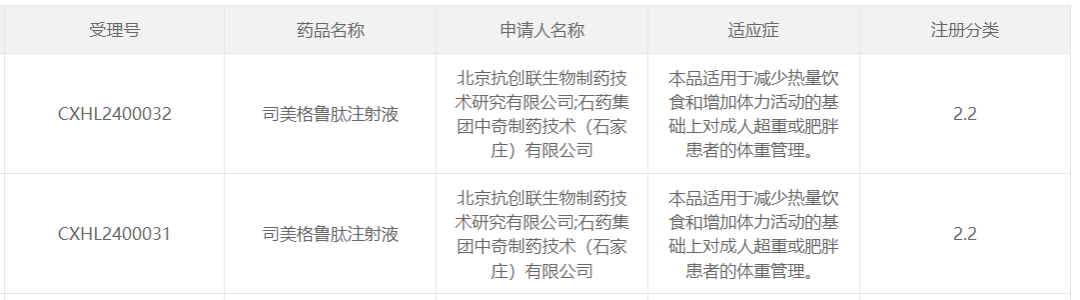
图片来源:CDE官网
01
2.2类化药
Ⅲ期临床已启动
2023年,司美格鲁肽为诺和诺德贡献了211.57亿美元销售额,其中减肥版 Wegovy 销售额约45.48 亿美元。本月初,FDA又批准Wegovy用于降低患有心血管疾病和肥胖或超重的成人心血管死亡、心脏病发作和中风风险的新适应症。毫无疑问,2024年司美格鲁肽将仍然是市场价值及适应症拓展方面最 具潜力的药物之一。
目前,国内已有多家企业布局司美格鲁肽生物类似药或改良型新药。2023年8月,石药集团的司美格鲁肽注射液获得NMPA临床试验批准,用于成人2型糖尿病患者的血糖控制,该药物是一款2.2类化药新药。
据石药集团新闻稿显示,该产品完全使用化学合成法制备,与DNA重组技术制备的司美格鲁肽注射液相比杂质水平更低。此外,石药集团的司美格鲁肽在2~8℃长期储存条件下无新杂质产生。

图片来源:石药集团
在临床前研究中,石药集团的司美格鲁肽展现出了与DNA重组技术制备的司美格鲁肽相似的体外生物活性和体内降糖效果。日前,石药集团在报道中提到,2024年2月司美格鲁肽在中国开展的用于治疗2型糖尿病的Ⅲ期临床研究首家启动,目前处于入组阶段。
本次用于减重的临床试验申请成功获批后,该产品的研究进度有望进一步加速。
02
GLP-1、DPP-4…
消化及代谢管线
石药集团聚焦抗肿瘤、精神神经、心脑血管、消化与代谢等六大领域,已建起涵盖化学创新药、生物制剂创新药、新型制剂的研发管线。其中,在消化与代谢领域,石药集团多款药物正处于临床阶段或提交了上市申请。
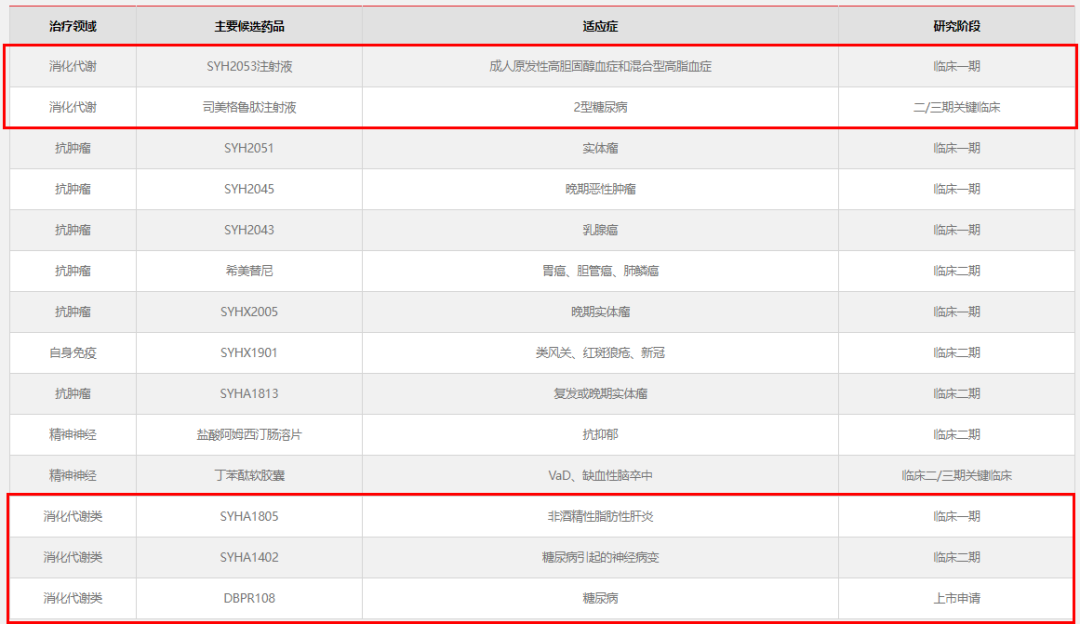
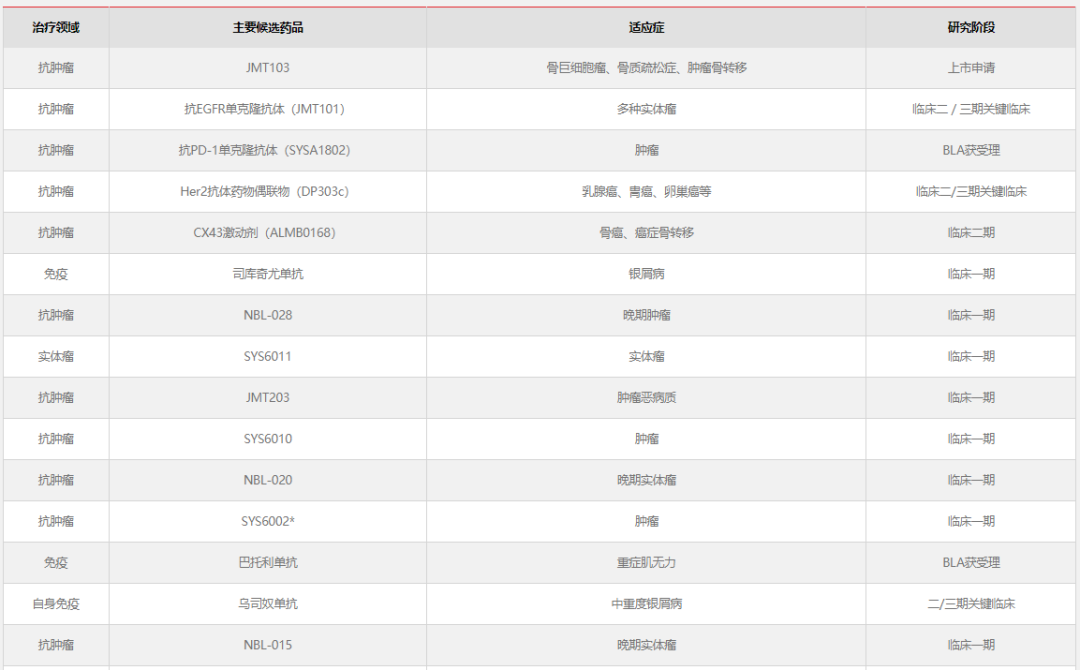
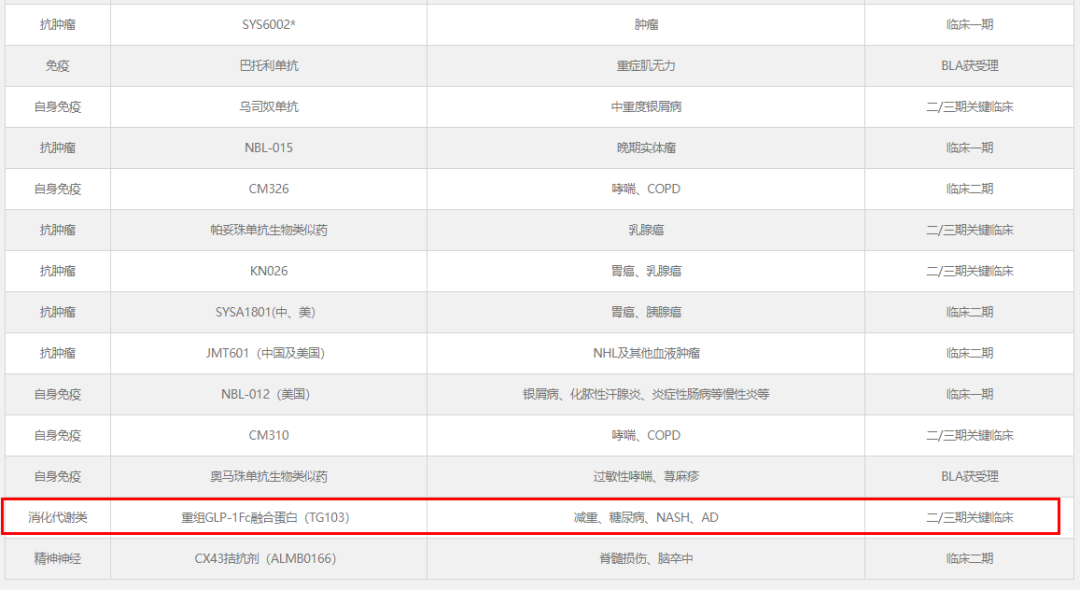
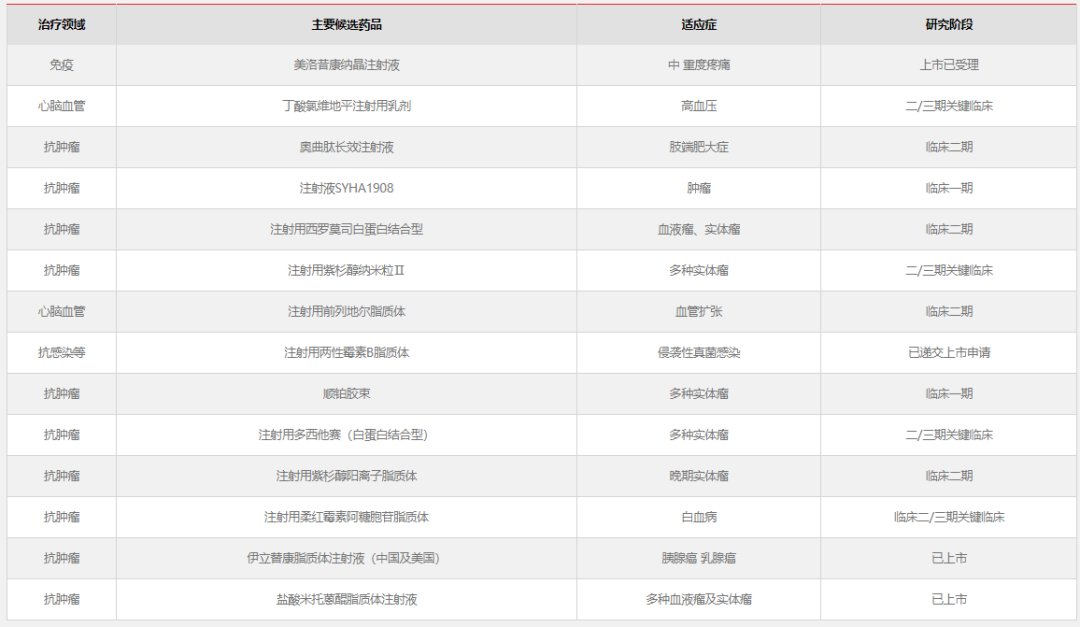
图片来源:石药集团
DBPR108
普卢格列汀(DBPR108)是一款DPP-4抑制剂,其用于治疗2型糖尿病的上市申请于2023年4月获得了国家药监局受理。今年1月,DBPR108片单药治疗2型糖尿病的III期临床研究成果被Diabetes, Obesity and Metabolism期刊接收并公示,据报道,DBPR108在该研究中展现了良好的降糖疗效和优异的安全性。
SYH2053
SYH2053由石药集团自主研发,是一款PCSK9 siRNA药物,通过偶联乙酰半乳糖胺(GalNAc)实现肝脏靶向递送。2023年11月,SYH2053的临床试验申请获得NMPA批准,适应症为成人原发性高胆固醇血症或混合型血脂异常。石药集团表示,该产品是其首 个获批临床试验的siRNA产品。
TG103
TG103是一款创新型重组人源胰高血糖素样肽-1(hGLP-1)Fc融合蛋白,石药集团以约1.5亿元从天境生物引入。据了解,TG103的分子设计具有延长GLP-1在体内的半衰期的特点,临床研究显示该药物有望实现每周一次或每两周一次的皮下给药,很大程度上改善患者的依从性。
03
结语
日前,石药集团进行了2023年创新回顾,全年研发费用达到48.3亿元,约占成药业务收入18.8%。通过持续加大研发投入、加强创新力度,石药集团有望在2024年迎来更多创新成果。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57