https://www.cphi.cn 2023-10-11 12:20 来源:CPHI制药在线 作者:江湖之远
近日,中国国家药监局药品审评中心(CDE)官网最新公示,Incyte公司递交的1类新药INCB099280片获得临床试验默示许可,拟用于晚期实体瘤患者的治疗。公开资料显示,这是一款小分子PD-L1抑制剂,目前已在海外进展至2期临床试验阶段。

INCB099280是一种选择性的小分子口服PD-L1抑制剂,已在实体瘤患者中显示出良好的临床活性和安全性。根据ClinicalTrials官网,目前INCB099280正在开展多项临床试验,包括:联合CTLA-4抑制剂伊匹木单抗治疗某些实体瘤的1期研究;治疗晚期皮肤鳞状细胞癌患者的2期研究;治疗免疫检查点抑制剂阴性的选定实体瘤的2期研究等。
小分子PD-L1抑制剂全球研发进展
自首 个PD-1--Opdivo于2014年获FDA批准上市后,截止目前,中国也已有10款PD-1抑制剂、4款PD-L1抑制剂上市。PD-1/L1抗体可以说是目前癌症靶向药物研发中的"过热"赛道。
值得注意的是,目前ICI疗法以单克隆抗体药物为主,其高昂的治疗费用也往往让很多患者望而却步。与单克隆抗体相比,小分子抑制剂除了口服更方便之外,还具备半衰期短、制备工艺简单、价格较低、有效穿透血脑屏障、更易进入肿瘤微环境等优势。因此,越来越多的研究人员在探索小分子化学药作为PD-1/L1抑制剂以规避治疗性抗体的缺点。另一方面,靶向PD-L1的药物开发备受追捧,在靶点同质化、治疗性抗体如此严重的今天,若想针对此靶点有所作为。或许,靶向PD-L1小分子抑制剂的开发可以找到破局之路。
目前国内 PD-L1 小分子抑制剂已有7款进入临床。此外根据已公开专利信息,还有多家企业处于临床前研发阶段,包括微芯生物、东阳光药、圣和药业等。
国内临床阶段 PD-L1 小分子抑制剂
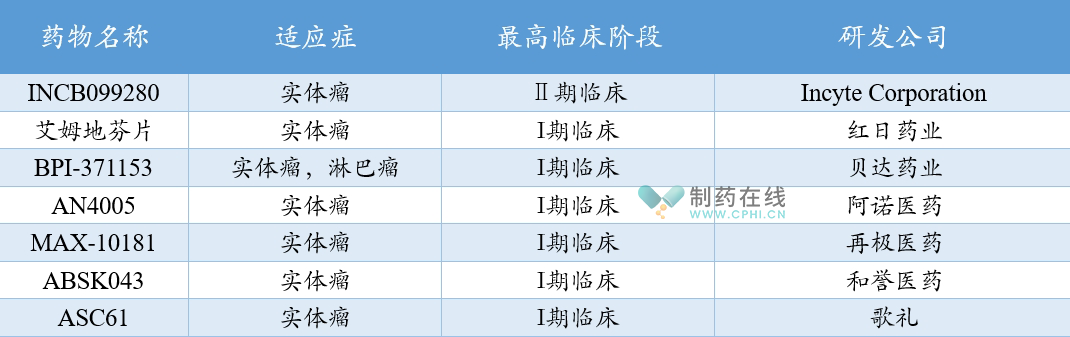
艾姆地芬片
2019年11月14日,红日药业发布公告称,其小分子口服PD-L1抑制剂艾姆地芬片(IMMH-010)于近日收到国家药监局下发的临床试验通知书,同意其进行临床试验,这是国内首 个获临床试验批准的口服PD-L1小分子抑制剂。该研究计划入组96例恶性实体瘤患者,评估艾姆地芬60、120、240、360mg治疗恶性实体瘤的安全性和耐受性,确定艾姆地芬的最大耐受剂量和II期推荐剂量,同时评估食物对晚期实体瘤患者的药代动力学影响。
BPI-371153
2021年11月12日,国家食品药品监督管理局(CDE)承办了贝达药业1类新药 BPI-371153胶囊的临床申请。BPI-371153是由贝达药业自主研发的新分子实体化合物,属于新型强效、高选择性的口服PD-L1小分子抑制剂。拟用于局部晚期或转移性实体瘤或复发/难治性淋巴瘤患者的治疗。临床前数据显示,BPI-371153可有效诱导和稳定PD-L1二聚体的形成及内吞,从而强有力地阻断PD-L1/PD-1相互作用。临床前研究中展现出优秀的体外及体内活性、良好的安全性及药代动力学性质。
AN4005
2021年10月11日,药审中心承办了杭州阿诺生物1类化药AN4005片的临床申请。AN4005片是阿诺医药全新研发的口服小分子PD-L1抑制剂,在去年5月20日,阿诺医药宣布向FDA递交了AN4005的临床试验申请,将于美国启动药物安全性和药代动力学评估的临床I期试验。临床前研究显示,AN4005具备出色的体外活性和强大的抗肿瘤活性,可有效诱导和稳定PD-L1二聚体的形成及二聚化,从而有力地破坏PD-1/L1蛋白质间的相互作用。同时,AN4005也表现出良好的成药性和安全性。
MAX-10181
2021年2月1日,CDE 官网显示,再极医药1类新药 MAX-10181 片首次在国内获批临床,用于晚期实体瘤。MAX-10181 是一款口服 PD-L1 抑制剂,此前已在澳洲启动 I 期临床。在2019年美国癌症研究协会的年会(AACR)上, 再极医药公布了MAX-10181在人源化的肿瘤模型中与阿斯利康PD-L1度伐利尤单抗的头对头比较数据。在两次试验中,MAX-10181与度伐利尤单抗都表现出相同的MC38肿瘤抑制活性,同时MAX-10181表现出了更高的 CD8+/Treg 比值(p<0.01)。
ABSK043
2022年4月1日,和誉医药自主研发的创新口服小分子PD-L1抑制剂ABSK043的临床试验获得NMPA临床研究许可。ABSK043可与PD-L1特异性结合并诱导其从细胞表面内吞,有效地抑制PD-1/PD-L1的相互作用,恢复PD-L1介导的T细胞活化抑制。ABSK043在多个临床前模型中展现出与已获批PD-L1抗体相当的强大抗肿瘤功效。ABSK043此前已在澳大利亚开展针对实体肿瘤的I期临床试验。
ASC61
2022年11月17日,歌礼制药自主研发的口服PD-L1小分子抑制剂ASC61获NMPA批准开展用于治疗晚期实体瘤的新药临床试验(IND)申请。ASC61美国I期剂量递增研究正在有序进行,中国IND获批将加速ASC61全球开发。ASC61是一款强效、高选择性的口服PD-L1小分子抑制剂,可以在体内代谢活性代谢物ASC61-A,通过诱导PD-L1二聚体的形成和内吞,从而阻断PD-1/L1的相互作用。ASC61单药在人源化小鼠模型等多种动物模型中表现出显著的抗肿瘤疗效。临床前研究显示,ASC61在动物模型中有良好的安全性和药代动力学特征。
总语
由于小分子药物特异性较差,可能存在多种靶标,因此后续应当对小分子PD-L1副作用展开更加广泛且深入的研究。但是,考虑到小分子药物制作成本较低、便于肿瘤渗透、可口服用药等优势,我们期待INCB099280这类小分子能够在后续的临床试验中保持较高的治疗效果,为广大癌症病人提供一款经济型、实用型、安全型的抗癌药。
参考来源
1. Imai K, Takaoka A. Comparing antibody and small-molecule therapies for cancer. Nat Rev Cancer. 2006;6(9):714-727.
2. Guzik K, Tomala M, Muszak D, et al. Development of the Inhibitors that Target the PD-1/PD-L1 Interaction-A Brief Look at Progress on Small Molecules, Peptides and Macrocycles. Molecules. 2019;24(11):2071. Published 2019 May 30.
3. Shaabani S, Huizinga HPS,Butera R, Kouchi A, Guzik K, Magiera-Mularz K, Holak TA, D?mling A. A patent review on PD-1/PD-L1 antagonists: small molecules, peptides, and macrocycles (2015-2018).Expert Opin Ther Pat. 2018 Sep;28(9):665-678.
4. CDE官网
5. 各企业官网
版权所有,未经允许,不得转载。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030