https://www.cphi.cn 2023-03-13 14:49 来源:CPHI制药在线 作者:小泥沙
近期,由诺如病毒(NoV)感染导致的病毒 性胃肠炎进入高发期,引起全民广泛关注。上篇,我们介绍了抗诺如病毒相关靶点药物。这篇,我们着重介绍诺如病毒的检测及其疫 苗研发进展情况。
诺如病毒的检测
科学检测是诺如病毒防控管理的基础,能够准确地为患者病情评估奠定基础,提高疾病处置能力。目前 NoV 检测方法主要有电镜法、核酸检测法和蛋白质检测技术。电镜法为NoV最早检出的方法,其灵敏度相对较低,故标本中病毒的检测范围须≧106才可检出,另外,对操作技术也要求较高,所以不适用于临床诊断。
核酸检测是常见的检测技术之一,是 NoV 检测的主要方法及金标准,具有较高的应用价值。核酸扩增法包括常规 RT-PCR 检测、多重 RT-PCR 检测、荧光定量 PCR 技术和环介导等温扩增技术。常规 RT-PCR 检测是在临床检测技术应用过程中以逆转录 PCR识别为主形成的一种检测技术,能够满足患者的检测需求,在检测过程中,能有效的评估患者病情。杂交技术和逆转录聚合酶链反应(RT-PCR)不仅能更准确、灵敏地检测标本中低浓度的NoV感染,还可以进一步对病毒进行基因型的研究,不会受到获得分型单克隆抗体的限制,对流行病学研究具有重要意义。多重RT-PCR 检测敏感性更高,特异性更强,检测速度更快,应用于临床检测工作中,对提高诊断质量有积极作用。多重RT-PCR 技术是在同一个 PCR 反应体系中加入多对引物以检测不同类型或亚型的病毒,它可以同时检测多种不同型别的病毒,减少反应次数,节约时间,但该方法灵敏度较低,因此需要优化 PCR 反应条件来尽可能减少非特异扩增。荧光定量PCR技术借助探针技术对NoV的分布情况作出分析评价,能够在诊断过程中通过荧光定量PCR 检测技术对病毒的传播形式及病毒载体进行识别,提高临床疾病诊断准确率。环介导等温扩增技术是一种以基因扩增技术为基础的新型检测技术,具有简单、快速及超高的灵敏度,该技术应用能够满足患者诊断工作实际需求,具有广泛的应用前景,尤其是对于欠发达或偏远地区的临床诊断和传染病监测具有重要的作用。此外,基因芯片技术是一种大规模集成的固相杂交技术,其基本原理是以核酸分子杂交即依据 DNA 双链碱基互补配对、变性和复性的原理,以大量已知序列的寡核苷酸、cDNA 或基因片段作为探针,检测样品序列及其互补序列,然后通过检测系统对杂交信号进行检测,可定性或定量检测,与传统基因诊断技术相比,DNA 芯片技术具有微型化、高通量、高度平行性和高速性的特点。
蛋白质检测技术也是NoV检测过程中常用的检测技术之一,可以有效识别病毒载体,对病毒的追踪有一定意义。蛋白质检测方法的原理主要是利用NoV特异性单(多)克隆抗体与标本中NoV衣壳抗原特异结合而进行检测,目前利用该技术的检测试剂盒已被临床广泛应用。该方法的灵敏度和特异性与抗原和抗体的差异性有关,目前较常用的免疫学方法包括 ELISA 技术和免疫胶体金技术等。此外,免疫层析技术结合了免疫亲和作用及层析技术,可用于快速检测NoV,具有节约时间,操作方便的优点,因此广泛用于临床检测。
诺如病毒的疫 苗研发
目前针对NoV引发的疾病尚无有效的治疗和预防手段,因此对于易感人群以及群发性感染,研发相关疫 苗是必不可少的。由于未找到合适的细胞系对NoV 进行体外培养,灭活和减毒疫 苗的研发受到极大限制,但随着基因工程技术的发展,基于NoV重组抗原的基因工程疫 苗进人了人们的视野。目前主要研发了基于P 颗粒、病毒样颗粒(VLPs)和重组腺病毒载体的 NoV 候选疫 苗。
1、NoV P 颗粒疫 苗
P 颗粒是由RGD4C 肽修饰的P结构域( P domain, PD) 二聚化并进一步聚集形成,具有真实组织血型抗原(HBGA)受体结合特性,可在大肠埃希菌中大量表达,生产简单,成本低。VP1蛋白中的P结构域可以在体外自发组装形成亚病毒颗粒P颗粒,该颗粒由12个P结构域二聚体组成,P 结构域的环状结构经自我组装后存在于颗粒的外表面,适合外源抗原的插入与展示,所以 P 颗粒不仅可以作为载体递呈外源抗原,也可以作为NoV疫 苗抗原。P 颗粒形态和大小与 NoV 差距较大,免疫原性可能较真实的病毒粒子低。但有研究发现,P颗粒和VLPs 均能很好地被树突状细胞( dendritic cell, DC)递呈,体液免疫和细胞免疫的免疫原性相似,且鼻内接种 NoV P 颗粒疫 苗对 NoV 急性胃肠炎具有交叉保护作用,保护效力与VLPs 疫 苗相当,所以 P 颗粒仍可作为一种良好的候选疫 苗。
联合疫 苗不仅提高了免疫效率,还降低了成本,是P颗粒疫 苗较VLPs 疫 苗的另一大优势。研究显示,大肠埃希菌系统表达的P 颗粒嵌合疫 苗包含NoV G II. 4和RV中和抗原VP8、可以诱导针对RV VP8以及NoV P抗原的强烈免疫应答,并且保护小鼠免受RV感染。此外,NoV P颗粒分别与流感病毒、戊型肝炎病毒组成二联疫 苗,与戊型肝炎病毒以及星状病毒组成三联疫 苗,免疫BALB/c小鼠后均可以引起免疫应答。同时,这些免疫血清阻断NoV 与HBGA结合的效率也更高。这些疫 苗免疫结果表明,P 颗粒可以用作预防NoV及相关病毒的候选疫 苗成分。
2、 NoV VLPs 疫 苗
VLPs保留了与人类组织血型抗原(HBGA)结合的能力、病原相关分子模式以及高密度B细胞和T细胞表位,可以诱导强烈的体液以及细胞免疫应答。目前用于表达NoV VLP的表达系统主要转基因植物、酵母和各种病毒载体,如杆状病毒、新城疫病毒(NDV)、水疱性口炎病毒(VSV )、委内瑞拉马脑炎病毒(VEE )及甲病毒等。
研究发现,BALB/c小鼠口服转基因植物(马铃薯、番茄和烟草)表达的NoV VLP后,可以检测到特异性血清Ig G以及分泌型IgA,在此基础上将烟草表达系统进行优化,可使表达的GI和GⅡ.4VLP产量增加到毫克级。用表达GⅡ.4 VLP的毕赤酵母提取物(0. 1 mgVLP,无佐剂)口服免疫BALB/c小鼠,可引起体液和黏膜免疫应答;以更高剂量(1 mgVLP )免疫时,免疫应答时间提前且更为强烈,相比于口服免疫,通过鼻内免疫VLP (无佐剂)更能刺激免疫应答,以大肠埃希菌不耐热肠毒素R192G突变体为佐剂更增强了免疫应答。将从芦荟中提取的惰性原位胶凝多糖干粉制剂与烟草表达的NoV VLP混合,制成干粉疫 苗鼻内免疫豚鼠,产生的抗体滴度不低于含佐剂的VLP疫 苗。
杆状病毒-昆虫细胞是最为常用的病毒载体表达系统。NoV和轮状病毒(RV)是引起幼儿病毒 性腹泻的主要病原体,而肠道病毒71 型(enterovirus 71,EV 71)是导致手足口病的主要病原体,有学者利用杆状病毒载体研发了 NoV (G II.4)和 EV71二联疫 苗以及NoV(G I .3 和GⅡ.4)和 RV (VP6)二联疫 苗。将NoV (G II.4)和 EV71各 5μg VLP 疫 苗经腹腔注射免疫BALB/c小鼠,可引发长时间的抗 GII.4NoV和EV71免疫应答,且抗体滴度与2种疫 苗单独免疫后诱导的滴度相当。动物实验结果表明,NoV 和RV二联疫 苗诱导了强烈的免疫应答,在动物体内检测到了高水平的血清特异性抗NoV 和RVIgG以及IgA 抗体,这些特异性抗体效价在6 个月内保持恒定水平。同时,血清特异性抗NoV 抗体可以阻断VLP与HBGA的结合,具有中和NoV的作用。联合疫 苗免疫原性研究表明,NoV与EV71和RV疫 苗不同抗原之间均没有免疫干扰,可以作为良好的候选疫 苗。
与杆状病毒载体表达的VLP相比,重组水疱性口炎病毒(VSV)和新城疫病毒(rVSV 、rNDV)作为载体表达的NoV VLP可以在BALB/c小鼠体内诱导更强的体液和细胞免疫应答。rNDV载体主要诱导针对Th1应答的IgG2a 亚类抗体,具体表现为在脾细胞中检测到高水平的IFN-γ、TNF-a 和IL-2。与之类似的是,接种委内瑞拉马脑炎病毒(VEE)和甲病毒载体表达的NoV VL P也导致了小鼠特异性全身和黏膜免疫应答。
3、NoV 重组腺病毒载体疫 苗
肠道上皮细胞是NoV的自然宿主细胞,NoV 口服疫 苗可引起肠内局部黏膜免疫反应,防止病毒感染。美国 Vaxart制药公司利用其成熟的腺病毒载体口服疫 苗研发平台,研制出了一种由表达GI. 1 NoV VP1基因的非复制型腺病毒载体和双链 RNA 佐剂组成的片状疫 苗,单次免疫后能有效诱导效应性和记忆性 B 细胞黏膜免疫,在免疫后6个月,粪便IgA 反应仍较高,HBGA阻断抗体水平增加,疫 苗安全且耐受性良好。继而,Vaxart 公司研发出了GII.4 单价口服疫 苗和GI. 1/GII. 4 联合疫 苗,其1b 期临床试验结果显示该二价疫 苗具有良好的耐受性,在大多数接种者中诱导产生了强 IgA 反应,且互不干扰。中国疾病预防控制中心病毒病预防控制所借助重组腺病毒表达载体研发的 GII. 4单价疫 苗,可有效激发小鼠全身、黏膜和 Th1 / Th2 细胞免疫应答。且先用重组腺病毒疫 苗免疫再用 VLPs 加强免疫的小鼠比先用 VLPs 免疫再用重组腺病毒疫 苗免疫或者只用 VLPs 多次重复免疫的小鼠产生的体液、黏膜和干扰素-γ反应更强,提示调整不同形式疫 苗之间的组合免疫顺序也是提高免疫效果的一个重要思路。
查阅相关网站,目前,我国进入临床阶段的NoV VLP疫 苗有2个,分别为兰州生物制品研究所有限责任公司研制的重组诺如病毒双价(GI. 1/GII. 4)疫 苗和安徽智飞龙科马生物制药有限公司的四价重组诺如病毒疫 苗,目前均处于II 期临床试验中。具体情况如下表所示。
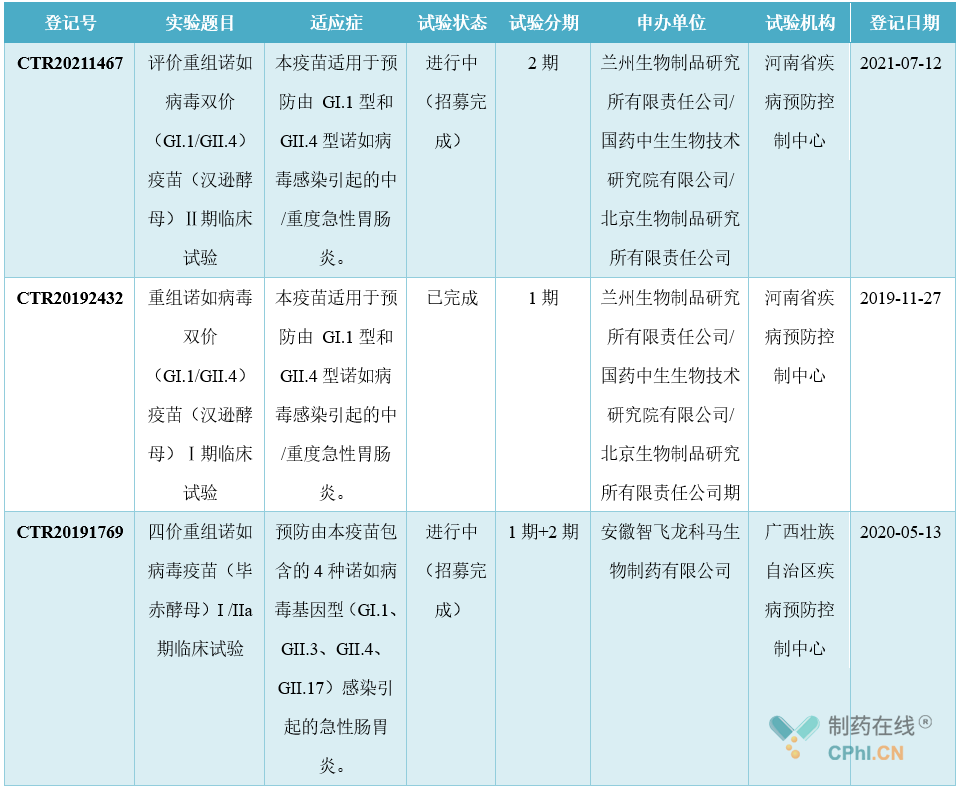
NoV疫 苗研发难度大,主要受制于 4 个方面的因素。其一是NoV有着极高的原漂变率,每两三年就会有一个新的流行优势毒株,不同流行株间交叉保护力弱。其二是常用的细胞株均不能感染或扩增NoV,仅 B 细胞和肠道类器官细胞模型可以检测到后代NoV的扩增,但培养条件极为复杂且成本昂贵。其三是缺乏一个简便且标准化的动物模型,可适用于所有人类NoV的感染及疫 苗的评价。其四是临床受试者招募难度大,受试者易感性影响试验结果,免疫效果不突出。尽管NoV 疫 苗的研发面对的困难较多,但随着分子检测技术的不断进步和体外感染模型的逐步完善,相信一定能够研制出一种安全、有效且可持续的NoV疫 苗。
参考资料
[1]王颖. 诺如病毒检测技术研究进展[J]. 中国城乡企业卫生, 2022, 37(6):3.
[2]李志凯, 苏国成, 苏文金,等. 诺如病毒检测方法研究进展[J]. 微生物学通报, 2014, 41(7):8.
[3]张巧玲. 人诺如病毒疫 苗及治疗药物的研究进展[J]. 国际生物制品学杂志, 2019, 042(005):239-246.
[4]何菲, 沈永明. 诺如病毒相关研究进展[J]. 中国城乡企业卫生, 2022, 37(8):3.
[5]赵璐, 段招军. 诺如病毒疫 苗研究进展和挑战[J]. 中华实验和临床病毒学杂志, 2022, 36(5):5.
作者简介:小泥沙,食品科技工作者,现就职于国内某大型药物研发公司,从事营养食品及功能性食品的开发与研究。
版权所有,未经允许,不得转载。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030