https://www.cphi.cn 2018-04-17 10:29 来源:药明康德
4、CAR-T疗法的**
接受ACT治疗后,T细胞活化会产生免疫刺激和炎症反应。目前,靶向CD19、BCMA和CD22的CAR-T细胞疗法都出现过严重的细胞因子释放综合征(CRS),比用TIL和TCR治疗出现的流感样综合征更加严重。CAR-T细胞疗法带来的CRS与肿瘤负荷相关。
此外,靶向CD19和BCMA的CAR-T细胞曾报道过意外神经系统并发症。其中CD19 CAR-T细胞疗法产生的神经**大部分可逆,但目前还不清楚脑水肿是CRS引起的还是另外有作用机制。目前,研究人员对于T细胞免疫疗法导致的CRS和脑水肿的机制仍不清楚。
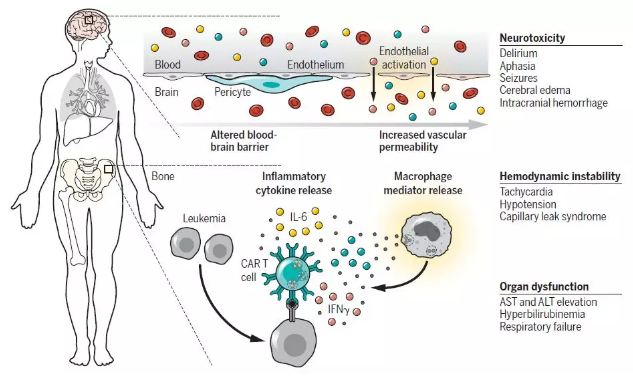
▲CAR-T细胞疗法的副作用:细胞因子释放综合症和神经**(图片来源:《科学》)
5、通用型CAR-T疗法
尽管ACT疗法属于异基因骨髓移植,但由于MHC的原因,ACT疗法目前仍集中在自体T细胞。如果可以消除MHC障碍,就能够实现同种异体T细胞治疗。与自体T细胞疗法相比,通用型CAR-T细胞来源于健康供体,有可能克服许多与癌症治疗相关的免疫缺陷;另外,通用型CAR-T细胞疗法的制造工艺更加简化,有望实现更快速、更便宜的“现成(off the shelf)”细胞疗法产品。
最近,一项采用TALEN(转录激活因子效应物核酸酶)基因工程化改造的细胞在两名患者身上进行了试验,结果证明了现成的CD19 CAR-T细胞疗法的可行性。但基因通用型CAR-T细胞的移植在两个受试者中都受到限制,减弱了疗法的有效性。重要的是,受试者1的所有MHC I等位基因发生错配,导致了移植物抗宿主病。这意味着完全的基因编辑对于该疗法的成功至关重要。另外,自然杀伤(NK)细胞对MHC I类缺陷细胞的识别也可能限制了移植。防止NK细胞溶解通用型CAR-T细胞的一种方法是插入HLA-E并删除HLA-A,-B和-C,这样可以阻止宿主T细胞杀死通用型CAR-T细胞。
由于该领域的快速发展,通用型CAR-T细胞可能得到广泛应用。然而,问题是它到底能作为单药疗法还是(例如干细胞移植或自体CAR-T细胞治疗的)辅助疗法。
6、基因编辑和多功能CARs
有许多基因编辑工具,包括锌指核酸酶(ZFNs),归巢核酸内切酶(meganucleases),TALENs和CRISPR-Cas9核酸酶。这些技术已经成功应用于工程化T细胞研究。现在该领域的主要问题是源自细菌的Cas9的免疫原性是否会影响CRISPR-Cas9基因编辑的T细胞的药物输送。
基因组编辑有可能用来解除CTLA-4和PD-1等免疫抑制信号,增强T细胞的功能,同时避免全面阻断免疫检查点分子带来的相关**。基因编辑也可以用于敲除T细胞表达的CAR靶点的基因,使得靶向不适用于T细胞免疫疗法的抗原成为可能。最近,研究者将CAR引入TCR基因座,可以在内源性TCR启动子的条件下控制受体表达,从而显着增强CAR-T细胞功能。
为了减少与ACT的自身反应性免疫的潜在风险,研究人员已经开发了使基因工程T细胞诱导性死亡的合成分子系统,通常称为“自杀开关”。最有名的方法是用促凋亡蛋白caspase-9与FKBP12(iCasp9)的结构域融合。在引入二聚体小分子例如利米德凝胶时,iCasp9的FKBP12结构域二聚化,使得T细胞经历快速凋亡性细胞死亡。在造血干细胞移植后的同种异体淋巴细胞输注中评估了iCasp9方法的试验,已经证实了强大T细胞消除能力,避免移植物抗宿主病。
7、CAR-T的推广之路
目前,全球有250多个关于CAR-T细胞的临床试验研究。其中,中国和美国是两大热门地区,欧洲、日本和南半球的临床试验数量要少得多。这与接受和投资新兴疗法的意愿,卫生监管政策以及社会差异都相关。
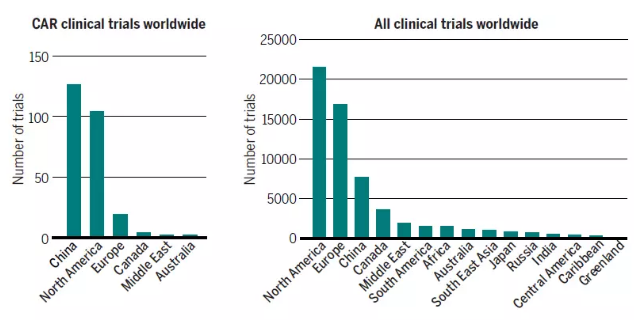
▲CAR-T细胞疗法临床试验的全球分布(图片来源:《科学》)
血液癌症患者,特别是CLL和多发性骨髓瘤患者接受有效、但不能治愈的疗法带来的经济负担也是一大挑战。CLL是美国最常见的白血病形式,2000年约有100,000名患者,而且目前的疗法都只能改善生存状况,并不能治愈。因此给患者带来了巨大的经济负担。据估计,每名患者的终生治疗费用为604,000美元,到2025年,美国的CLL的医疗费用估计超过50亿美元/每年。
CAR-T细胞治疗可能比现有的标准疗法更具成本效益。目前高度个体化的T细胞疗法的工艺需要定制,由此带来高成本。但随着工艺的成熟,制造成本会有所下降。
8、未来机会与挑战
治疗白血病和淋巴瘤的CAR-T细胞疗法的出现值得关注,有多个方面的原因。也许最重要的原因是,CAR-T是经美国FDA批准的第一种获得推广的基因疗法。
目前,开发细胞疗法的挑战之一是缺乏可以评估这些复杂疗法的安全性和有效性的临床前模型,或者是对早期临床研究中发现的安全问题的应对措施。另外,在治疗实体瘤方面仍然存在许多障碍。
值得期待的是,由于工程化T细胞、基因编辑和细胞制造领域的技术进步,未来基于T细胞的疗法有望扩大到其他细胞类型,如诱导多能干细胞、造血干细胞和NK细胞;适应症也会超越癌症,有望用于传染性疾病、器官移植和自身免疫性疾病等各类疾病。
参考资料:
[1] CAR T cell immunotherapy for human cancer
如果这篇文章侵犯了您的权利,请联系我们。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030