https://www.cphi.cn 2021-09-28 10:14 来源:CPhI制药在线 作者:zhulikou431
目前新冠疫情在全球持续肆虐蔓延,呈现全球大流行的明显趋势;而另外一方面病毒变异情况严重,近期出现了多种危险变异病毒,如缪(Mu)毒株、德尔塔(Delta)变异株、Gamma变异毒株等。如果要论全球抗疫最关键环节,毫无疑问就是多种新冠**的研制成功并积极实施商业化生产。因此,我们迫切需要更多更有效的**问世。
根据WHO官网提供的最新数据,截止至2021年9月21日,目前处于临床研究阶段的**121种,处于非临床研究阶段的有194种。(详见图1)
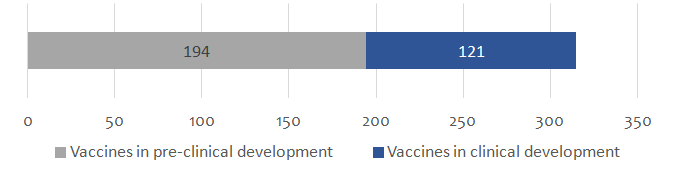
图1 全球候选**数量(图片来源WHO官网)
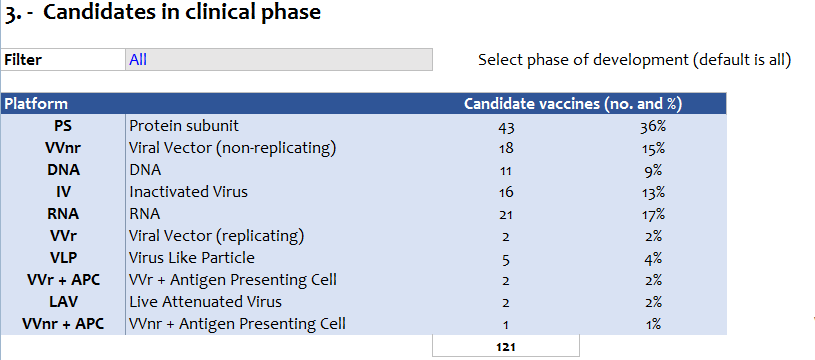
图2 处于临床研究阶段的新冠**种类(图片来源WHO官网)
另外,根据WHO的分类,处于临床研究阶段的候选新冠**一共分为10类(详见图2),按照大类分为以下几种:①减毒**、②灭活**、③蛋白亚单位**、④病毒载体**(复制/非复制/抗原提呈细胞参与)、⑤核酸**(mRNA、DNA)、⑥病毒样颗粒**,其中重组蛋白**类**所占的比例最高(达36%)。
FDA批准或紧急授权使用的新冠**
FDA目前批准或紧急授权使用了三款新冠**,其中辉瑞的**刚刚在2021年8月份正式得到完全批准,用于 16 岁及以上的人群;辉瑞的新冠**是2020 年 12 月首次获得FDA紧急使用授权的(EUA)。

欧盟批准的新冠**
欧盟目前附条件批准了四款新冠**,其中辉瑞和Moderna的两款为核酸(mRNA)**,阿斯利康和强生制药公司的两款为非复制病毒载体**。

列入WHO紧急使用清单的新冠**:
目前,已被列入世卫组织紧急使用清单的**包括,辉瑞/生物科技(Pfizer-BioNTech)**、 阿斯利康(AstraZeneca, AB)**、印度血清研究所 (Serum Institute of India Pvt. Ltd) **、强生(Janssen-Cilag International NV)**、Moderna Biotech**,以及我国的北京科兴中维生物和国药北京生物的新冠**。
国内**批准情况:
目前我国已有7款国产**获批附条件上市或开展紧急使用,并且积极同10多个国家开展**研发合作,新冠**的研发在全球处于领先地位:
◆北京生物制品研究所的新型冠状病毒灭活**(Vero细胞)于2020年12月30日附条件上市;
◆武汉生物制品研究所的新型冠状病毒灭活**(Vero细胞)于2021年2月25日附条件上市;
◆北京科兴中维生物技术有限公司的新型冠状病毒灭活**(Vero细胞)于2021年2月5日附条件上市;
◆康希诺重组新型冠状病毒**(5型腺病毒载体)于2021年2月25日附条件上市;
◆安徽智飞生物重组蛋白新冠**于2021年3月10日获得国内紧急使用批准;
◆康泰生物新型冠状病毒灭活**(Vero细胞)于2021年5月14日获得国内紧急使用批准;
◆中国医学科学院医学生物学研究所新型冠状病毒灭活**(Vero细胞)于2021年6月9日获得国内紧急使用批准。
新冠**研发新进展
2021年9月9日,Moderna公司宣布研发一针六靶mRNA增强**。该**是将Moderna目前的新冠**和一种也正在研发的流感**结合研制出的,可以同时防御新冠病毒和季节性流感病毒。
2021年9月22日晚,三叶草生物制药有限公司和流行病防范创新联盟 (CEPI) 共同宣布, 三叶草生物联合佐剂使用的重组蛋白新冠候选**SCB-2019 (CpG 1018/铝佐剂)在全球关键性2/3期临床试验 ("SPECTRA" )达到保护效力的主要和次要终点,对任何毒株引发的任何严重程度的总体保护效力为67%。目前三叶草生物已获得浙江省药品监督管理局签发的用于新冠**的《药品生产许可证》。
2021年9月22日晚沃森生物发布公告,公司与艾博生物合作研发的新型冠状病毒mRNA**于近日获得了尼泊尔药监部门颁发的Ⅲ期临床试验批件,标志着新型冠状病毒mRNA**在尼泊尔进入Ⅲ期临床试验阶段。
另外,康希诺的吸入式重组新冠病毒**(腺病毒载体),正在向国家药监局申请紧急使用授权;中科院微生物所与智飞生物正在推进二代重组**的研发;国药集团中国生物也在加速一款mRNA核酸**的研发。据最新媒体报道:9月25日,国药集团中国生物复诺健mRNA**产业化基地开工仪式在嘉定区南翔镇举行。国药集团中国生物复诺健mRNA**产业化基地位于南翔镇蕰北公路2111号,总建筑面积3.2万余平方米,生产车间将超过1.6万平方米,竣工投产后将成为国内产能、技术方面领先的mRNA**生产车间,打造低碳、节能、环保的mRNA**产业化基地。
总结
综上所述,面对突发的新冠疫情,世界各国**研发团队都积极投入并开展各项积极合作;同时,药政部门为了满足市场迫切的需求,在充分利用现有审评绿色通道政策的同时,还积极进行探索和尝试,为各类新产品研发和行业沟通,促进审评效率提高。中国医药行业经过改革开放以来的40多年发展,在**研发和生产领域积累的资源,不仅为中国抗疫工作起到保驾护航的作用,还积极为世界抗疫做出贡献。相信随着更多中国优秀公司的积极努力,中国医药行业会为世界呈现更多优秀新冠**产品。
参考资料:
1-WHO官网信息
2-FDA官网
3-EMA官网
4-NMPA官网
5-国药集团官网信息
作者简介:zhulikou431,高级工程师、PDA会员、ISPE会员、ECA会员、PQRI会员、资深无菌GMP专家,在无菌工艺开发和验证、药品研发和注册、CTD文件撰写和审核、法规审计、国际认证、国际注册、质量体系建设与维护领域,以及无菌检验、环境监控等领域皆具有较深造诣。近几年开始着力关注制药宏观领域趋势分析和制药企业并购项目的风险管理工作。
版权所有,未经允许,不得转载。
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030