目前,除了阿美替尼,三代EGFR-TKI还有进口的奥希替尼,国产的艾维替尼、BPI-7711等,这几种三代TKI相比,谁更优秀?今天我们比较一下。
 热门推荐:
奥希替尼
, EGFR-TKI
, 艾维替尼
, BPI-7711
, 阿美替尼
热门推荐:
奥希替尼
, EGFR-TKI
, 艾维替尼
, BPI-7711
, 阿美替尼
2019年7月,CDE受理承办了百时美施贵宝旗下纳武利尤单抗注射液新适应症的国内上市申请,涉及到两个受理号(JXSS1900037/ JXSS1900038),近日这两项申请已进入了"审批完毕-待制证"状态。
 热门推荐:
胃癌
, 免疫疗法
, 纳武利尤单抗
热门推荐:
胃癌
, 免疫疗法
, 纳武利尤单抗
从实验室药物发现到为临床实验提供样品,再到商业化大生产,达可替尼合成工艺的不断优化为其成功上市一路保驾护航。达可替尼合成工艺开发可大致分为三个阶段,第一阶段是对实验室药物发现的合成路线进行优化,作为早期工艺开发,第二阶段是N-芳基化路线的开发,第三阶段为经Dimroth重排反应,最终用于商业生产的后期工艺路线开发。
 热门推荐:
工艺开发
, Dacomitinib
, 达可替尼
热门推荐:
工艺开发
, Dacomitinib
, 达可替尼
在2020年3月12日国家药品监督管理局官网的药品批件发布通知中,由上海汇伦江苏药业研发的注射用西维来司他钠引起行业关注,其参股上市公司新天药业股票也随之涨停。
 热门推荐:
新冠肺炎
, 西维来司他钠
, 上海汇伦江苏药业
热门推荐:
新冠肺炎
, 西维来司他钠
, 上海汇伦江苏药业
近日,Immutep公司宣布,该公司的可溶性LAG-3融合蛋白eftilagimod alpha(efti,又名IMP321),与PD-1抑制剂Keytruda联用,在II期临床试验中获得积极中期结果。
 热门推荐:
肿瘤
, Immutep
, LAG-3
热门推荐:
肿瘤
, Immutep
, LAG-3
现代研究发现何首乌的有效成分主要有二苯乙烯甘(TSG)、蒽醌、大黄素、儿茶素、没食子酸、没食子酸酯等。其中TSG是何首乌中具有显著药理活性的水溶性有效成分。
 热门推荐:
何首乌
, 心血管系统
, 神经系统
热门推荐:
何首乌
, 心血管系统
, 神经系统
老药新用有很多介入契机,有的开发新的适应症,有的开发新的组合或者制剂形式,有的对药物结构形式进行修饰。在2019年大热的氘代茅台的故事,也在制药领域有所体现。本文汇总数据和信息,为各位制药同仁介绍中国氘代药物目前发展局面和形势。
 热门推荐:
研发
, 氘代药物
, 吉贝尔
热门推荐:
研发
, 氘代药物
, 吉贝尔
根据ClinicalTrials.gov上登记的信息显示,该研究为干预性研究,是一项开放、单臂的临床研究,计划纳入10名受试者。主要目的为在临床实际诊断和治疗条件下观察西地那非对COVID-19患者的疗效和安全性。
 热门推荐:
临床试验
, 西地那非
, 新冠肺炎
热门推荐:
临床试验
, 西地那非
, 新冠肺炎
2020年3月11日,国家药监局官网发布《药品上市许可持有人和生产企业追溯基本数据集》《药品经营企业追溯基本数据集》《药品使用单位追溯基本数据集》《药品追溯消费者查询基本数据集》《药品追溯数据交换基本技术要求》5项信息化标准,自2020年3月6日起实施。
 热门推荐:
药品管理法
, MAH
, 追溯系统
热门推荐:
药品管理法
, MAH
, 追溯系统
2020年03月11日,FDA加速批准纳武利尤单抗联合伊匹木单抗肝细胞癌二线新适应症,双肿瘤免疫疗法可使肝细胞癌患者CR 8%, PR24%,至此,纳武利尤单抗联合伊匹木单抗覆盖4种癌症。
 热门推荐:
Yervoy
, 肿瘤免疫疗法
, Opdivo
热门推荐:
Yervoy
, 肿瘤免疫疗法
, Opdivo
奥美替尼的上市申请在NMPA的状态变更为"在审批"状态,预示着奥美替尼有望早于艾维替尼在国内获批上市,成为国内首个获批的国产三代EGFR-TKIs。
 热门推荐:
NSCLC
, EGFR-TKI
, 奥美替尼
热门推荐:
NSCLC
, EGFR-TKI
, 奥美替尼
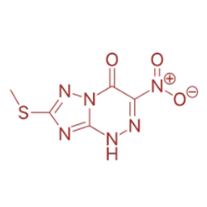
近日,新闻报道俄罗斯赠送中国一款俄罗斯研发的抗病毒 药三氮唑核苷(Triazavirin),正在测试其针对新型冠状病毒感染肺炎的效果。
 热门推荐:
利巴韦林
, 三氮唑核苷
, Triazavirin
热门推荐:
利巴韦林
, 三氮唑核苷
, Triazavirin
3月6日,AstraZeneca公布了其抗PD-L1疗法Imfinzi治疗膀胱癌III期Danube试验的最新进展,与标准护理化疗相比,Imfinzi单药或Imfinzi + tremelimumab联合疗法未能达到主要终点,无缘一线疗法。
 热门推荐:
膀胱癌
, Imfinzi
, Danube
热门推荐:
膀胱癌
, Imfinzi
, Danube
据EvaluatePharma预测,到2025年,全球NASH药物市场规模将达到400亿美元,如此庞大的市场,NASH江湖急需重磅炸 弹的来临。
 热门推荐:
研发
, NAFLD
, NASH
热门推荐:
研发
, NAFLD
, NASH
伊珠单抗奥唑米星(Inotuzumab Ozogamicin)是由辉瑞和优时比联合开发的一款抗体偶联药物(ADC),由靶向CD22抗原和单克隆抗体与一种细胞毒制剂卡奇霉素(calicheamicin)偶联而成,于2017年8月被FDA批准用于治疗复发或难治性前体B细胞急性淋巴细胞白血病(ALL),商品名为Besponsa。
 热门推荐:
优先审评
, ADC
, 伊珠单抗
, 奥唑米星
热门推荐:
优先审评
, ADC
, 伊珠单抗
, 奥唑米星
CDE官方网站显示,3月7日,恒瑞医药提交的10项临床申请均获得受理,这些申请涉及到1款治疗用生物制品及4款化药,且均为1类新药。
 热门推荐:
恒瑞
, 临床申请
, 1类新药
热门推荐:
恒瑞
, 临床申请
, 1类新药
动物试验,是任何药品研发的初步基础。在经历过动物试验后,人体试验未必就一定安全,但至少可以排除掉大部分风险。人体试验一期临床,检测的就是安全性。如果科学家把自己以身试药作为临床试验,对不起,这是不允许的。
 热门推荐:
临床试验
, 新冠**
, 以身试药
热门推荐:
临床试验
, 新冠**
, 以身试药
3月2日,美国FDA宣布,批准赛诺菲(Sanofi)公司开发的CD38抗体Sarclisa(isatuximab-irfc)上市,与泊马度胺(pomalidomide)和地塞米松(dexamethasone)联用,治疗成年多发性骨髓瘤(MM)患者。
 热门推荐:
赛诺菲
, 多发性骨髓瘤
, CD38抗体
, Sarclisa
热门推荐:
赛诺菲
, 多发性骨髓瘤
, CD38抗体
, Sarclisa
近日,印度制药企业Zydus Cadila旗下的Saroglitazar获得了印度药品管理局批准,用于非肝硬化性非酒精性脂肪性肝炎(NASH)的治疗。
 热门推荐:
非酒精性脂肪性肝炎
, NASH
, PPAR激动剂
, Saroglitazar
热门推荐:
非酒精性脂肪性肝炎
, NASH
, PPAR激动剂
, Saroglitazar
基石药业董事长兼首席执行官江宁军博士表示,CS3005的临床试验在澳洲获批体现了基石药业对迈向'管线2.0'的积极布局,期待通过对肿瘤微环境调节剂的探索与开发,能够扩大免疫治疗的获益人群。
 热门推荐:
基石药业
, CS3005
, A2aR拮抗剂
热门推荐:
基石药业
, CS3005
, A2aR拮抗剂
 报名 | ADC药物工艺开发和质量风险管理研习会
报名 | ADC药物工艺开发和质量风险管理研习会
 直播报名 | 制药行业日常仪器实验操作的安全、规范与维护
直播报名 | 制药行业日常仪器实验操作的安全、规范与维护
 直播报名 | 泛素化-蛋白酶体系统与药物研发
直播报名 | 泛素化-蛋白酶体系统与药物研发
 2024CPHI制药在线买家采购会邀您同启智慧采购之旅!
2024CPHI制药在线买家采购会邀您同启智慧采购之旅!
 2024制药产业线上主题展——天然提取物专场
2024制药产业线上主题展——天然提取物专场
投稿合作联系方式: Kelly.Xiao@imsinoexpo.com 021-33392297
地址:上海市徐汇区虹桥路355号城开国际大厦7-8楼 200030