近日,印度制药企业Zydus Cadila旗下的Saroglitazar获得了印度药品管理局批准,用于非肝硬化性非酒精性脂肪性肝炎(NASH)的治疗。作为一款PPARα/PPARγ的双重激动剂,Saroglitazar成为全球首个获批用于非酒精性脂肪性肝炎(NASH)治疗的药物。
NASH是一种严重的非酒精性脂肪性肝病,指的是酒精以外其它因素导致的肝细胞内脂肪过度沉积的病理综合征。据统计,在全球范围内,已经有10%-30%的人口受到该疾病的影响。根据德意志银行分析师曾做出的预测,2025年全球NASH治疗药物的市场将达到350~400亿美元的规模。这一肝病治疗细分市场的未来预期被普遍看好,属于潜在的价值高地,吸引了包括众多制药公司的参与。
PPARα/PPARγ双靶点激动剂Saroglitazar
Saroglitazar是一种过氧化物酶体增殖物活化受体(PPAR)激动剂,它同时具有调节PPARα和PPARγ活性的双重功能。在体内,Saroglitazar 作用于PPARα的降脂作用很明确,作用于PPARγ的降糖作用也很明确,PPARα/PPARγ是目前代谢领域最吸引人的一个机制。
2013 年9月,印度制药企业Zydus Cadila旗下的Saroglitazar在印度上市,用于治疗他汀类药物无法控制的血脂异常/高甘油三酯血症的II 型糖尿病患者。2020 年1月,该药的第二个适应症获批,扩大至II 型糖尿病患者治疗。
此次,Saroglitazar获批用于治疗非硬化性非酒精性脂肪性肝炎(NASH),属于新适应症的扩展。这次适应症扩展主要基于III 期临床试验EVIDENCES II的结果,在为期52周的观察期间,试验结束时以肝活检对NASH患者进行的肝组织学改善结果表明,治疗组的受试者达到了临床主要的终点和次要终点。
Saroglitazar尚在进行中的临床研究
除上述已获批的适应症之外,Saroglitazar目前尚有多项临床试验处于进行中,其中包括了4项II期临床及1项III期临床,适应症涉及到非酒精性脂肪性肝炎、患有非酒精性脂肪性肝炎的肝移植患者、原发性胆汁性肝硬化、患有多囊卵巢综合征的非酒精性脂肪肝女性患者。
从目前的进度来看,这些临床试验大多数将在2020年内完成,预计未来Saroglitazar仍将持续扩展新的临床适应症。
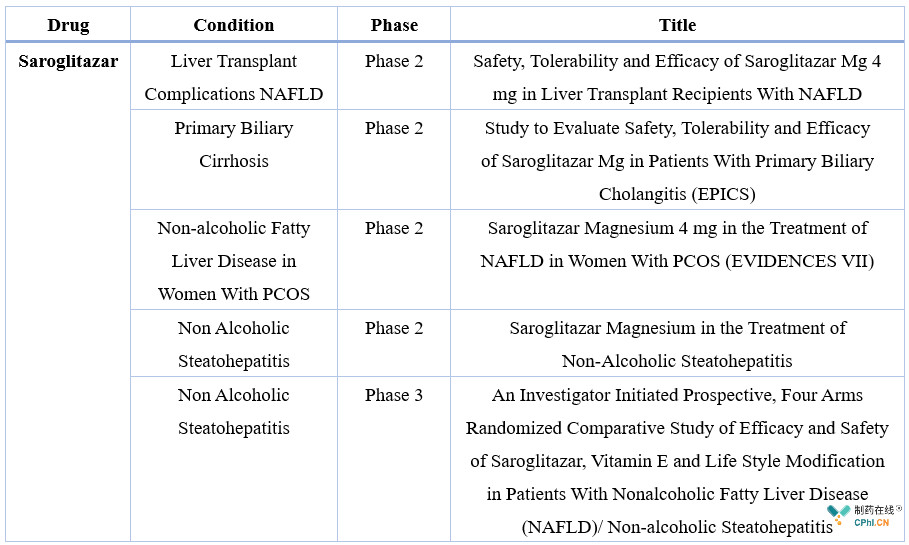
资料来源:ClinicalTrials
Saroglitazar化合物专利即将到期
据查询,Saroglitazar的化合物专利申请日为2002年7月,按照发明专利权20年的保护期限来计算,该化合物专利将在2022年到期。对于有意布局Saroglitazar仿制药的制药企业而言,准备工作可以早早开始了。

资料来源:NIPA
国内在研PPAR 激动剂类NASH治疗药物
在备战NASH治疗新药的竞赛中,目前国内有3家本土制药企业参与其中。
众生药业旗下一款用于非酒精性脂肪性肝炎(NASH)治疗的新药ZSP0678片已进入I 期临床试验阶段,该药物为PPARα/δ 双重激动剂。目前,ZSP0678片已经完成了4 个剂量组的单次健康人给药,I 期临床稳步推进。
在众生药业的NASH治疗药物在研管线中,2018年1月,1类化学小分子创新药ZSP1601片的Ⅰ期临床试验启动,用于非酒精性脂肪性肝炎(NASH)的治疗,这是国内首个进入临床阶段的在研非酒精性脂肪性肝炎(NASH)治疗新药。该试验在国内实际入组了94名受试者,目前已完成。众生药业已经启动了ZSP1601片的Ib/IIa期临床试验,拟招募36人,用于评价ZSP1601片在非酒精性脂肪性肝炎(NASH)患者的安全性、耐受性、药代动力学特征和早期药效,为ZSP1601片治疗NASH患者的进一步研究提供支持。ZSP1601片与ZSP0678片的作用机制不同,作用于NASH的不同病程阶段。
除了众生药业之外,泽璟制药旗下的在研产品ZG0588目前处于临床前研究阶段,预计将于今年申请IND,该在研药物为为PPAR α/γ 双重激动剂;2018年,拓瑧生物与 Genfit 签订了合作协议,获得了后者在研新药 Elafibranor在 NASH 和 PBC 等适应症的大中华区独家开发、注册和商业化权益。Elafibranor为 PPARα/δ 双重激动剂,是当前最受瞩目的NASH 新药之一,目前处于临床 III 期阶段,有望于近期公布中期结果。
作者简介:小药丸,制药行业从业者,自媒体时代的文字搬运工,专注于制药圈内的阴晴冷暖。
点击下图进行CPhI & P-MEC China 2020观众预登记抽奖,奖品多多!



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57