一、 简介
阿尔茨海默症是一种神经退行性疾病,主要特征表现为全面性的痴呆。在我国,大约有阿尔茨海默症患者1000万,居世界首位,且该数字还在不断攀升。该病是目前公认的较为难治的疾病,近20年来,几乎TOP10国际制药巨头都参与了该领域的药物研发工作,然而并没有成功的药物上市。面对这一"毁灭性"的疾病,之所以没有进展,很大一部分原因是因为学术界并没有阐明该病的发病机制,没有统一的观点,例如,在学术界关于该发病机制的有以下三种假说:1)遗传因素致病;2)β-淀粉样蛋白假说;3)tau蛋白假说。然而这些都处于假说阶段,目前尚无定论,由此可以看出,在基础科学领域没有完全阐明发病机制的前提下,药物研发将会变得异常艰难,很难取得成功。然而面对这一危害极大地疾病,人类并没有退缩,而是前仆后继、勇往直前。上个月,上海绿谷制药宣布,其联合中国海洋大学、上海药物所开发的药物"甘露寡糖二酸(GV-917)"已顺利完成Ⅲ期临床试验,标志着该药的研发工作已经突破了最关键的一步,朋友圈里竞相转发这一振奋人心的消息,希望该国产药能够上市,造福患者。本篇文章主要介绍的是获得FDA快速审批通道的处于Ⅲ期临床试验中表现优异的药物。
二、 药物介绍
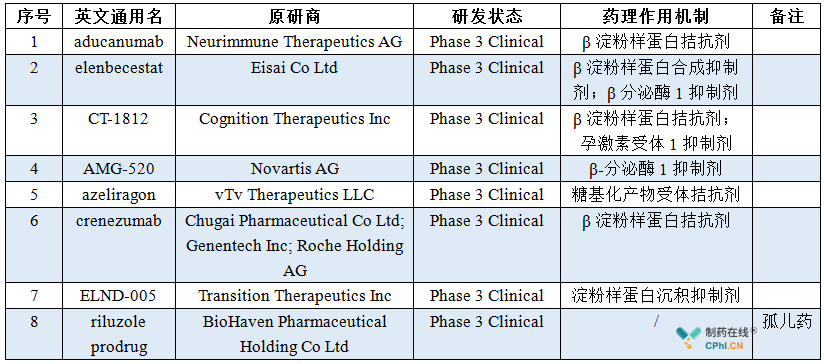
表1 全球抗阿尔茨海默症Ⅲ期临床试验药物
上表列举了8个进入FDA快速审批通道的药物,除了Azeliragon已经宣告暂停临床试验外,其他药物都被寄予厚望,有希望成为新一代阿尔茨海默症治疗药物,下面将逐一介绍。
1、 Aducanumab
该药由Biogen与Neurimmune联合开发,该药为单克隆抗体,是β淀粉样蛋白聚集体刺激B细胞产生的物质中筛选出来的能够特异性结合β淀粉样蛋白的分子。其可以通过靶向结合脑内淀粉样蛋白块,激活免疫系统,从而将沉积蛋白清理出大脑。被认为是最有可能成功的阿尔茨海默症治疗药物。2016年9月,《nature》杂志以封面文章报道了该药物在Ⅰ期临床中的积极效果,介绍了在Ⅰb期的随机、双盲、安慰剂对照等实验结果,每月静脉滴注一次该药,由于样本数量有限,不足以对试验结果做出过度解读,但是大量的临床前的动物实验,显示出该药对新形成和成熟的斑块均有效。同月,该药获得了FDA快速审批通道资格认定。其三期临床结果将于2019年或2020年左右完成。
2、 Elenbecestat
2014年,Eisai和Biogen联合开发的小分子药物Elenbecestat。在β淀粉样蛋白的形成过程中,有一个至关重要的酶--β淀粉样蛋白裂解酶(BACE),该药物正是通过抑制BACE,从而减少淀粉样斑块的形成,抑制或延缓疾病进展。该药于2016年9月获得了FDA快速审批通道资格认定。在2018年7月22~26日的阿尔茨海默病协会国际会议(AAIC)会议上,公布了该药详细的Ⅱ期临床研究结果,目前三期临床试验正在进行中,具体时间轴见下图:
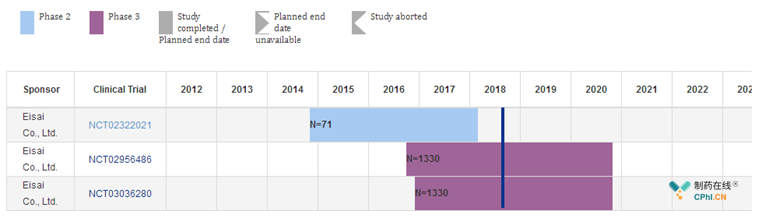
图1 Elenbecestat临床试验时间轴
3、 CT-1812
该药由Cognition Therapeutics公司开发,是一种全新的小分子药物,目前笔者仅查到了其研发代码,通用名尚不可知。该药物的作用机制较为新颖,它是通过抑制β淀粉样蛋白寡聚体与神经元受体的结合,从而降低β淀粉样蛋白对神经元的损害,使得突触得以再生,促进认知功能恢复。该药在2017年10月完成了临床Ⅰ、Ⅱ期试验,同期,获得了FDA快速审批通道资格。目前正在进行Ⅲ期临床研究。
4、AMG-520
由Novartis和 Amgen联合开发,也是一个小分子BACE抑制剂,作用机制与Elenbecestat类似,在2015年进行的Ⅰ、Ⅱ期临床试验,得到了较好的结果。2017年6月进行了随机、双盲、多中心的临床Ⅲ期试验,实验结果预计在2024年得到。
5、Azeliragon
该药物由vTv Therapeutics公司开发,晚期糖化终产物受体(RAGE)被认为在阿尔茨海默症中有着较为关键作用,该药是一种新型口服RAGE小分子抑制剂药物。该药也具有快速审批通道资格。然而其在2018年4月,得到的Ⅲ期临床试验并不理想,目前该公司已暂停临床研究,后期将全面评估该药物是否具有进一步开发的潜力。列举这个药物就是想说明,即使业界和监管部门都看好的药物,在其开发过程中,失败也是常见的事,在临床Ⅲ期试验中失败的抗阿尔茨海默症药物,比比皆是、不胜枚举。
6、Crenezumab
由Chugai Pharmaceutical和Genentech开发,为单克隆抗体药物,是β淀粉样蛋白抑制剂。在2018年7月22~26日的阿尔茨海默病协会国际会议(AAIC)会议上,其公布了Ⅱ期临床试验结果,表明Crenezumab能够优先结合β淀粉样蛋白并促进去除该物质,使脑脊液中β淀粉样蛋白质(Abeta)低聚体水平的持续下降,为疾病的治疗带来积极的作用。目前Genentech正在进行该药的两项Ⅲ期临床试验。
7、ELND-005
在前文中提到了我国自主研发的抗阿尔茨海默症药物--甘露寡糖二酸(GV-917),该类药物作用机制较为新颖,它可以抑制β淀粉样蛋白的形成,并且能够促进β淀粉样蛋白解聚,抑制β淀粉样蛋白的**。ELND-005是由Transition Therapeutics和Elan联合开发的糖类药物,作用机制与GV-917类似。该药于2013年获得了快速审批通道认定。
8、Trigriluzole
该药是利鲁唑的前药,为谷氨酸调节剂,BioHaven Pharmaceutical公司正在开发其用于治疗运动失调和阿尔茨海默症,不幸的是2017年10月运动失调的临床试验失败。在2017年9月开始了阿尔茨海默症的临床Ⅱ期试验。在2018年7月份开始了临床Ⅲ期试验,目前正在进行中。
三、 小结
以上介绍了目前在研的阿尔茨海默症药物,除了Azeliragon,剩下的药物似乎都有上市的可能性,然而正如前所述,作为近年来失败率的药物研发领域,这些药物未来的命运仍"扑朔迷离",最后也希望我们的国产药GV-917也能在该领域大放异彩。
作者简介:W&D,医药行业从业人员,对立项调研、专利检索分析、医药行业动态、医药新技术新方法感兴趣,希望通过自己的写作,与大家分享、探讨医药行业变化。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57