基因疗法是指采用基因工程技术将正常或野生型基因导入细胞,以纠正或补偿因基因缺陷引起的机体功能缺陷,从而实现减缓或者治愈疾病的目的。近年来,新一代基因编辑技术、药物递送技术不断取得突破,促进该领域新产品不断获批上市,新兴企业持续受到金融资本的火热追捧。公开数据显示,全球基因疗法领域近五年累计投融资事件数超400起、总融资额超350亿美元,充足的资金推动基因疗法快速发展。本文将介绍近一年来获批上市的基因疗法产品,呈现该领域蓬勃发展势头。
一、基因疗法发展历程
人体疾病的发生主要是由生命活动过程中重要物质代谢失衡或对应信号通路调节失衡所引起,其中,部分疾病是基因表达缺陷造成的对应代谢功能缺失造成。基因治疗是运用基因工程技术将正常或野生型基因导入细胞,纠正或补偿因基因缺陷引起的机体功能缺陷,从而实现减缓或者治愈疾病的目的,具有潜在的"一次治疗,终生获益"。目前,基因疗法尚无明确的界定范围,从FDA定义来看,主要包括:Plasmid DNA、Viral vectors、Bacterial vectors、Human gene editing technology、Patient-derived cellular gene therapy products等类型,广义上来说,核酸药物也属于基因治疗的范畴。相较于化学药和抗体药物,基因疗法具有组织特异性强或者根源上至于疾病的优势,这主要是由于化学药靶向性较差,抗体药物虽具有较好靶向性,但作用靶点位于细胞膜膜表面,无法作用于细胞内靶点尤其是机体核酸靶点,且须长期注射使用,因此,随着基因技术的不断突破,基因疗法有望成为最 具潜力的下一代新兴疗法。
近年来,随着基因技术的不断突破,尤其是药物递送技术的快速发展以及基因测序、RNA-seq、CRISPR等技术不断迭代,行业对于基因疗法的关注度迅速提高,近五年来,全球基因疗法领域项目投融资年均增长超40%,国内的增速更是超60%,全球融资项目超400件,累计融资额近400亿美元,显示出基因疗法领域巨大的资本吸引力。Tessera Therapeutics、Kriya Therapeutics等初创型基因疗法公司陆续获得3亿美元以上的融资,罗氏、诺华、武田以及拜耳等成熟型跨国巨头则通过项目合作、兼并购等方式,加速布局基因疗法药物,体现了基因疗法的广阔前景。2022年以来,多款基因疗法接连获批上市,尚有一批在研品种处于快速推进之中。
二、多款产品集中上市
1. 芳香族L-氨基酸脱羧酶缺乏症药物--Upstaza
芳香族L-氨基酸脱羧酶缺乏症(AADCD)是一种致命的罕见遗传病,全球约有140名患者,其中我国约有20名。由于患者体内DDC基因缺失突变,导致AADC酶缺乏,影响机体左旋多巴与5-羟色胺的代谢,造成身体多巴胺和血清素缺乏,在患者出生后6个月时开始出现疾病症状,包括严重的发育迟缓,通常无法说话、进食,甚至无力抬头,并且患者经常出现持续数小时的癫痫样发作(眼动危象),往往还伴随着睡眠障碍和情绪失控。在Upstaza出现之前,该罕见遗传病尚无有效治疗方法。
2022年7月21日,PTC Therapeutics公司基因疗法Upstaza(eladocagene exuparvovec)获得欧盟委员会批准上市,用于治疗L-氨基酸脱羧酶缺乏症(AADCD)患者,是直接注入大脑的首 款获批基因疗法,也是改变AADCD疾病进程的首 款获批疗法,在AADCD的治疗乃至基因疗法领域具有里程碑意义。Upstaza通过腺相关病毒2(AAV2)递送载体将功能正常的DDC基因直接递送到大脑的壳核中,促使机体AADC酶的恢复至正常水平,多巴胺代谢正常。美国PTC Therapeutics公司成立于1998年,专注于罕见疾病药物开发和商业化,聚焦细胞中RNA转录后调控机制研究,形成了RNA剪接平台、基因治疗平台和Bio-e平台等核心技术,目前已上市6款产品,尚有一批覆盖遗传性疾病、肿瘤学、病毒学等领域的在研产品。
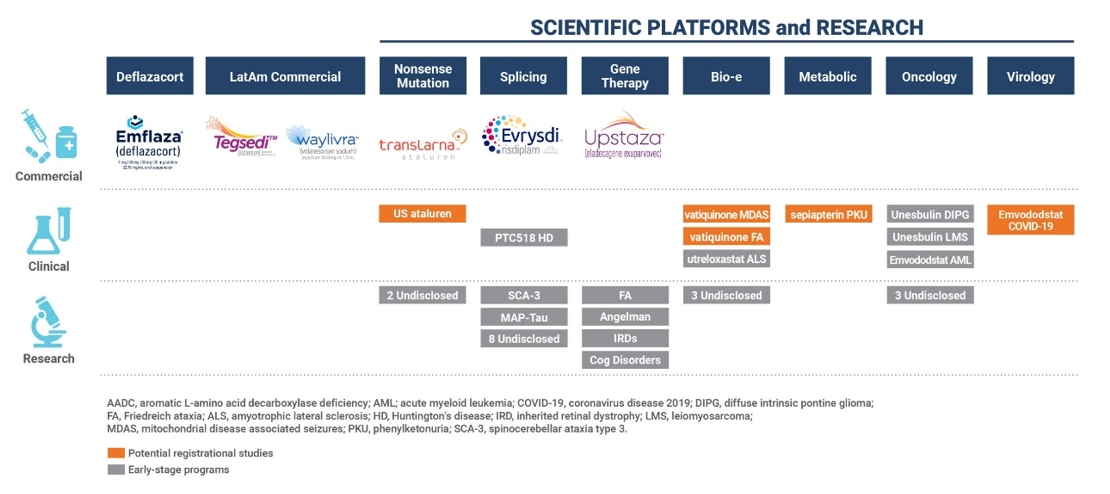
图1 PTC产品管线情况
2.β地中海贫血症药物--Zynteglo
β地中海贫血是一种严重的遗传病,由于基因缺陷导致血红蛋白中的β珠蛋白链合成缺失引起的贫血或病理状态,该病广泛分布于世界各地,全球地贫基因携带者约3.45亿人,其中我国内地地贫基因携带者约有3000万人,重型和中间型地贫患者人数约30万人,并且正以每年约10%的速度递增。当前对于地中海贫血传统疗法中,造血干细胞移植是唯一可以根治β-地中海贫血的方法,但费用昂贵且配型极其困难,此外,规律输血和充分祛铁治疗目前仍是重要的治疗方法之一。为了生存,患者不得不终身接受输血治疗,虽然输血可以暂时缓解与严重贫血相关的症状,包括疲劳、虚弱和呼吸急促,但它们并不能从根本上治疗疾病,并可能产生因为铁过载和多器官损伤导致的严重并发症。
2022年8月18日,bluebird bio公司开发的首 款用于治疗需要接受常规血红细胞输注的β地中海贫血症的基因疗法Zynteglo(betibeglogene autotemcel,beti-cel)获得FDA批准上市,Zynteglo是一次性基因治疗药物,与CAR-T基因疗法类似,属于个性化定制药物,将患者体内分离的造血干细胞在体外进行基因工程改造,经改造后的造血干细胞回输患者体内,从而源源不断地生成具有正常功能的血红细胞,极大减少患者对输血的需求甚至不需要再进行输血治疗。然而该药定价较为昂贵,高达280万美元,患者可及性上仍面临较大挑战。美国bluebird bio是全球知名的基因治疗公司,构建了世界上最庞大的离体基因治疗数据库,多项遗传疾病的临床研究世界领先,通过基因添加、细胞治疗和基因编辑等技术,对大脑型肾上腺脑白质营养不良、镰状细胞病、输血依赖型β-地中海贫血及多发性骨髓瘤等领域进行研究。
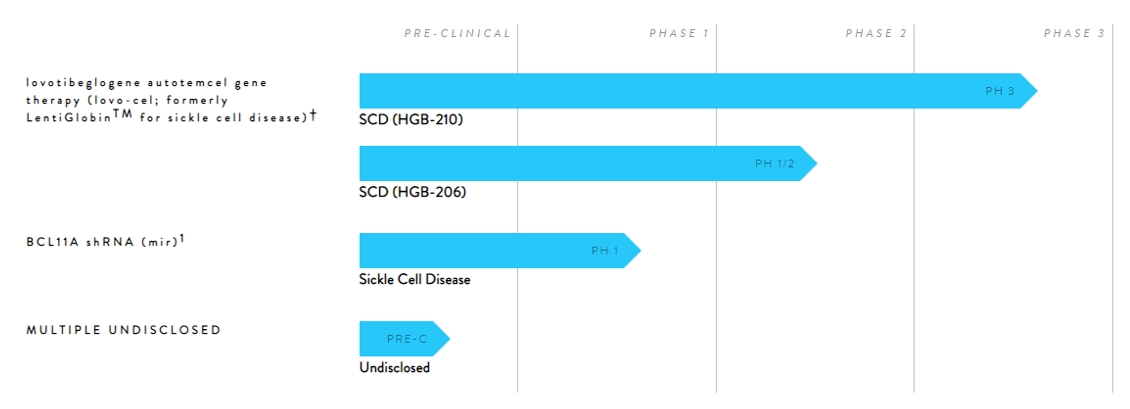
图2 bluebird bio产品管线情况
3.严重血友病A药物--Roctavian
血友病是一种因遗传性凝血活酶生成障碍引起的出血性疾病,由于人体凝血因子基因异常,导致凝血因子缺乏,引起凝血机制异常,临床表现多为自发或外伤后出血不止、形成血肿及关节出血,其中凝血因子Ⅷ缺乏为血友病A型更为常见且绝大多数患者为男性。全球约有80万血友病患者,其中重症患者约27万人,重度A型血友病的护理标准是长期终身静脉输注凝血因子VIII,以维持血液中有足够的凝血因子VIII防止出血,根本解决方案是将健康基因移植到患者体内或纠正导致疾病的基因缺陷部分。
2022年8月25日,BioMarin Pharmaceutical公司全球首 款用于治疗严重血友病A成人患者的基因疗法Roctavian在欧盟委员会附条件批准上市,Roctavian通过腺相关病毒5(AAV5)递送载体,通过基因改造修饰,产生与凝血因子VIII相似的氨基酸序列,相当于将编码凝血因子VIII基因的功能性拷贝递送到患者体内,从而帮助患者恢复自身凝血因子VIII生产能力,该药的优势在于患者可能只需要接受一次治疗,肝细胞就可以持续表达因子VIII,从而不再需要长期接受预防性凝血因子注射。美国BioMarin Pharmaceutical公司,聚焦于严重的、危及生命的罕见病治疗药物开发,目前已有7款产品上市以及多款处于临床或临床前在研药物。
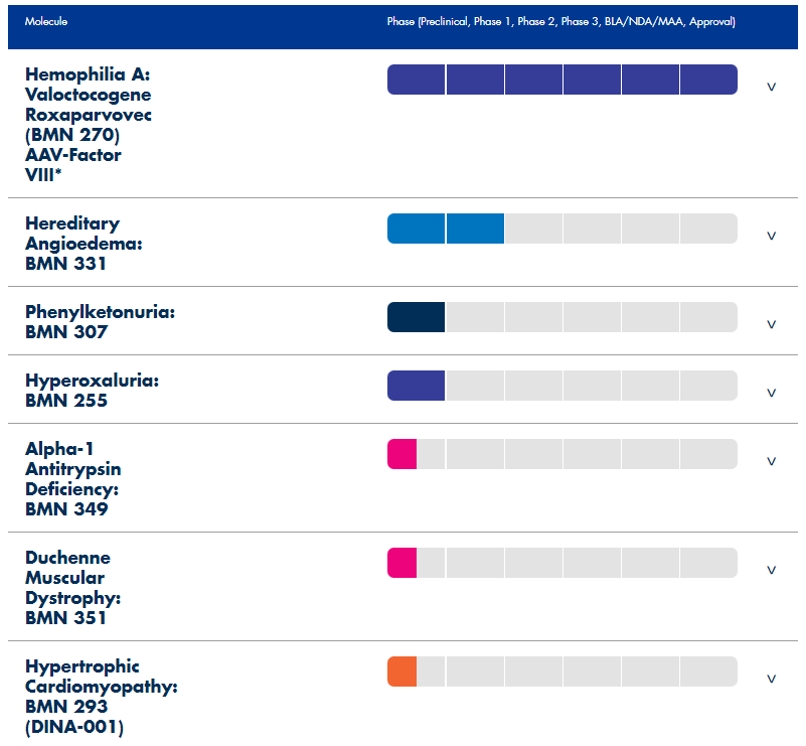
图3 BioMarin Pharmaceutical产品管线情况
4.肾上腺脑白质营养不良症药物--Skysona
肾上腺脑白质营养不良(ALD)是一种罕见的X连锁隐性遗传病,以男性患者为主,全球每2万名男性新生儿中就约有一名患有ALD,该疾病的致病基因编码生成肾上腺脑白质营养不良蛋白(ALDP),细胞中过氧化物酶体对超长链脂肪酸(VLCFA)的氧化发生障碍,导致超长链脂肪酸在血、脑白质、肾上腺皮质等器官和组织内大量聚积,引起中枢神经系统脱髓鞘和肾上腺皮质萎缩或发育不良,大约40%的ALD男童患者会发展为CALD,这是ALD中最严重的一种,CALD是一种罕见的神经退行性疾病,症状通常发生于儿童时期(中位年龄为7岁),可迅速导致进行性、不可逆的神经功能丧失和死亡。目前该病尚无特 效治疗药物,且治疗方法有一定的局限性,大多采用大量糖皮质类固醇,亦可用抗凝治疗。未来非特异性治疗包括诱导完好少突胶质细胞对脱髓鞘轴突重新进行修复,形成新的髓鞘或进行胚胎干细胞移植,后者可分化成有功能的,成髓鞘的少突胶质细胞。
2022年9月,bluebird bio公司用于延缓4-17岁早期活动性脑性肾上腺脑白质营养不良(CALD)男童的神经功能障碍的基因疗法Skysona(elivaldogene autotemcel,eli-cel)上市。Skysona有望实现一次给药、终身有效,且无需造血干细胞移植,曾获FDA授予的突破性疗法认定、孤儿药和优先审评资格。该药利用慢病毒载体,在体外将ABCD1基因的功能性拷贝导入到患者自身的造血干细胞中,再输回到患者体内产生ALD蛋白,从而促进VLCFAs的分解,其治疗目标是阻止CALD的进展,并尽可能保留神经功能,包括保留患者的运动功能和沟通能力。
到了2023年,5月,Krystal开发的基因疗法Vyjuvek获得FDA批准上市,用于治疗营养不良性大疱性表皮松解症(DEB),是首 个FDA批准的外用基因疗法,也是首 款可重复给药的基因疗法;6月,Sarepta与罗氏联合开发的基因疗法Elevidys获得FDA加速批准上市,成为首 个用于治疗杜氏肌营养不良(DMD)4-5岁患者的一次性基因疗法,实现该领域基因疗法零的突破。
三、市场应用及展望
基因疗法大多数针对罕见疾病,通常认为患者人数较少,然而就我国而言,面对庞大的人口基数,或许罕见病并不"罕见",且这类疾病通常面临无药可用的窘境,严重影响了患者生存,亟需突破性疗法药物。基因疗法开发难度较大,首先要确保药物的安全性,对技术水平要求较高,尤其依赖药物递送和基因编辑等技术,其发展历程也是几经沉浮,近年来逐渐迎来了大突破、大增长。然而,基因疗法突破技术上的艰难险阻,产品获批上市后即面临商业化的难题,国内CAR-T疗法高达120万元的定价令部分患者遥不可及,上文bluebird bio公司的Zynteglo定价更是高达280万美元,基因疗法定价屡创新高,如何商业化,提高患者可及性成为了企业必须面对的问题。
目前,国际上主要的基因治疗药物支付模式有:分期付款:在规定的时间范围内,若治疗有效则定期费用,将一次治疗产生的高额费用分散到一段时期,降低患者及社会短期内资金压力;按疗效付费:基于治疗结果的付款方式,使得在应对基因治疗长期效果的不确定性方面更具可操作性;专项基金:通过成立专项基金的方式,缓解支付压力。国内目前的支付方式仍较为单一,对基本医保存在一定的依赖,据公开数据,去年国家医保目录已经纳入涵盖29种罕见病的58种药物,纳入医保的罕见病药物数量占所有上市的罕见病药物的比例已达到2/3,然而目前仍有部分年治疗费用超50万元的高值药未进入医保,受限于高昂的治疗费用,患者依然面临"用不起药"的困境。我国应尝试加快构建基于基本医保保障的多层次支付体系,一是加快完善各层级商业保险,以"政府指导+市场化运行"的方式,开发出更多的商业保险产品,作为医保的有效补充形式;二是探索设立专项基金,通过政府引导,探索设立专项救助基金,资金来源可以是慈善捐赠、社会众筹等。只有建立起完善的支付体系,才能真正惠及患者,从市场终端拉动基因治疗药物的发展。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57