作者:糖醋小里脊
据CDE官网显示,来凯医药科技(上海)有限公司(以下简称“来凯医药”)治疗用生物制品1类新药LAE102注射液获得临床试验默示许可,适应症为超重和/或肥胖。4月15日,来凯医药宣布该药物的肥胖适应症获得了美国FDA IND批准。

图片来源:CDE官网
01
针对全球新靶点
中美IND双获批
据相关研究显示,肌生长抑制素是肌肉质量的主要负调节因子,主要通过激活素II型受体 (ActRII) 发挥作用。更进一步研究认为,Activin-ActRII通路与肌肉萎缩、脂肪累积及癌症的发生有所关联,阻断该通路可促进肌肉再生并减少脂肪。
2023年7月,礼来公司以19.25亿美元巨额收购了Versanis公司,囊括其ActRIIA/B抗体。据公开资料显示,该抗体的突出特点为在减脂肪的同时能够保留肌肉质量。ActRII作为全球新兴靶点,受到了研究者们广泛的关注。
LAE102是来凯医药研发的一款ActRIIA单抗,在临床前研究中展现出了增加肌肉并减少脂肪的效果。据来凯医药报道,LAE102还能够与GLP-1受体激动剂联用,在进一步减少脂肪的同时能够显著降低GLP-1受体激动剂导致的肌肉流失。2023年5月,LAE102用于非小细胞癌的临床试验获得了美国FDA批准;而后,其在中国的实体瘤适应症临床试验申请也获得了默示许可。
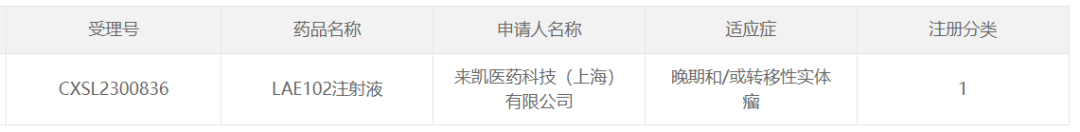
图片来源:CDE官网
来凯医药曾表示,计划探索LAE102应用于其他适应症,包括其他代谢疾病以及肺动脉高压等。
02
聚焦肿瘤、代谢…
加快药物临床进度
来凯医药聚焦癌症、代谢疾病及肝纤维化等疾病领域,目前已建起全面丰富的在研管线,并持续加速管线的临床研究进度。

图片来源:来凯医药
Afuresertib
肿瘤领域,来凯医药已披露10款在研药物。其中,新一代小分子泛AKT激酶强效抑制剂Afuresertib(LAE002)是其研发进展最快的药物,正在海内外推进多个临床试验。在2024 AACR大会上,Afuresertib联合PD-L1单抗及白蛋白紫杉醇用于三阴性乳腺癌的Ⅰ期临床研究结果发布,显示该组合具有可控的安全性。
LAE001
LAE001是新一代雄激素合成抑制剂,靶向于CYP17A1和CYP11B2双靶点,具有减轻“原发性醛固酮”症状的潜力。在2023 ESMO大会上,LAE001联合AKT抑制剂Afuresertib用于mCRPC展现出了积极的抗肿瘤活性,有望为患者带来良好的治疗效果。
LAE103、LAE123
围绕ActRII受体,来凯医药还自主开发了更多候选药物,包括ActRIIB选择性抗体LAE103以及ActRIIA/IIB双靶点抑制剂LAE123,拟用于肌肉再生及与之相关的适应症。其中,LAE103正在进入PCC阶段。
此外,来凯医药在2023年报中表示,包括具有sHSC杀伤和抗纤维化活性的双功能aHSC-NK接合剂LAE105、FGFR2b特异性单抗LAE112以及USP1抑制剂LAE120等在内的多个在研项目正进入PCC阶段。
03
结语
来凯医药计划于在2024年下半年启动LAE102的首次人体临床研究,通过加速推动相关研究,来凯医药有望为全球肥胖人群带来更新的选择。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57