上周(6月24日~6月30日),共62个品种通过/视同通过一致性评价。其中,一品红的奥美沙坦酯口崩片、石药集团的哌柏西利片等为国产首个获批药物。同期,76个品种申报一致性评价。
01
国产首家
一品红、石药…
据NMPA官网显示,一品红的奥美沙坦酯口崩片、石药集团的哌柏西利片均于6月25日获得上市批件。
《中国心血管健康与疾病报告2020》显示,根据2012年—2015年的中国高血压调查(CHS),中国≥18岁成人高血压患病率已经达到了27.9%。2013年,中国卫生总费用为31869亿元,其中高血压直接经济负担占6.6%。国家心血管病中心发布的《国家基层高血压防治管理手册 2020版》提到:“所有高血压患者一旦诊断,建议在生活方式干预的同时立即启动药物治疗。”在高血压防治中,药物手段至关重要。
奥美沙坦酯是一种非肽类血管紧张素Ⅱ受体拮抗剂,原研企业为第一三共。其降压效果强大且持久,一天一次给药可以维持降压24小时。同时,奥美沙坦酯还可以保护心血管和肾脏,不经过细胞色素P450酶代谢,与心血管系统常用药物联用顾虑少。
奥美沙坦酯属于前体药物,经胃肠道吸收水解为奥美沙坦。奥美沙坦属于新一代、血管紧张素Ⅱ拮抗剂,通过选择性阻断血管紧张素Ⅱ与血管平滑肌AT1受体的结合而阻断血管紧张素Ⅱ的收缩血管作用,因此它的作用独立于AngⅡ合成途径之外。奥美沙坦与AT1的亲和力比与AT2的亲和力大12500多倍。
此外,与普通片剂相比,口崩片剂型拥有服用方便;能够避免肝脏首过效应,起效迅速;口感良好,容易吞咽,降低胃肠道刺激等特点。
据一品红报道,其获批的奥美沙坦酯口崩片是国内首家获批的视同通过一致性评价产品,原研尚未进入国内销售。根据核准的说明书,奥美沙坦酯口崩片适用于高血压的治疗。
哌柏西利是一款小分子CDK4/6抑制剂,原研公司为辉瑞,商品名为Ibrance(爱博新)。哌柏西利是全球首个上市的细胞周期蛋白依赖性激酶(CDK)4/6抑制剂,可通过抑制CDK4/6恢复细胞周期控制,从而阻断肿瘤细胞增殖,相继获批了胶囊和片剂两种剂型。据辉瑞财报统计,2023年Ibrance的全球销售额为47.53亿美元。
2023年1月18日,国家医疗保障局、人力资源和社会保障部公布了《国家基本医疗保险、工伤保险和生育保险药品目录(2022年)》,哌柏西利胶囊成功进入目录。哌柏西利片是辉瑞开发的另一口服剂型,于2019年11月获FDA批准。2023年8月,辉瑞25mg、125mg的哌柏西利片获批在华上市。
据了解,2022年5月9日,石药欧意公示了其哌柏西利片的生物等效性试验,规格为125mg,适用于激素受体(HR)阳性、人表皮生长因子受体 2(HER2)阴性的晚期或转移性乳腺癌,应与芳香化酶抑制剂联合使用作为绝经后女性或男性患者的初始内分泌治疗或与氟维司群联合使用用于内分泌治疗后疾病进展的患者。同年8月17日,该项BE试验完成。
02
一致性评价通过情况
6月24日~6月30日期间,共62个品种通过/视同通过一致性评价。
具体情况如下:
表1: 6月24日~6月30日,通过一致性评价的品种图片
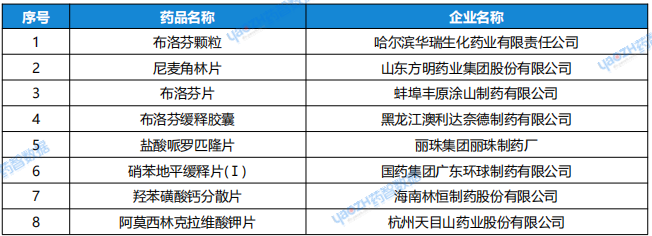
资料来源:药智数据企业版——仿制药一致性评价分析系统数据库
表2:6月24日~6月30日,视同通过一致性评价的品种图片图片
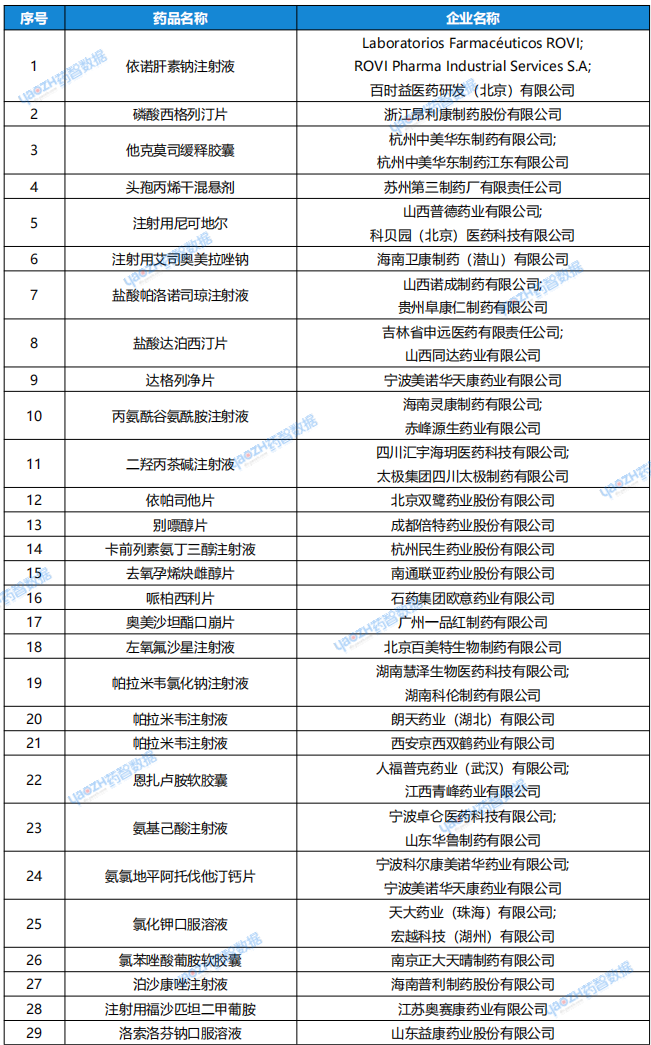
资料来源:药智数据企业版——仿制药一致性评价分析系统数据库
03
一致性评价受理情况
6月24日~6月30日,共76个品种申报一致性评价,具体情况如下:
表3: 6月24日~6月30日,一致性评价申报情况
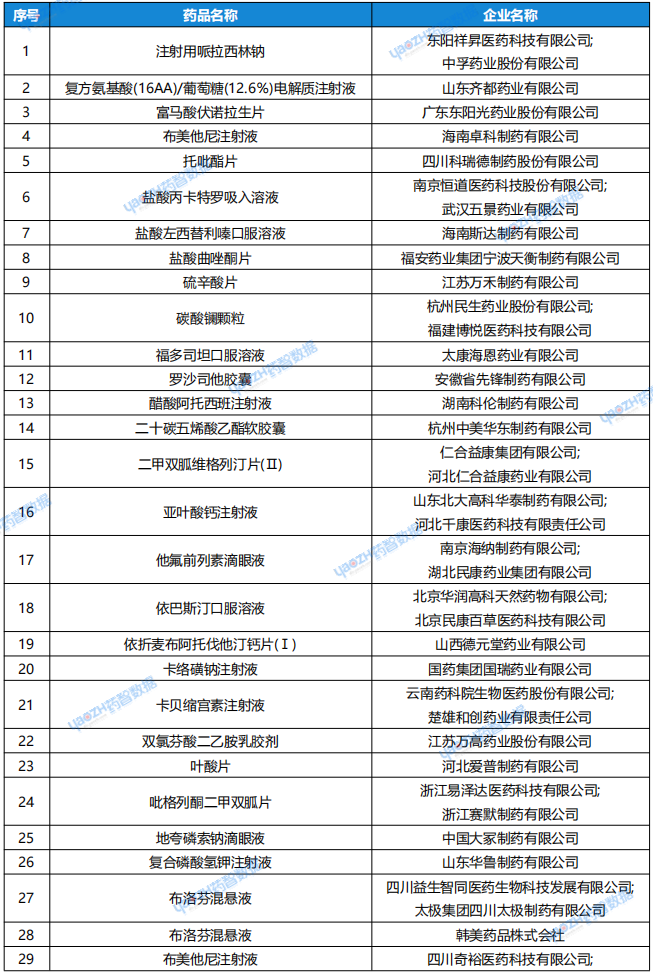
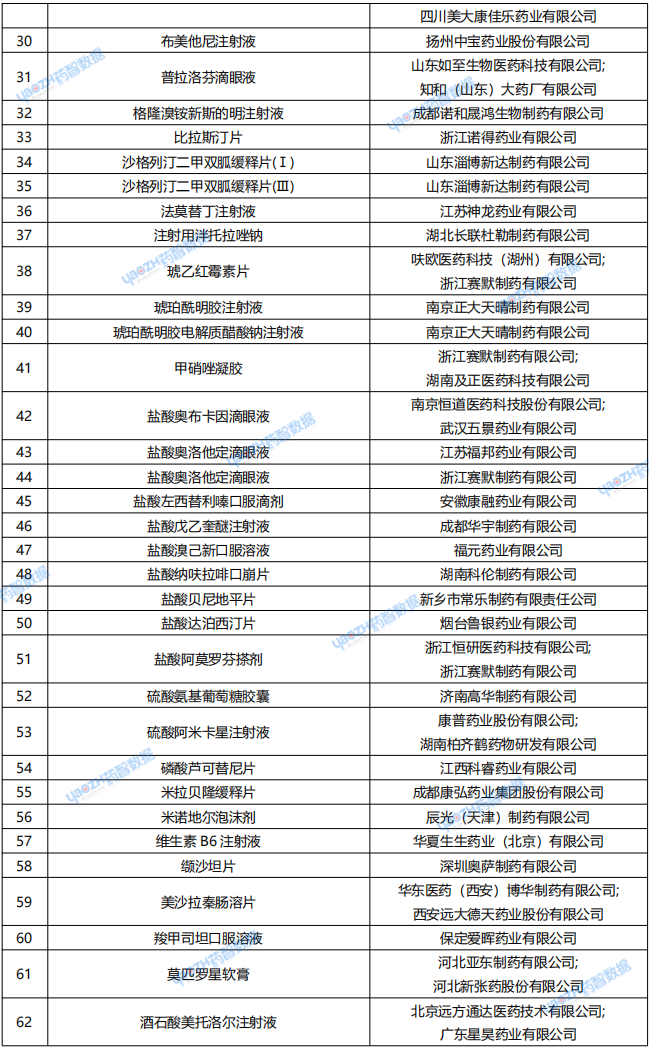
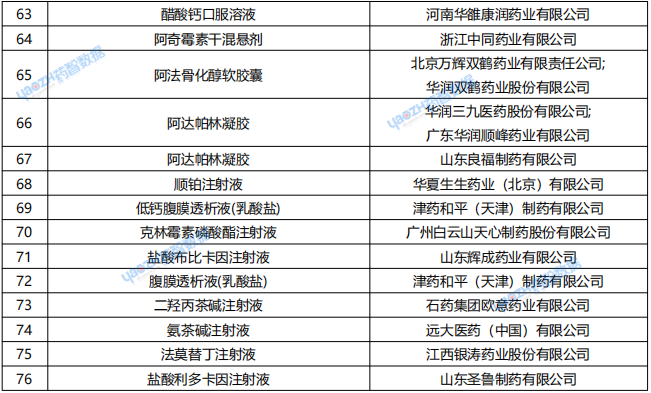
资料来源:药智数据企业版——仿制药一致性评价分析系统数据库



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57