据笔者观察,目前国内很多药厂只设有一些常规部门,如生产部、质量部、仓储部、采购部、销售部、行政部、财务部,甚至公关部、上市办、EHS部等,往往没有设置专门的部门管理医学、药政和知识产权。虽然缺少医学、药政和知识产权管理的支持,企业日常运转看起来可能也没有什么问题,但这些属于战略层次的内容,少了这些战略层面的指导,企业运行就像大海航行没有指南针一样。
1、医学研究部门:药品质量为临床服务
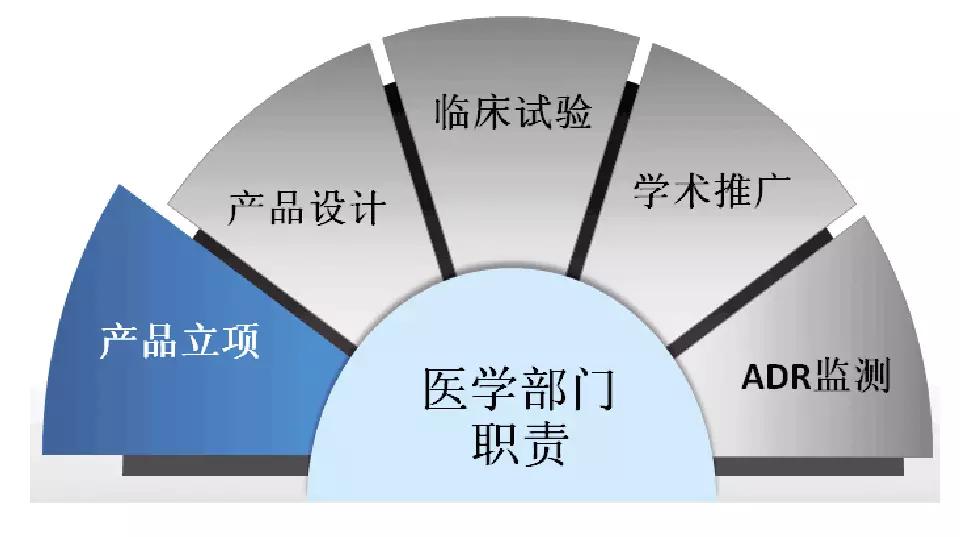
离开医学,也许药什么都不是;了解药,首先要了解医——只有清楚疾病的发病机理、流行情况、治疗手段及未来发展趋势,才能清楚某种药物在不同适应症、不同适用人群中的临床价值,可能的替代药物和其他治疗手段,进而清楚其目标市场在哪里,处于产品生命周期的哪一个阶段(导入期、成长期、成熟期还是衰退期),进而采取相应的市场策略。
医学知识在产品立项、产品设计、临床试验过程、不良反应监测、学术推广等各个环节必不可少。
在产品立项阶段,医学部门就应向项目负责人提供流行病学、疾病治疗手段及其趋势等资料。假如计划仿制或创新的药物,其在目标适应症上的应用近期内可能为其他风险效益比更好的治疗手段(如其他药疗方案或理疗方案)所取代,立项就不成立。
在药理毒理和临床试验阶段,则可根据其在不同适应症和/或适用人群的临床价值,建议优先完成哪些药理毒理和临床试验。
产品上市前,根据临床试验数据,判断药物在不同适应症和/或适用人群中的药物经济学价值,完成产品定位;产品上市后,根据收集的临床资料(包括不良反应资料),分析药物在不同适应症、适用人群及不同用药方案(如联合用药)中的价值,修订用药方案,并进行新用途开发,为学术营销提供资料。
国产治疗风湿性关节炎的某药品,曾受R国同类产品在R国投放数月后给5名患者造成严重影响,品种本身的风险效益比受到怀疑,该国同品种厂家因为有替代品种,准备采取默认的策略以打击我们的竞争产品。后来,我们的国产厂家收集到了大量的药品不良反应统计数据,提供了令人信服的风险效益比证据,从而避免了一场大 麻 烦,不能不说是医学帮了大忙。说到这里,笔者不得不提到中国药品GMP规范中的一个特殊章节“不良反应报告”一节,很多国家和地区都没有,在笔者看来,我国GMP规范在最初设计时在潜意识中已经认识到药品质量是为临床服务的。
当然,医学知识的应用远远不止这些。以质量管理为例,质量的本质就是满足客户需求,药品的最终客户是谁?是患者,所以,质量管理的起点是临床,终点也是临床。
欧盟GMP中描述得很清楚,药品质量风险评估最终要与保护患者相关联。药品的关键质量属性,就是那些与药品安全性和有效性相关的质量属性。不懂医,谈何药品质量?
有人可能认为医学是搞创新药的企业才该玩的,做仿制药则无所谓,这种观点大错特错。创新药当然需要医学的支持,仿制药同样需要,不清楚目标适应症的流行病情况及其治疗趋势,不清楚产品的生命周期就仿制相当于赌博,万一要仿的品种马上就被新的医学手段所替代呢?更何况一个仿制药的投入也不低。
同样,医学不仅制剂厂家需要重视,原料药厂家一样要重视,只要想一想原料药生产出来干什么用的就清楚了。不搞清楚制剂,就不可能搞清楚原料药。
2、知识产权管理部门:扎紧自己的“篱笆”+突破别人的“篱笆”
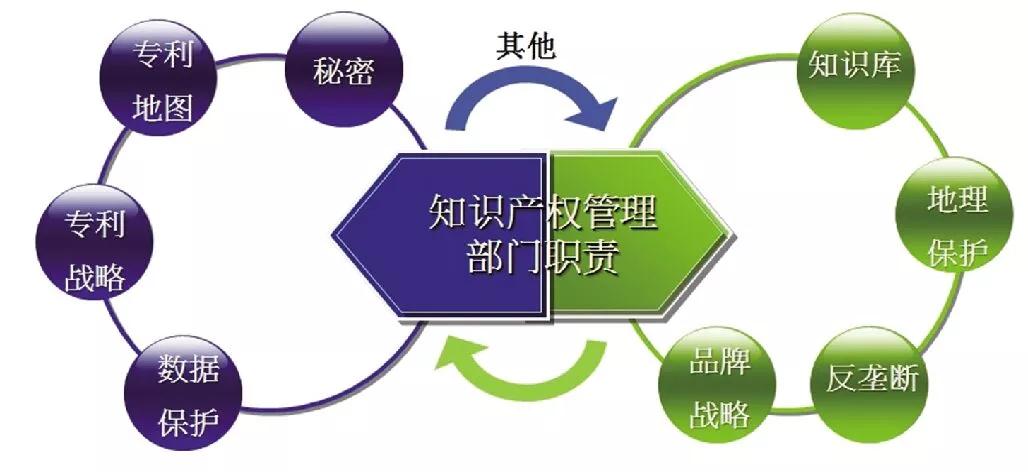
从经济学角度讲,任何没有壁垒的市场,经济利润最多只能是零,即的情况就是获得平均利润。所以,扎紧“篱笆”和想办法突破别人的“篱笆”,是所有企业的重要工作。
笔者留意到,1月初,国家知识产权局专利复审委员会发布Entresto(沙库巴曲缬沙坦钠片,LCZ696)的专利审查结果,宣告其《含有缬沙坦和NEP抑制剂的药物组合物》“全部无效”。以“沙库巴曲缬沙坦钠”为关键词,在CDE收审情况栏搜索发现,有3家公司已于2017年12月以化药2.1类提出了沙库巴曲缬沙坦钙钠共晶体和沙库巴曲缬沙坦钠片新药临床试验申请。当然,当事药企依然拥有向北京知识产权法院起诉的权利,但不能不说,这足以给国内药企一个启示,那就是办好药厂不能不懂专利。
毫无疑问,知识产权管理是扎“篱笆”和突破别人“篱笆”的主要手段。上述案例中,以“涉案专利说明书公开不充分”等理由,向专利复审委员会提出《含有缬沙坦和NEP抑制剂的药物组合物》专利无效宣告请求,就属于拆“篱笆”行为。
笔者曾在某药企任总工程师,经常与专利打交道,根据经验,在产品立项前,企业应建立专利地图,清楚本产品目前的专利状况。包括哪些企业和个人在哪些国家和地区申请了哪些专利?其法律状态如何?仔细研究每个影响立项的专利稳定性,为立项的可行性提供依据。
确定立项后,告知研发部门,目前有哪些技术属于公用公知技术可以拿来就用;哪些有专利保护,需要获得授权或绕开它;自己的哪些技术是专有的,可以通过技术秘密或专利保护起来,设置自己的“篱笆”防止他人擅入。
公司专利部门还可建立和维护自己的知识库,分清楚哪些是公用公知技术(包括过期专利技术和论文等),哪些是专有技术,建立知识分享、收集、整理、分析体系。还应帮助公司制定专利战略(如进攻策略、防守策略等)。
我国的药品注册管理办法也计划纳入专利链接制度,届时,企业更应重视制度研究,学习和利用好该制度。
很多小公司以为,发明是大公司的事情,小公司搞不了,这是不对的。比如创口贴,有圈内朋友就职于生产创口贴的药企,全公司上下不足百人,但相关产品在国内已获授权的发明专利就有6个,还有1个美国发明专利。
除了专利,商标、反不正当竞争、反垄断等也是药企重要的知识产权获得。当然,对于不同类型的企业,知识产权管理的重点有所不同。OTC企业,商标、商品名和包装设计是其客户首先关注到的内容,可能非常重要;对于原料药企业,生产工艺技术的专利和秘密、反垄断就很重要。
值得一提的是,我国近年频频重拳打击原料药经营者价格垄断行为。去年末,国家发改委发布了《短缺药品和原料药经营者价格行为指南》,值得研究。个人认为,原料药生产只要获得技术上的突破,成本就有可能大幅下降。特别是发酵产品或以发酵为起始物料的半合成产品,发酵表达成倍的增长都是有可能的。尽管制剂厂家变更原料药成本较高,需要进行稳定性试验等并获得监管方批准,但只要质量和价格具有优势,就可能压倒其他厂家一家独大。
3、药政法规研究部门:无论企业体量大小都应重视
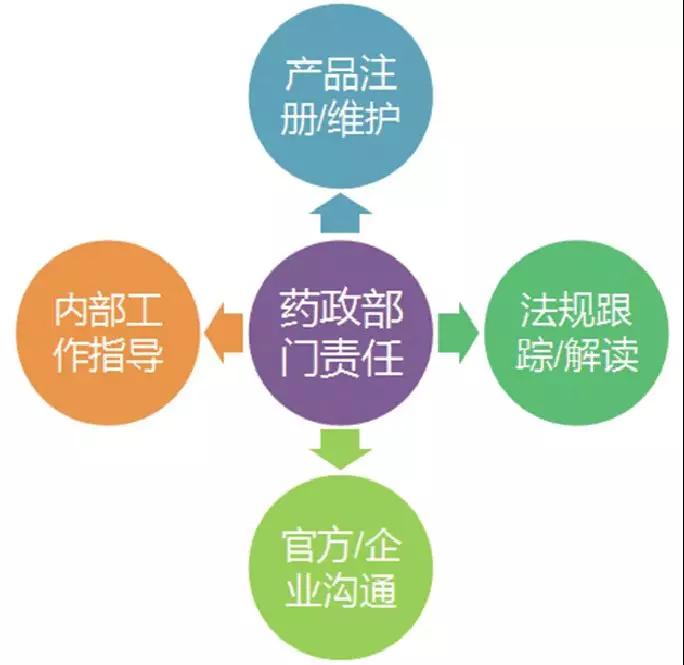
两年前,笔者参加了一场“制药企业国际化过程中常见问题及解决方案”培训课程,非常认同授课人讲的国内制药企业国际化过程中遇到的很多问题,与其组织机构设置上没有设置专门的药政法规部门有关。
没有专门的药政法规部门,企业在药政法规、指南的跟踪与研究,并及时转化成企业管理规范,及对其他企业失败信息的了解,以指导本企业有针对性地整改上就很难做好。
1.出口型企业 特别是出口型药企,面临的国际环境非常复杂,各国和地区法律体系不同,药政管理思路不尽相同,药政注册要求和质量管理要求不断变化,应有专门的机构和人员去跟踪和解读所有目标市场的法规变化。这样的部门通常还会负责法规文件(如DMF文件)编写和维护、检查动向与趋势分析、公司内部文件的法规符合性审查,以及公司对外承诺(如稳定性承诺、TSE/BSE申明)的检查等。
企业药政法规部门通常作为指导部门设在企业负责人之下,在研发、技术转移、偏差、变更、OOS、风险评估等方面提供法规符合性和技术指导原则方面指导,没有指挥权,只有审查权和建议权。从某种角度讲,正因为质量、生产、研发环节都必须在合法合规基础上运行,所以对药政法规进行深入了解的重要性甚至还要更胜一筹。
2.内销型企业 对于完全只内销的企业,是否可以完全不需要药政法规部门呢?个人认为并不一定,得从企业实际出发。当前,中国药品监管方面的法律法规变化非常大,药品管理、药品注册管理办法、一致性评价等,再加上中国正式加入了ICH,没有专门的组织和人员负责政策研究,恐怕也很难吃透。
此外,对于小体量的出口企业,建议引入外脑。企业不管大小,只要目标市场一样,其法规需求是一样的。比如同样出口欧盟和美国,不管是年产值100个亿的大公司还是年产值1000万元的小公司,都应熟悉欧盟和美国的药事法规和各种指导原则,熟悉欧盟和美国的监管模式、未来发展趋势。大公司可能会组建一个几十个人的专门组织研究这些问题,小公司可能根本办不到,但借助适合的外脑可以完成大部分工作。
总结<<<
现代药企离不开医学、知识产权和药政法规方面的指导,相应的,在组织机构设置上必须要考虑这方面的职责分配。至于具体怎么设置,各个企业可以根据自身情况具体安排。
笔者所在企业规模较小,就只设置一个药政法规部,同时负责医学、知识产权和药政法规方面的工作。很多圈内朋友的公司会设置一个总工程师职位,负责技术和质量及以上工作。不管怎么样,个人认为,这些方面应有指定专人负责,做到事事有人管,事事有人做。
国内外GMP规范中都有专门的章节讲述组织机构与人员,说明要做好工作,组织保证很重要。同样的,在医学、知识产权和药政法规研究上,组织机构的设立和岗位工作职责必须明确。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57