2月12日,石药集团公告称其注射用紫杉醇(白蛋白结合型)已获得CFDA的注册批件。石药成为白蛋白紫杉醇在国内的首仿厂家。

石药集团欧意药业和恒瑞是国内最早提交白蛋白紫杉醇生产申请的两家企业。在白蛋白紫杉醇的首仿争夺战中各辟蹊径。欧意是在完成BE后按照化药新分类直接报产。恒瑞之前以“首仿”的理由获得了优先审评资格(CYHS1300522),在仿制药获批BE临床后,直接寄国家局药审中心申请生产(CYHS1790004)
石药集团赢得首仿之后,恒瑞预计将成为第2家上市白蛋白紫杉醇的厂家。恒瑞的注射用紫杉醇(白蛋白结合型)6类仿制申请在2017/2/20获得CDE承办受理,目前处于在审评审批状态。
白蛋白紫杉醇由美国Abraxis BioScience公司开发,是一种紫杉醇与白蛋白结合的全新制剂,克服了普通紫杉醇水溶性差、效率低和副作用大等缺点,于2005年1月被FDA批准上市治疗乳腺癌(商品名Abraxane),随后又获批治疗肺癌、胰 腺癌。2010年新基以29亿美元首付款收购Abraxis,将Abraxane收入囊中。
我国于2008年批准新基Abraxane进口药品,2015 年注射用紫杉醇(白蛋白结合型)中国市场销售额约为 3614.2 万美元,2017年,Abraxane的全球销售额是9.92亿美元(+2%)。
新基Abraxane历年销售额(百万美元)
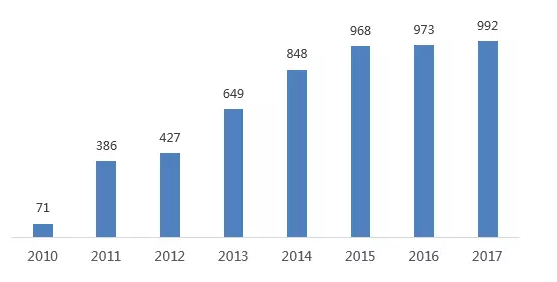
新基去年7月在与百济神州的交易中,将Abraxane在中国的市场权益授予了后者。同时,百济神州也全面接管了新基在中国的商业团队,负责Abraxane在中国的商业推广和销售。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57