辉瑞公司-纽约在2018年3月29日宣布,Tafamidis的三期临床评估结果显示: tafamidis治疗转甲状腺素蛋白心肌病符合其主要终点,阳性。试验进行了30个月,与使用安慰剂的组别相比,tafamidis显着降低全因死亡率和心血管相关患者的住院频率,结果具有统计学意义。 初步的安全性数据显示,tafamidis在受试人群中的耐受性良好,没有发现新的安全性信号。
以下是其药品相关说明:
Tafamidis临床试验日期:
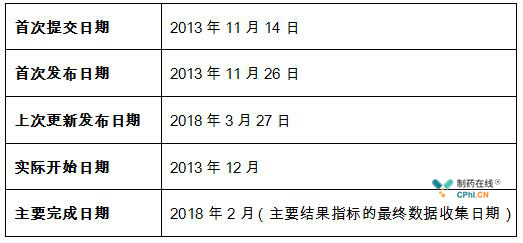
Tafamidis注册信息:

同时,辉瑞公司宣称该研究包括患有变异或遗传性疾病的患者,以及具有野生型形式的患者-这种形式是不具有遗传性的,并且可能随着年龄增长而发生。同时,这些结果是初步的主要数据,有待进一步分析。完整的数据和详细的结果将提交在即将举行的美国的科学大会上,并在同行评审的期刊上发表。
什么是罕见病?
罕见病(Rare Disease),是指流行率很低、很少见的疾病,一般为慢性、严重性疾病,常危及生命。国际确认的罕见病有7000多种,约占人类疾病的10%。在种类繁多的罕见病当中,约有80%是由于基因缺陷所导致的。我国尚无罕见病的官方定义。
什么是ATTR-ACT?
ATTR-ACT即甲状腺功能亢进性心肌病,是体内甲状腺素T3和(或)T4持续升高对心脏传导系统和心肌细胞的作用而导致的一系列并发症,属于罕见病的范畴。
罕见病和ATTR-ACT治疗现状
罕见病全球有七千余种,而有药能够治疗的罕见病不到5%。现在全球的跨国企业中,诺华、罗氏、塞尔基因、辉瑞、赛诺菲、罗氏、梯瓦制药等企业在罕见病的治疗方面投入较多资本,但一个创新药品的出现成本很高,对于全球众多有需要的患者而言杯水车薪。
目前国内外治疗的ATTR-ACT的方法均是将甲亢首先治愈,缓解给心血管系统带来的负担,然后再采用对应的心血管治疗方案,并没有针对ATTR-ACT专门的药物。因此辉瑞公司的Tafamidis三期临床结果为患者带来了福音,在全球都具有广阔的医疗市场。
参考文献:
1、Data on file. Pfizer Inc. New York, NY.THAOS - Transthyretin Amyloidosis Outcomes Survey. Disease Background - transthyretin amyloidosis.
2、Safety and Efficacy of Tafamidis in Patients With Transthyretin Cardiomyopathy (ATTR-ACT).U.S. National Library of Medicine(NIH). https://www.clinicaltrials.gov/ct2/show/record/NCT01994889?view=record
作者简介:小药迷,硕士,药物制剂专业,长期关注国内外新药的研究和开发、药学药师相关国家政策,希望从事药学领域相关的市场工作。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57