
近日,由于临床试验的收益/风险比不平衡,AbbVie研发管线中的一项针对实体瘤治疗的ADC药物SC-007的I期临床试验被终止。而就在上周,另一家ADC研发公司ADC Therapeutics同样放弃了其处于临床试验中的ADC药物ADCT-502,可见目前ADC药物的研发中还存在一些挑战。
新药从立项到上市需要经过重重挑战,如临床前研究和临床试验,而在整个新药研发过程中临床试验是成本、起决定性作用的阶段。如果可以在早期临床试验(I期临床)中发现候选药物的潜在成功率,选择性地放弃部分候选药物不失为一种节约研发成本的策略。
近日,AbbVie终止了其抗体偶联药物(Antibody-Drug Conjugate,ADC)SC-007的I期临床试验,因其没有表现出收益/风险的平衡,SC-007是AbbVie在2016年98亿美元收购Stemcentrx时获得的研发管线。临床试验对象为结直肠癌和胃癌患者,然而ADC药物SC-007的靶点还未被揭示,这项试验采用多剂量的给药方式,以患者对药物的耐受**为主要终点。
AbbVie的发言人表示,"SC-007的临床试验还只是处于非常早期的仅有7名患者参与的临床I期试验,并且没有表现出收益/风险的平衡,"发言人没有提到SC-007的副作用及是否会再进行研究。虽然来自Stemcentrx SC-007的I期临床试验被终止了,但AbbVie表示Stemcentrx在多种恶性肿瘤领域中还有不少具有潜力的临床研究,Stemcentrx的肿瘤研究和药物研发平台也是AbbVie需要的。

(图片来源于网络)
无独有偶,一周前ADC Therapeutics靶向HER2的ADC药物ADCT-502的I期临床试验结果没有显示出临床收益,产生疗效的给药剂量存在耐受性问题,基于此ADCT宣布停止其后续的ADCT-502的临床试验。作为主攻ADC药物的ADCT公司,一处研发管线的失利并不会造成太大的影响,在2019年早期ADCT还会有6种ADC药物进入临床试验,但这同时也体现出ADC药物从临床阶段到获批上市的困难。
就目前而言,虽然有上百项正在进行的ADC药物的临床试验,但只有为数不多的获得FDA批准上市,如Pfizer治疗白血病的Mylotarg、Genetics/Takeda治疗霍杰金淋巴瘤的Adcetris和Roche治疗乳腺癌的Kadcyla。ADC药物复杂的结构带来的不仅是较强的肿瘤杀伤作用,伴随而来的是临床收益不明显和安全隐患,从而在临床试验中多次遭遇失败。
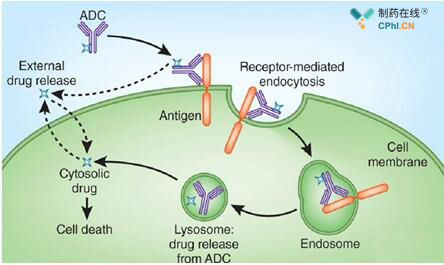
ADC结构及其作用机理(图片来源于网络)
ADC由单克隆抗体、细胞**药物和linker三部分组成,其集单克隆抗体和细胞毒素两者优点于一身,在具有高度靶向性的同时,增加了对肿瘤细胞的杀伤性。然而复杂的ADC结构同样带来了挑战,为获得明显的临床收益,选择高活性细胞**药物、稳定的交联技术、优化细胞毒素药物连接数量、选择合适的抗原已经成为新型ADC药物研发面临的问题,此外ADC药物的规模化生产也是需要克服的难题。
当ADC药物进入临床试验阶段时,安全性、有效性和临床收益成为其上市的准则。有研究表明,ADC药物由于Linker的关系而具有旁观者效应,在杀伤肿瘤细胞的同时也将周围正常细胞,即脱靶效应。由于肿瘤微环境的影响,针对实体肿瘤的ADC药物还会面临对靶点特异性不高、向肿瘤核心部位穿透力不足等问题。与研究较多的单抗不同,ADCs药物还需进行特定的药动学和药效学研究,从而优化临床试验设计方案以达到试验目的,上述的因素给ADC药物的临床试验的顺利进行带来了挑战。
其实收益/风险比一直是ADC药物临床研究中的一个关卡。以Mylotarg (gemtuzumab ozogamicin)为例,其是由Pfizer公司研发的ADC药物,曾在2000年获得FDA批准用于治疗CD33阳性60岁以上首次复发的急性骨髓性白血病患者。而在后续的临床试验中临床效果不明显且存在安全隐患,于2010年由Pfizer主动撤出市场。之后Pfizer继续进行Mylotarg的临床研究,在调整了剂量并补充了更多数据后,2017年Mylotarg的收益/风险比终于获得FDA认可,重新上市。
参考来源:
1. AbbVie halts trial of Stemcentrx-sourced ADC for cancer;
2. 抗体偶联药物(ADCs)的原理、影响因素及应用现状。
作者简介:知行,生物化工硕士,从事细胞培养方面的研究。工作之余密切关注国内外医药行业动态以及研究进展,用简单的语言讲述不简单的未来,一个不断前行的医药人。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57