9日,江苏恒瑞医药股份有限公司(以下简称“恒瑞医药”)发布公告称,公司及子公司上海恒瑞医药有限公司近日收到国家食品药品监督管理总局核准签发的《药物临床试验批件》,并将于近期开展 I 期临床试验。
药品基本情况:
药品名称:SHR2554 片
剂型:片剂
申请事项:国产药品注册
注册分类:化学药品第 1 类
申请人:江苏恒瑞医药股份有限公司、上海恒瑞医药有限公司
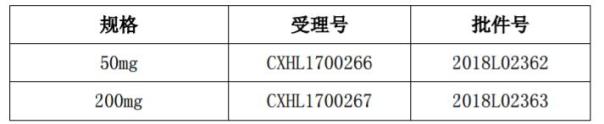
审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,本品符合药品注册的有关要求,批准本品进行临床试验。
据了解,2017 年 11 月 6 日,恒瑞医药和上海恒瑞医药有限公司向江苏省食品药品监督管理局递交的临床试验申请获受理。
SHR2554 拟用于治疗恶性肿瘤。目前,国内外有多个同类产品处于临床研究或临床前开发阶段,但尚无同类产品获批上市,亦无相关销售数据。
截至目前,公司在 SHR2554 及片研发项目上已投入研发费用约为 1350 万元人民币。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57