喜讯,8月11日,alnylam pharmaceuticals公司宣布其研发的RNAi疗法药物Onpattro (patisiran)被美国FDA批准用于治疗遗传性转甲状腺素蛋白淀粉样变性(hATTR)引起的神经损伤,也称家族性淀粉样多发性神经病变(FAP)。这意味着Onpattro成为FDA批准的第一款用于治疗hATTR引起的多发性神经病的药物、美国上市的首款RNAi疗法药物。
关于hATTR
hATTR是一种罕见的进展性、系统性、致死性遗传性神经疾病,该病由于转甲状腺素(TTR,一种转运蛋白)淀粉样变性导致三级结构折叠出错,引起变性蛋白在全身多个器官和组织(包括周围神经、心脏、肠道、眼睛、肾 脏、中枢神经系统、甲状腺和骨髓)中聚集、沉淀,不仅干扰其功能,而且会导致感觉、运动和自主神经功能障碍。hATTR患者常表现混合表型,并经历多发性神经病和心肌病的重叠症状。该病诊出率很低,不到1%。全球大约有5000名hATTR患者,这些患者一般在症状发作的3-15年内就会死亡。
目前hATTR治疗方法有限,迫切需要有新型疗法延缓或者逆转疾病进展。TTR稳定药物,如二氟尼柳和氯苯唑酸可延缓神经病变的进展,但对心肌病变是否有效仍有待进一步研究。而清除已形成淀粉样物质的药物(多西环素/牛磺熊去氧胆酸和抗血清淀粉样物质P抗体)在早期研发阶段。基因沉默(如反义寡核苷酸和小干扰RNA)技术虽初步显示能持续显著抑制突变和野生TTR合成,但多处在临床试验阶段。在此之前获批的hATTR药物有辉瑞的TTR稳定剂Vyndaqel(tafamidis)和美国生物制药公司Ionis Pharmaceuticals的反义核苷酸药物Tegsedi(inotersen),但这些药物都未在美国批准上市。目前hATTR药物的研发情况见下图:
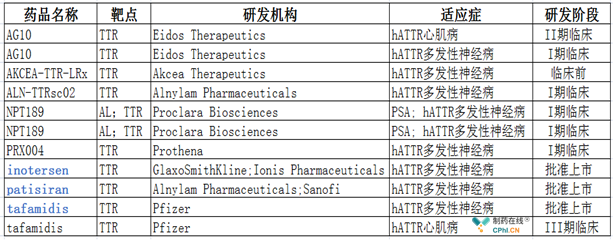
何为RNAi疗法
RNAi即RNA干扰(RNA interference),一种通过双链RNA对基因进行沉默的方法。最初发现RNAi现象的是两位植物学家,他们发现在矮牵牛花中,过量表达查尔酮合成酶(花青素合成通路里的一种限速酶)会使矮牵牛花的颜色变浅,当时他们就猜测从体外引入RNA会对具有同源序列的基因产生"沉默", 但他们一直没有把这个发现转化为实际应用的技术。直到1998年Fire教授与Mello教授发现在线虫里只有注射与基因序列一致,或是高度接近的双链RNA,才能有效地对基因产生沉默,这才使RNAi技术在基础科研中得到广泛应用,并用于研究基因的功能,这种发现也是他们获得了2006年诺贝尔生理学或医学奖。
但RNAi药物选择性、稳定性、免疫原性、过膜性、大规模生产等传统药物不怎么常遇到的技术障碍、以及衍生的递送、安全性等挑战使是RNAi技术的研发困难重重,直到2010年该公司研究发现利用基于配体的技术能实现对RNAi疗法靶向递送,才使RNAi技术看到一丝曙光。
Onpattro获批的基础
Onpattro是一种靶向TTR的RNAi疗法药物,它可以通过靶向和沉默特定信使RNA来阻碍TTR蛋白生成,从而降低引起TTR淀粉样变的TTR蛋白的水平。此次获批是基于一项名为APOLLO的随机、双盲、安慰剂对照的全球性3期临床研究。该研究旨在评估Onpattro在hATTR淀粉样变症患者中的有效性和安全性,覆盖了全球19个国家的44个研究地点,共招募225名hATTR多发性神经病变淀粉样变患者,试验中患者按2:1的比例随机分到Onpattro治疗组和安慰剂对照组,在18个月内Onpattro治疗组患者每三周静脉注射0.3 mg/kg patisiran。该试验主要终点是18个月内修正神经病变损害评分(mNIS + 7)从基线的变化(mNIS + 7是一个神经损伤的综合测量,评估感觉运动能力、神经传导、反射和自主功能)。次要终点是Norfolk QOL-DN生活质量评分以及机械力量(NIS-W)、残疾(R-ODS)、步速(10米步行测试)、营养状况(mBMI)和自主症状(COMPASS-31)。探索性终点包括有心脏介入患者的心脏测量,以及测量皮肤淀粉样负荷和神经纤维密度的皮肤活组织检查。
最终试验结果显示:在18个月期间内,与安慰剂对照组相比,Onpattro治疗组患者在多发性神经病变测量方面有更好的结果,而且在行走、营养状况和进行日常活动能力的评估中也有更高的得分,并且试验组和安慰剂组有类似比例的不良事件(AEs)(分别为96.6%和97.4%)和严重不良事件(SAEs)(分别为36.5%和40.3%)。
此次Onpattro获批,不仅弥补了美国hATTR市场的空白,而且也开创了hATTR治疗的新疗法。同时alnylam pharmaceuticals公司宣布将继续对Onpattro进行研究,以期将其应用于心脏损伤的hATTR病人。
参考资料:
[1] FDA approves first-of-its kind targeted RNA-based therapy to treat a rare disease, Retrieved August 10, 2018, from https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm616518.htm
[2] Alnylam Pharmaceuticals, Retrieved August 10, 2018, from http://www.alnylam.com/
作者简介:Dopine,注册执业药师,河南省药学会会员,就职于河南省某三级甲等医院PIVAS,精于临床药学服务,专注临床用药安全和不合理用药。对国内外医药审评审批政策,研发动态,新药注册审批等长期关注。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57