2019年02月22日,Alder BioPharmaceuticals(后简称“Alder”)宣布向FDA递交CGRP抗体eptinezumab上市申请,适应症为(急性/慢性)偏头痛。药物递交上市申请时间早于预期,对于Alder,这是一个颇具里程碑意义的事件,eptinezumab是Alder首个处于上市审评阶段的药物。Eptinezumab也将成为全球第4款CGRP抗体药物,本文关注eptinezumab关键临床试验数据,并概述全球CGRP单克隆抗体/小分子药物管线以及2018年市场业绩。
一. 全球第4款CGRP抗体药物:eptinezumab
截至目前,eptinezumab在急性、慢性偏头痛患者中开展2项随机、双盲、安慰剂对照的3期临床试验,汇总如下:
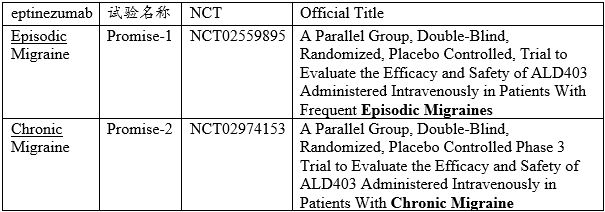
这2项注册临床试验数据已经公布,核心数据如下:
Promise-1:PRevention Of Migraine via Intravenous eptinezumab Safety and Efficacy 1
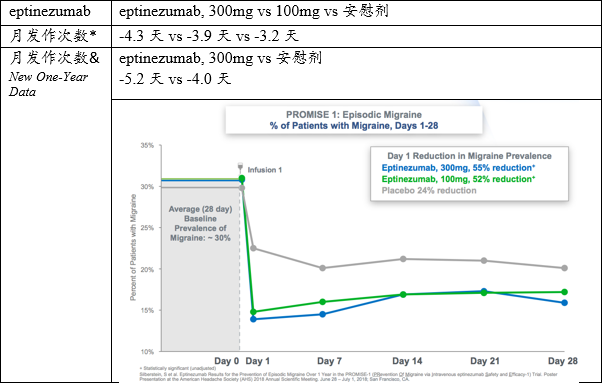
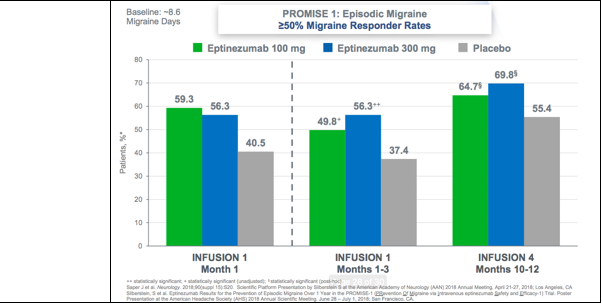
*top-line数据,详见https://investor.alderbio.com/news-releases/news-release-details/alder-biopharmaceuticals-announces-positive-eptinezumab-phase-3
& New One-Year Data数据,详见
1. https://investor.alderbio.com/news-releases/news-release-details/alder-biopharmaceuticalsr-presents-new-one-year-data-eptinezumab
2. https://investor.alderbio.com/static-files/01aab079-f31d-4687-b3c5-5b090285c904
Promise-2:PRevention Of Migraine via Intravenous ALD403 Safety and Efficacy 2
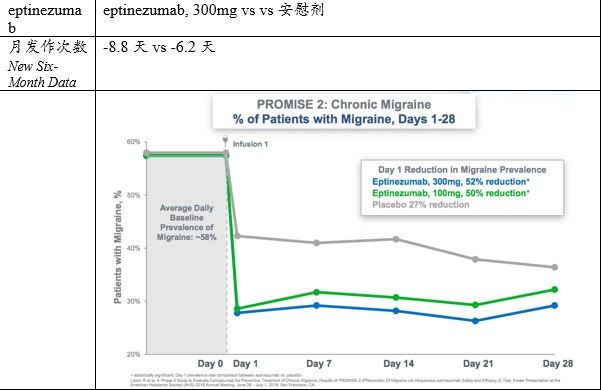
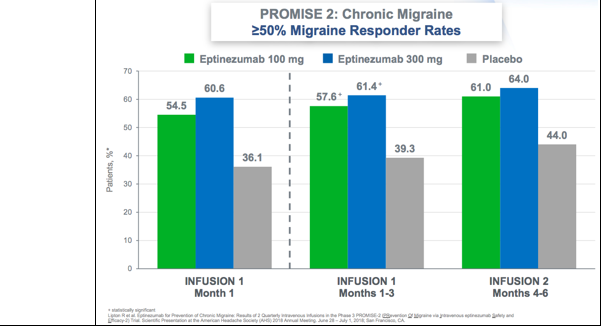
综上,Promise-1(1年数据)和Promise-2 (6月数据)显示,eptinezumab 相比安慰剂能够明显降低急性或慢性偏头痛患者的月发作次数,同时eptinezumab能够给偏头痛患者带来持续的临床获益。
二.eptinezumab上市之路已经扫清障碍
Alder 与Teva 双方对eptinezumab核心专利曾有纷争,目前,双方已达成CGRP抗体和解协议,eptinezumab上市之路已经扫清障碍。
2018年,01月08日,Alder 和 Teva联合宣布达成EP 1957106 B1专利和解协议,协议确认:
1. Teva专利的合法权益,Alder将获得Teva的抗CGRP抗体专利的非独家许可,用于在美国和全球(日本、韩国除外)开发、生产和商业化eptinezumab。
2. Alder将撤回在欧洲专利局的上诉,并立即向Teva支付2500万美元的款项,在获得美国FDA批准的生物制剂许可证申请(BLA)之后,再次向Teva支付2500万美元。
三. 全球CGRP市场2024年预计可达50亿美金
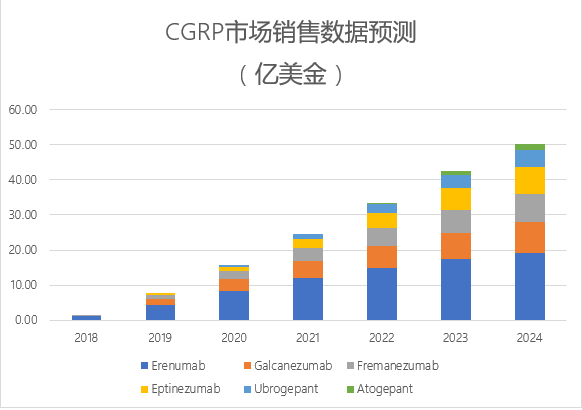
截至目前,全球范围内值得关注的靶向CGRP的药物有7款,其中4款属于单克隆抗体,3款属于小分子药物,Evaluate Pharma预测,2024年全球CGRP市场规模为50亿美金,4款CGRP抗体位列TOP4。
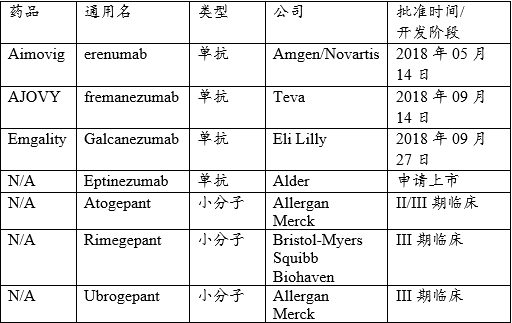
2018年,安进/诺华、Teva、Eli Lilly开发的CGRP单抗相继获批上市,定价$6900/年,其中,安进/诺华Aimovig (erenumab) 为同类首款CGRP单克隆抗体药物,此类药物的获批上市具里程碑意义,药物开启偏头痛新一代治疗方案。
相关公司财报数据显示,Aimovig (erenumab),AJOVY(Fremanezumab) ,Emgality (Galcanezumab) 2018年销售额分别为1.19亿美元,490万美元,300万美元。2019年销售额继续积极、快速增长,预计分别为5亿美元,2亿美元,1亿美元。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57