2019年05月28日,Viela Bio, Inc. ("Viela") 与豪森药业达成一项inebilizumab开发和商业化合作协议,双方将共同推进该CD19单抗在视神经脊髓炎谱系疾病(neuromyelitis optica spectrum disorder)、自身免疫性疾病以及血液癌症在中国的开发。同时,豪森药业将会支付Viela总计至少2.2亿美元里程碑付款(包括首付款、里程碑款以及销售分成)。
Inebilizumab是一款靶向CD19的人源化单抗,Viela开发,核心专利为WO2008031056,专利中能够看出该抗体是由鼠源单抗克隆HB12b人源化后得到,笔者认为人源化后的克隆HB12B-(3-72JH4)重链可变区和HB12B-3649轻链可变区,即为单抗inebilizumab的重链和轻链可变区序列,IgG1Kappa,请分别参考同族专利CN103694349A的序列106和111,本文文末展示,感兴趣的读者也可以查看专利。
目前,inebilizumab是Viela开发进展最快的一个药物,其他2个临床阶段的产品分别为VIB4920 (CD40L-Tn3融合蛋白), VIB7734 (ILT7单抗)。视神经脊髓炎谱系疾病是inebilizumab开发中最受关注的一个适应症,适应症的关键临床试验N-MOmentum (NCT02200770) 已达到临床终点,同时,FDA授予药物突破性疗法和孤儿药资格,预计在2019年年中递交上市申请,Soliris (Eculizumab)将是该药物一个强大的竞品,Eculizumab预计在2019年06月28日获批用于视神经脊髓炎谱系疾病!
一. Inebilizumab:视神经脊髓炎谱系疾病成功达临床终点
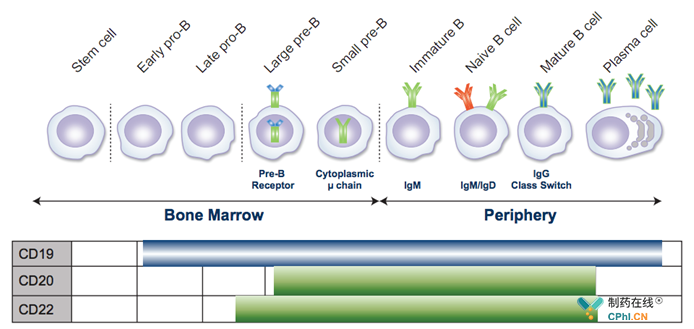
Overview of B-Cell Lineage
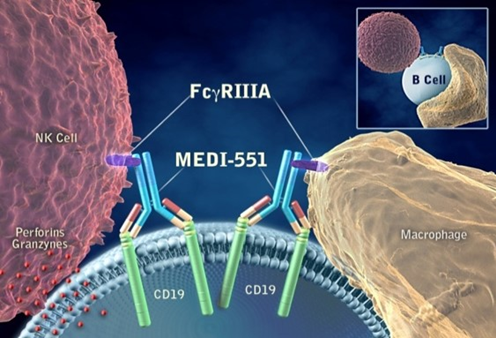
Inebilizumab,参考官网
视神经脊髓炎谱系疾病,主要由靶向aquaporin-4的自身抗体引起,CD19广泛表达于各个阶段的B淋巴细胞,在前B淋巴细胞同样表达,inebilizumab可靶向并清除CD19+ 浆细胞,减少自身抗体的产生,这是inebilizumab治疗视神经脊髓炎谱系疾病的基本理论基础!
N-MOmentum (NCT02200770) 临床数据
N-MOmentum:A Double-masked, Placebo-controlled Study With Open Label Period to Evaluate MEDI-551 in Neuromyelitis Optica and Neuromyelitis Optica Spectrum Disorders
数据更新于AAN 2019 年会
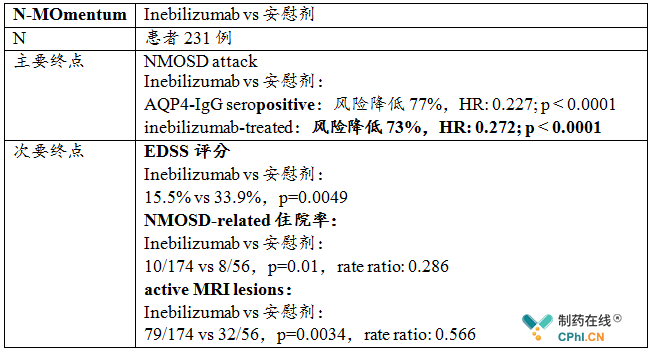
N-MOmentum是一项注册临床试验,备受关注,2019年05月07日,数据更新于AAN 2019 年会,N-MOmentum达到临床主要终点和所有次要终点,inebilizumab vs 安慰剂能够显著降低患者NMOSD attack风险(-73%),同时有效减缓疾病恶化,降低NMOSD住院率以及改善NMOSD 患者MRI 病灶活跃度。
Viela 2018年从阿斯利康剥离,inebilizumab将会是该公司第一个递交BLA的药物,预计2019年年中递交上市申请。其他2个临床阶段的产品分别为VIB4920 (CD40L-Tn3融合蛋白), VIB7734 (ILT7单抗)。
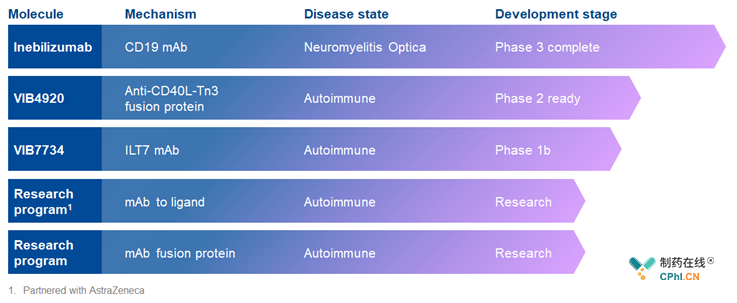
参考官网
二. Inebilizumab的强大竞品:Soliris (Eculizumab)
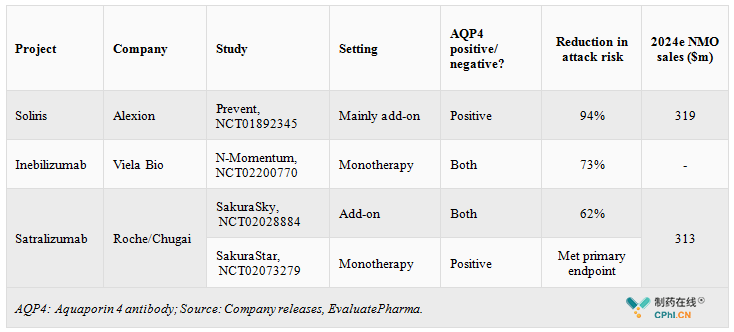
上表中为NMOSD中3款进展最快的药物,其中,Soliris (Eculizumab)已经于2019年02月22日递交该适应症的上市申请,预计2019年06月28日批准,药物定位于辅助疗法,这是其与Inebilizumab不同的一个点;
Inebilizumab目前已完成关键临床试验,定位单药疗法,招募患者230例,AQP4 positive患者占比91%,能够使AQP4 positive患者NMOSD attack风险降低77%,该结果与Eculizumab无法直接对比,Prevent临床试验中患者同时使用了免疫抑制剂!
罗氏Satralizumab是另外一个值得关注的产品,但是相较于上面两个抗体,其临床效果逊色不少,辅助疗法时,NMOSD attack风险-62%,单药疗法已达到临床终点,但是尚未公布具体数据,后续可继续关注!
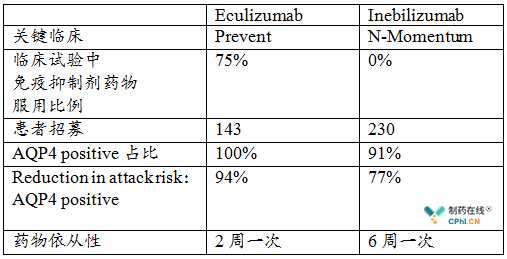
Eculizumab vs Inebilizumab:
Inebilizumab重链可变区序列

Inebilizumab轻链可变区序列

点击下图,观众预登记成功送20元话费



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57